固体溶解度的概念 知识点题库
含有铵根离子的物质称为农业生产中的铵态氮肥,如表是氮肥氧化铵不同温度下的溶解度:
温度℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 |
溶解度(g/100g水) | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.0 | 60.2 |
(1)从表中可知:在70℃时,50g水中最多溶解氯化铵 克.
(2)烧杯A是70℃时,含有100g水的氯化铵不饱和溶液,经过如图的变化过程(在整个过程中不考虑水分的蒸发),则到C烧杯时,溶液的质量为 g.
(3)如图所示,是对氯化铵性质的探究实验:

①图1说明氯化铵溶液水会热量;
②图2是观察到湿润红色石蕊试纸变色;
③农业生产中 (填“能”或“不能”)将铵态氮肥与碱性物质混用.
溶液在生产和科研中具有广泛的用途。请回答下列问题:
(1)每年5月12日为全国“防灾减灾日”。家庭准备云南白药、碘酒、红药水、双氧水、高锰酸钾等杀菌消毒、止血、防感染的药品,是很好的预防措施。
①碘酒的溶剂为 ,双氧水中的溶质为(填化学式) 。
②高锰酸钾由(填数字) 种元素组成。
(2)在我国青海湖地区有一种说法:冬天捞碱,夏天晒盐。这里的碱指的是Na2CO3 , 盐指NaCl,两种物质的溶解度曲线如右图表示。
①10 ℃时,100 g水中最多溶解碳酸钠 g。
②40 ℃时,碳酸钠的溶解度(填字母序号) 氯化钠的溶解度。
a.大于 b.等于 c.小于
③请根据两种物质的溶解度曲线图说明我国青海湖地区冬天捞碱的原因为 。
右图是A、B两种物质的溶解度曲线,根据图示回答下列问题:
(1)t1℃时,向两只盛有100g水的烧杯中,分别加入A、B两种物质至不能溶解为止,所得溶液的溶质质量分数较大的是 溶液(填“A”或“B”)。
(2)t2℃时,欲配制等质量的A、B两种物质的饱和溶液,所需水的质量关系是A B。 (填写“>”、“<”或“=”,下同)
(3)将t2℃的A、B两种物质的饱和溶液各200g,降温至t1℃,析出晶体的质量关系是A B。
(4)将t2℃的A、B两种物质的饱和溶液各200g,升温至t3℃,欲使它们仍为饱和溶液,若不改变溶剂质量,所需加入固体溶质的质量关系是A B。

-
(1) N点的意义是.
-
(2) 温度为t1℃时,a、b、c三种物质的溶解度从大到小的顺序是(用“>”连接,下同).
-
(3) 将t3℃时a、b、c三种物质的饱和溶液都降温到t1℃,三种溶液中溶质的质量分数由大到小的顺序为.
-
(4) 现有一定质量的b溶液,将该溶液在50℃下恒温蒸发10克水后析出了2克b晶体,再恒温蒸发5克水后,又析出了2克b晶体,则b物质在50℃时的溶解度是.


-
(1) 随温度升高,溶解度减小的物质是。
-
(2) 甲和乙的溶解度相同时,温度是。
-
(3) 分别将甲、乙、丙三种物质的饱和溶液从t2℃降到t2℃,降温后甲、乙、丙三种溶液的溶质质量分数由大到小的顺序是。
-
(4) 将150g甲的饱和溶液从t3℃降到t2℃后,向其中加入50g水,此时所得溶液的溶质质量分数是(计算结果精确到0.1%)。
|
温度(℃) |
10℃ |
20℃ |
30℃ |
40℃ |
60℃ |
80℃ |
100℃ |
|
溶解度(g/100g水) |
35.8 |
36.0 |
36.1 |
36.4 |
37.1 |
38.0 |
39.2 |
①80℃氯化钠的溶解度是g/100g水。
②20℃时,15g水中溶解g氯化钠刚好形成饱和溶液。
③粗盐(含有泥沙的氯化钠)提纯的实验过程如图一所示,溶液A是溶液(选填“饱和”或“不饱和”);操作Ⅱ是。


④操作Ⅲ过程中溶液质量与时间变化关系示意图如图二所示,相关分析正确的是(选填编号)
a.m3=20g
b.L、P表示的溶液,溶质质量分数相同
c.(m2-m1)是减少的水的质量
d.N点时,停止加热

|
温度/℃ |
10 |
20 |
30 |
40 |
50 |
60 |
70 |
80 |
90 |
|
|
溶解度/g |
KCl |
31.0 |
34.0 |
37.0 |
40.0 |
42.6 |
45.5 |
48.3 |
51.1 |
54.0 |
|
KNO3 |
20.9 |
31.6 |
45.8 |
63.9 |
85.5 |
110 |
138 |
169 |
202 |
|
-
(1) 两种物质的溶解度随温度变化较大的是 。
-
(2) 40℃时氯化钾的饱和溶液中溶质与溶液的质量比为 。
-
(3) M是两种物质中的一种,取35gM进行如下实验:

溶质质量分数最大的是(填字母);属于不饱和溶液的是(填字母)。
-
(1) 表3是氯化钠和碳酸钠在不同温度时的溶解度,根据此表回答:
温度/℃
10
20
30
40
溶解度/g
氯化钠
35.8
36.0
36.3
36.
碳酸钠
12.2
21.8
39.7
53.2
表3
① 40℃时,氯化钠的溶解度为g。
②碳酸钠的溶解度随温度的升高而(填“增大”或“减小”)。在20℃时,
将100g的水加入30 g碳酸钠中,充分搅拌后得到的是(填“饱和溶液”或“不饱和溶液”),将上述溶液升温到30度,该溶液的溶质质量分数为 (计算结果精确到0.1%)。
③10℃时,分别配制表中两种物质的饱和溶液,其中溶质质量分数较小的物质是。
-
(2) 将足量的稀盐酸加入一定量的铁、铜混合物中,写出其中反应的化学方程式。图7是实验过程生成气体或剩余固体的质量随反应时间的变化关系,其中表示正确的是(填标号)。


-
(1) 乙中的溶液为 (填“饱和”或“不饱和”)溶液;
-
(2) 该固体物质在当时温度下的溶解度为 ;
-
(3) 甲、乙、丙、丁中溶液的溶质质量分数的大小关系是。

| 温度/℃ | 10 | 20 | 30 | 60 | 80 | 100 |
| 溶解度/g | 20.9 | 31.6 | 45.8 | 110 | 169 | 246 |
|
温度/℃ |
0 |
10 |
20 |
30 |
40 |
50 |
|
NH4Cl溶解度/g |
29.4 |
33.3 |
37.2 |
41.4 |
45.8 |
50.4 |
|
NaCl溶解度/g |
35.7 |
35.8 |
36.0 |
36.3 |
36.6 |
37.0 |
-
(1) 由表中数据可知溶解度随温度变化较大的物质是。
-
(2) 氯化钠与氯化铵溶解度相等的温度在℃之间。
|
温度/℃ |
10 |
20 |
30 |
40 |
|
|
溶解度/g |
Na2CO3 |
12.2 |
21.8 |
39.7 |
48.8 |
|
NaCl |
35.8 |
36.0 |
36.3 |
36.6 |
|
|
NaHCO3 |
8.2 |
9.6 |
11.1 |
12.7 |
|
-
(1) 由上表可知,在10℃﹣40℃之间溶解度随温度变化最小的物质是(填名称)。
-
(2) 由表中数据可知,氯化钠和碳酸钠都属于(填“易溶”、“可溶”或“难溶”)物质。
-
(3) 20℃时,将等质量的三种表中物质的饱和溶液升温至40℃,所得溶液中溶质的质量分数由大到小的顺序是(用化学式表示)。
-
(4) 制碱原理为向饱和的NaCl溶液中通入足量NH3和CO2生成NaHCO3晶体和NH4Cl,NaHCO3加热分解即制得纯碱。结合上表分析,析出NaHCO3晶体的原因可能有(填序号)。
A溶剂质量减少
B同温下NaHCO3溶解度小于NaCl
C生成的NaHCO3质量大于消耗的NaCl质量
|
温度℃ |
0 |
10 |
20 |
30 |
40 |
50 |
60 |
|
|
溶解度/g |
NaCl |
35.7 |
35.8 |
36.0 |
36.3 |
36.6 |
37.0 |
37.3 |
|
KNO3 |
13.3 |
20.9 |
31.6 |
45.6 |
63.9 |
85.5 |
110 |
|
-
(1) 两者的溶解度受温度影响较小的是。
-
(2) 20℃时,某同学进行了如下实验,得到相应溶液①~④。

其中,①~④中是饱和溶液的是
 填序号,下同
填序号,下同  ,溶质质量分数相等的是①和。若再将②和④中溶液降温至
,溶质质量分数相等的是①和。若再将②和④中溶液降温至 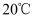 ,所得溶液质量较大的是
,所得溶液质量较大的是  填化学式
填化学式  溶液。
溶液。
|
物质 |
NaOH |
AlCl3 |
Al(OH)3 |
|
溶解度/g |
109 |
69.9 |
0.0015 |
-
(1) 配制溶液。其中配制20℃时100g 饱和氯化铝溶液的基本步骤是∶称取氯化铝固体—量取水—溶解—装瓶贴标签。
①称取氯化铝固体的质量g。(保留小数点后一位)
②量取水加入烧杯溶解。
③装瓶后贴标签,在标签上填写∶
-
(2) 进行性质探究实验。20℃时,根据数据回答下列问题∶
向氯化铝溶液中通入氢氧化钠直至过量,先生成 Al(OH)3 , 再转化为 NaAlO2 , 可观察到的现象是;Al(OH)3与氢氧化钠的反应方程式反应。
温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 |
KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 |
KCl | 27.6 | 31.0 | 34.0 | 37.0 | 40.0 | 42.6 | 45.5 | 48.3 |
回答下列问题:
-
(1) 20℃时,KCl的溶解度为g。
-
(2) 依据表中数据,绘制KNO3和KCl的溶解度曲线,下图中能表示KCl溶解度曲线的是(选填“a”或“b”)。

-
(3) 20℃时,向10g水中加入2.5gKNO3充分搅拌得到X,再加入2.5gKNO3充分搅拌得到Y,继续升温至50℃得到Z,则X、Y、Z中为饱和溶液的是。
-
(4) 40℃时,现有质量均为100g的硝酸钾和氯化钾两种饱和溶液,若将它们同时降温至10℃。下列说法正确的是。
A 40℃时,硝酸钾饱和溶液中水的质量大于氯化钾饱和溶液中水的质量
B 降温至10℃时,析出的KNO3晶体质量比析出的KCl晶体质量大
C 降温至10℃时,硝酸钾饱和溶液的质量分数大于氯化钾饱和溶液的质量分数
D 当温度降至20℃和30℃之间的某一温度,两种溶液的质量分数可能相等

|
温度 |
KNO3 |
NaCl |
|
20℃ |
31.6g |
36.0g |
|
30℃ |
45.8g |
36.3g |
- 按我国温度带和干湿区的划分,福建省属于 A.暖温带、湿润地区
- “两个凡是”的实质是 () A.坚持思想 B.对“”的否定 C.要把晚年的“左”倾错误延续下去 D. “左”倾教条主义的
- 根据下列表格的对应值:x 0.00 0.25 0.50 0.75 1.00 x2+5x﹣3 ﹣3.00 ﹣1.69 ﹣0
- 易中天在《帝国的终结》中说“秦,虽死犹存,它亡得悲壮。”从政治上看“秦,虽死犹存”最主要是指( ) A.统一度量衡、货
- 有机物是一种扁桃酸衔生物。下列关于该有机物的说法正确的是( ) A.该有机物的分子式为C9H10O3Br B.分子中
- 豆类、动物肝脏中含有丰富的铁和锌,这里的“铁”、“锌”是指() A.原子 B.分子 C.元素 D.单质
- (8分)如图A~G是初中化学常见的物质,其中A为黑色固体,E为红色固体,B、C、D通常均为无色气体,F为一种不含氢元素的
- 2001年2月11日晚上,在中央电视台“实话实说”节目中,为了揭露各种歪理邪说,司马南与主持人崔永元合作表演了“铁锤砸砖
- 商务部等九部委决定从2009年8月至2010年2月,在全国范围内开展打击借“家电下乡”等名义制售假劣产品专项整治活动,这
- 舟过谢潭三首(之一)(3分)风头才北忽成南,转眼黄田到谢潭。仿佛一峰船外影,褰帷急看紫巉岩。【小题1】本诗第二句中的“转
- 现有等质量甲、乙、丙三种金属,分别放入三份溶质质量分数相同的足量稀硫酸中,产生氢气的质量与反应时间的关系如右图所示(已知
- 一战改变了人们的思想观念,战后出现的两大社会思潮是( )①社会主义思潮②民族主义思潮③孤立主义思潮④和平主义思潮A
- 二战后主要资本主义国家经济高速发展的原因不包括
- 判断下列属于地域文化的是 A.北京的汉堡 B.济南的烤鸭 C.苏州的
- (2011年四川内江,13题)小红同学在化学实验课上建议,用碘水可将淀粉溶液与食盐溶液区别开来,这个环节属于科学探究中的
- 在“红桃5、红桃7、红桃9”这三张扑克牌中任取一张,抽到“红桃7”的概率是A. B. C.
- 从“只生一个好”到“农村适当放宽生育两孩的条件”,再到“単独二孩”,然后再到全面放开二胎,随着人口与经济社会的发展形势,
- 8.阅读下面这首诗歌,然后回答问题。 登岱 [清]陆次云 得过三观古[注],因上岱宗颠。 海吸长河远,天包大地圆。
- 如图是温带草原生态系统食物网的一部分图解。请据图分析回答。(1)该食物网含________条食物链,猫头鹰占有的营养级是
- 按时间先后,正确的顺序是( )①清政府设置台湾府 ②郑成功收复台湾 ③荷兰



