固体溶解度的概念 知识点题库

-
(1) 图中一处明显错误的操作是 (填序号),改正操作后,用上述图示的序号表示配制溶液的正确操作顺序 .
-
(2) 现配制100kg这种溶液,需氯化钠 kg;
-
(3) 现用质量分数为12%的氯化钠溶液(密度约为1.09g/cm3),配制50g质曼分数为6%的氯化钠溶液.需要质量分数12%的氯化钠溶液 mL(计算结果精确到0.1),需要水 mL(水的密度为1g/cm3).
-
(4) 20℃时,向50g水中加入20g氯化钠,充分溶解后,得到溶液的质量为68g,则20℃时,氯化钠的溶解度为 g.
温度/℃ | 10 | 20 | 30 | 40 | 50 |
KCl | 30g | 33g | 35g | 38g | 41g |
KNO3 | 21g | 31g | 45g | 65g | 88g |
NaCl、KNO3两种物质的溶液度曲线图如图所示,请回答:

-
(1) 由图可知,20℃时氯化钠的溶解度为g.
-
(2) 依据图分析下列问题:50℃时,将氯化钠、硝酸钾固体各40g 分别加入两只各盛有100g水的烧杯中,充分搅拌,其中(填写物质化学式)得到饱和溶液;另一种物质的溶液中再加 入 g该溶质,溶液恰好饱和;若将温度都降到20℃,硝酸 钾溶液中溶质的质量分数(填“>”“<”或“=”)氯化钠溶液中溶质的质量分数.
-
(1) 过去,水曾被看成是一种元素,1781年英国科学家卡文迪许发现,在氢气与氧气的混合气中点火后会有水球生成。微观示意图如下所示:
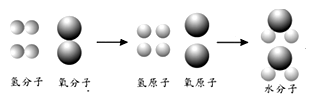
上述变化的微观实质为。
-
(2) 1783年拉瓦锡通过实验合成了水,还将水分解为氢气和氧气,确认了水是由组成的(填化学用语)。
-
(3) 水是最重要的溶剂。已知20℃时,氯化钠的溶解度为36g,20℃时把20g氯化钠放入50g水中,形成溶液的质量为g,该溶液中含有的粒子有(填化学用语)。

 时,进行了如下图所示的实验,下列叙述正确的是:
时,进行了如下图所示的实验,下列叙述正确的是: 

-
(1) 甲和乙的溶解度相等时的温度为
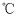 ;
;
-
(2) 上述实验过程中,属于不饱和的溶液的是(填字母,下同);溶液中溶质的质量分数相同的是。
-
(3) 将
 时,等质量的甲、乙饱和溶液降温至
时,等质量的甲、乙饱和溶液降温至  ,所得溶液中溶剂的质量甲乙(填“
,所得溶液中溶剂的质量甲乙(填“ 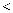 ”、“
”、“  ”或“
”或“  ”)。
”)。
-
(4) 将
 时,
时,  甲的饱和溶液降温至
甲的饱和溶液降温至  时,析出晶体的质量
时,析出晶体的质量 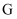 .
.


 ℃时NaCl和KNO3饱和溶液升温到40℃,KNO3溶液的溶质质量分数大于NaCl溶液的溶质质量分数
℃时NaCl和KNO3饱和溶液升温到40℃,KNO3溶液的溶质质量分数大于NaCl溶液的溶质质量分数
|
温度(℃) |
10 |
20 |
30 |
40 |
60 |
80 |
100 |
|
|
溶解度(g/100g水) |
硝酸钾 |
20.9 |
31.6 |
45.8 |
64 |
110 |
169 |
246 |
|
氯化钠 |
35.8 |
36 |
36.3 |
36.4 |
37 |
38.4 |
39.8 |
①从含有80g硝酸钾和9g氯化钠的混合物中提纯硝酸钾,进行如下实验(实验中不考虑各种损耗)

Ⅰ80℃时,硝酸钾的溶解度是。
Ⅱ80℃时,“溶液1”是(选填“饱和”或“不饱和”)溶液。将此溶液恒温蒸发50g水,降温至20℃,所得“溶液3”中硝酸钾的溶质质量分数是。
Ⅲ“溶液2”中硝酸钾质量(选填“<”“>”或“=”)“溶液3”中硝酸钾质量。
Ⅳ若固体M是纯净物,为得到更多固体M,“溶液3”最多还可以恒温蒸发g水。
②20℃时,在100克水中分别放入等质量的硝酸钾和氯化钠,都形成了饱和溶液,如右图所示。

请用两种不同的方法鉴别A和B烧杯中的物质,写出方法、现象与结论。
方法一。
方法二。
-
(1) 汽水中的气态溶质是(填化学式),打开瓶盖会有气体溢出,其原因是压强(填“增大”或“减小”),气体的溶解度减小。
-
(2) 厨房中的下列物质中放入足量水中,能得到溶液的是____(填字母序号)。A . 食盐 B . 蔗糖 C . 食用碱 D . 花生油 E . 面粉
-
(3) 氯化钠和蔗糖的溶解度如下表所示:
温度/℃
20
40
60
80
100
溶解度/g
氯化钠
36.0
36.6
37.3
38.4
39.8
蔗糖
203.9
231
287.3
362.1
487.2
①氯化钠和蔗糖都属于(填“易溶”、“可溶”、“微溶”、“难溶”)物质。
②若蔗糖中混入了少量的食盐,可以用(填“蒸发结晶”或“降温结晶”)的方法提纯蔗糖。
③若向60℃的100g水中加入250g蔗糖,可形成g蔗糖溶液,若将此溶液降温至20℃,可析出晶体g。
温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | |
溶解度/g | NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 |
NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | |
-
(1) 50℃时,NaCl的溶解度是g。
-
(2) 如图是NaCl和NH4Cl的溶解度曲线,则NH4Cl的溶解度曲线是(填“a”或“b”)。t℃时,若饱和NaCl溶液和饱NH4Cl溶液中溶质的质量相等,则下列说法错误的是(填字母)。

A.两种溶液中溶剂的质量相等
B.两种溶液中溶质质量分数相等
C.t℃大于20℃
-
(3) 20℃时,将mgNaCl不饱和溶液平均分为三份,并分别进行如下操作:



据此分析,x=,mgNaCl不饱和溶液中水的质量为g。

-
(1) 在t2℃时,向盛有10ga物质的烧杯中加入10g水,充分溶解后,所得溶液的质量为g。
-
(2) t2℃时,a、b、c三种物质的饱和溶液各100g,所含溶剂的质量由大到小的顺序是。
-
(3) 将t1℃时,将盛有c的饱和溶液的小试管放入盛水的烧杯中(如图2),向烧杯中加入一定量的氢氧化钠固体后,试管中产生的现象是。

-
(1) t1℃时,三种物质的溶解度由大到小的顺序是。
-
(2) t2℃时,使b的饱和溶液变为不饱和溶液,可采用的方法有。
-
(3) t2℃时,将40g a物质加入到50g水中充分搅拌,得到g溶液。
温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 |
溶解度/g | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 |
-
(1) 由表中数据可知,硝酸钾属于(填“易溶”“可溶”“微溶”或“难溶”)物质。
-
(2) 由表中数据可知,硝酸钾的溶解度随温度升高而。
-
(3) 使硝酸钾饱和溶液变为不饱和溶液,可采用的一种方法是。
- 将10mol A和5molB放入10L真空箱内,某温度下发生反应:3A(气)+B(气) 2C(气)在最初0.2s内,消耗
- pH是水质监测的重要指标之一,下列水样酸性最强的是() A.pH=1.3的工业废水 B.pH=4.5的雨水 C.pH=7
- 已知,Rt△ABC,,AB = AC,BC = 10,则△ABC的面积为_________.
- 下图所示的军队臂章开始出现在A.北伐战争时期 B.国共十年对峙时期 C.抗日战争时期 D.人民解放战争时期
- 已知为等差数列,为其前项和,若,,则_________
- 如图表示细胞有丝分裂一个细胞周期所用的时间,下列说法正确的是 A、 甲→乙的过程表示分裂间期 B、 乙→甲的
- 根据右侧经纬网地图,完成3-5题。3.关于A、B、C三点所在半球的说法,正确的是 A.三点均在北半球
- 2012年11月,有甲、乙、丙、丁四架飞机以同样的速度沿所在纬线自西向东飞行(如下图),据此回答36~37题。36.四架
- 完形填空 Sam is eleven years old. One day, his friend Tony says
- 读南昆铁路分布示意图,完成相关问题。(9分)(1)在现代运输系统中,铁路运输的主要优点是_____________,__
- 某烃的结构简式是,它不可能具有的性质是 A.它能使溴水褪色,也能使酸性KMnO4溶液褪色 B.易溶于水,也易溶于有机溶剂
- 今年,教育部直属师范大学将招收一批免费师范生,学生毕业后须回生源所在省份的中小学任教十年以上,你愿意成为一名免费师范生吗
- The bank is reported in the local newspaper, in broad da
- 英国君主立宪制的本质是( ) A.封建的政权组织形式 B.资产阶级的政权组织形式 C.封建主义和资本主义
- 已知函数f(x)=ax3-x2+cx(a≠0)的图像如下所示,它与x轴仅有两个交点O(0,0)和A(xA,0)(xA&g
- 农民诗人王老九受到新中国领导人的接见,回乡后,他走街串巷用自己的诗歌宣传党在过渡时期的总路线,他领导的互助组经过整顿,发
- 下列关于多核心模式的叙述,错误的是() A.城市可以围绕多个不同的核心点发展起来 B.城市中心商务区并不一定居于城市的几
- 如图为某地东亚飞蝗种群数量变化示意图,下列叙述错误的是( )A.为有效防治蝗灾,应在a点之前及时控制种群密度 B.a~
- 幂函数f(x)=x,若0<x1<x2,则f(),大小关系是( ) A.f()> B.f()< C.f()= D.无法
- 目前,中国人口的男女性别比已经达到了116.9:100,这也就意味着在中国重男轻女的观念仍然存在,下列关于这种观念形成的



