空气 知识点题库

-
(1) (探究一)影响过氧化氢分解速率的因素有哪些? 兴趣小组同学做了四个实验,实验数据如下表:
实验
序号
H2O2 溶液的溶质质量分数%
H2O2 溶液的体积/mL
温 度
/℃
MnO2的用量/g
收集O2的体积/mL
反应
时间
①
5
1
20
0.1
4
16 s
②
15
1
20
0.1
4
6 s
③
30
5
35
0
4
98 min
④
30
5
55
0
4
2 0min
对比③④两组实验,可得出过氧化氢分解速率与温度的关系:当过氧化氢溶液的体积和浓度等其它条件相同时,。
-
(2) 能说明过氧化氢的分解速率与其质量分数有关的实验是填实验序号)。
-
(3) (探究二)其他金属氧化物能否起到类似 MnO2 的催化作用?
兴趣小组同学用天平称量 0.2 g CuO,用量筒量取 5 mL 5% 的H2O2溶液,进行如下图所示实验(①~⑦代表实验操作步骤)。

小组同学通过上述实验得出结论:CuO 可作过氧化氢分解的催化剂,支持该结论的实验证据是。
-
(4) 欲比较不同催化剂 CuO 和 MnO2对H2O2 分解速率的影响,实验时需要控制的变量有。
-
(5) 过氧化氢能被MnO2 催化分解放出氧气的文字(或符号)表达式为。

[提出问题]这瓶气体中氧气的体积分数是多少?
-
(1) [实验验证]活动小组设计了如图两套实验装置,用来测定该瓶气体中氧气的体积分数:在氮气环境下,将过量的铜粉分别装入干燥的硬质玻璃管和具支试管后,密封。用两支干燥的注射器从该瓶中抽取气体,分别按图示连接,推拉注射器一段时间后,用酒精灯在铜粉部位加热,加热时反复推拉注射器至反应完全。甲装置比乙装置更合理,理由是,用甲装置测定氧气的体积分数,需要测定的实验数据是。
-
(2) [反思交流]实验完毕,待装置冷却后,应先将气球内的气体全部挤出,再读数,否则会使测得结果(填 偏大或偏小或无影响),原因是。
-
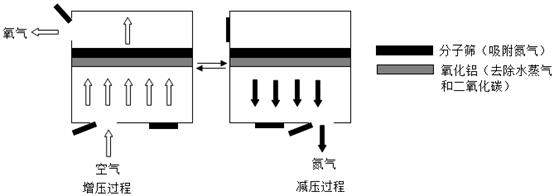
(1) 下列说法正确的是 (填序号)。
A 变压吸附法制取的氧气中含有稀有气体
B 变压吸附法制取的氧气中含有二氧化碳
C 分子筛对氮气的吸附能力与吸附塔内气体压强有关
-
(2) 另一种分离氧气和氮气的方法是先将空气液化,再利用氮气和氧气沸点的差异进行分离。
资料:常压下,氧气的沸点是-183℃,氮气的沸点是-196℃。 分离时,氮气和氧气的状态是 (填序号)。
A
B
C
D
氧气
液态
液态
气态
气态
氮气
液态
气态
液态
气态
 检查装置的气密性
C .
检查装置的气密性
C .  检验氧气是否集满
D .
检验氧气是否集满
D .  检验氢气的纯度
检验氢气的纯度


-
(1) 写出图中标示①的仪器名称:①。
-
(2) 实验室用KMnO4制取O2 , 应选用的发生和收集装置为(填字母序号,)取用KMnO4药品时,应选用仪器A,写出该反应的化学方程式。
-
(3) 注射器C与装置E相连可用于检查装置E的气密性,步骤如下:
①向锥形瓶中加入少量水至浸没过长颈漏斗下端处。
②将注射器C连接到装置E的导管口处。
③缓慢拉动注射器C的活塞,观察到,说明装置E的气密性良好。
-
(1) 空气中O2所占的体积分数约为。
-
(2) 含有较多可溶性钙、镁化合物的水为(“硬水”或“软水”)。
-
(3) 净化水的操作有①过滤②蒸馏③静置沉淀等多种,其中净化程度最高的操作是(填序号)。
-
(4) 下图所示为电解水的实验,该实验证明水是由组成的,该反应的化学方程式为。

-
(5) 工业生产中,水可作为多种反应的反应物,写出将一氧化氮和氧气通入水中制备硝酸的化学方程式。

 C . 实验完毕,并冷却到室温,左管水面上升约至“1”刻度处
D . 用木炭代替白磷也能得到相同的结果
C . 实验完毕,并冷却到室温,左管水面上升约至“1”刻度处
D . 用木炭代替白磷也能得到相同的结果

-
(1) 装置D中仪器a的名称是。
-
(2) 实验室用装置B制取氧气,反应的化学方程式为。
-
(3) 实验室制取氢气选用的装置组合是。
-
(4) 若用F装置收集二氧化碳。气体应从(填“m”或“n”)端通入。
|
实验编号 |
过氧化氢溶液的质量分数/% |
过氧化氢溶液的用量/mL |
催化剂(二氧化锰)的用量g |
反应温度/℃ |
收集气体体积/mL |
所需时间/S |
|
① |
20 |
5 |
0.1 |
85 |
20 |
3.8 |
|
② |
15 |
2 |
0.2 |
20 |
20 |
2.8 |
|
③ |
5 |
2 |
0.2 |
20 |
20 |
7.4 |
|
④ |
20 |
5 |
0.1 |
55 |
20 |
10.5 |
|
⑤ |
15 |
2 |
0.1 |
20 |
20 |
21.6 |
数据如上表,请你一同参与他们的探究,并回答下列问题。
(提出问题)过氧化氢溶液分解制氧气速率与哪些因素有关?
(猜想与假设)兴趣小组中三位同学分别作出如下猜想:
A同学:与过氧化氢溶液的质量分数有关
B同学:与催化剂的用量有关
C同学:与反应温度有关
(实验与结论)
-
(1) 请写出该实验涉及的反应的文字表达式:。
-
(2) 实验(填序号)证明A同学的猜想是正确的,B同学的猜想的依据是实验(填序号)。
-
(3) C同学得出的结论是。
-
(4) (拓展探究)请你再设计出一个方案,进一步探究其它影响过氧化氢溶液分解制氧气速率的因素(写出猜想、方法)
-
(1) 下列仪器中:①的名称是;组装氧气发生装置时,应选择(填序号)。

-
(2) 研究显示:氧气的体积分数大于36%时就可使带火星的木条复燃。因此,氧气验满时采用使带火星的木条复燃的方法(填“可靠”或“不可靠”)。为了收集一瓶较纯净的氧气,最好采用集气法。化学方程式为。

-
(1) 写出仪器的名称:②;⑤。
-
(2) 实验室用高锰酸钾粉末制取氧气,宜选用的发生装置是(填序号),该装置需要进行的改进是:,目的是。若要收集较纯净的氧气,需要选择(填C、D或者E)装置,这种收集气体的方法称为集气法,氧气可以用该方法收集是因为。若用C装置收集氧气,检验氧气集满的方法是。
-
(3) 实验用氯酸钾制氧气,有下列操作:①固定试管,加热②检查气密性③向试管中装药品④有均匀气泡时开始收集⑤实验完毕,撤导气管⑥熄灭酒精灯。其正确的顺序是。
-
(4) 实验室用过氧化氢制氧气的文字或符号表达式是:。B和F两个装置都可作该反应的发生装置。试选其中一个装置,并指出其优点。装置:,其优点是。

-
(1) 写出双球管中一个可能发生的化学反应方程式。
-
(2) 挤压右滴管并微热燃烧管,白磷燃烧而红磷不燃烧,由此得出燃烧的一个条件为。
-
(3) 挤压左滴管可观察到燃烧的白磷熄灭,其灭火的原理为。
- 人体甲状旁腺细胞能够摄取氨基酸作为原料合成某种分泌蛋白。下图为人体甲状旁腺细胞示意图,请分析回答:(1)人体甲状旁腺细胞
- “谢太傅寒雪日内集,与儿女讲论文义”这一句总述了谢太傅家人咏雪的背景,极精炼地交代了时间“________”、地点“__
- 划船的事各人在数天以前就早有了准备,分组分帮,各自选出了若干身体结实、手脚伶俐的小伙子,在潭中练习进退。船只的形式,和平
- 森林中的鸟类有垂直分层现象。这种现象主要与下列哪一因素有关 A. 温度 B.食物种类 C
- 肾脏结构和功能的基本单位是( ) A 肾小球 B 肾小囊 C肾小管
- 金属是生产与生活中的重要材料 (1)下列铁制品的用途中,利用金属延展性的是 (填字母)。
- Liu Yang is the first Chinesewoman astronaut_______ has ever
- 对果树进行压条时,需要把压条的树皮环割一圈,环割后剥圈以下的侧芽会迅速发育成侧枝,这是因为( ) A.顶芽不再会
- 如图2-3-16所示,光滑的球半径为10 cm,悬线长L=50 cm,物体B厚20 cm,重12 N,B物体与墙之间的动
- 阅读下文,回答问题。(5分) 农夫耕田 农夫耕于田,数息而后一锄。行者①见而笑曰:“甚矣,农之惰也!数息而后一锄,此田终
- 为保证司乘人员的安全,轿车上设有安全带未系提示系统。当乘客坐在座椅上时,座椅下的开关S1闭合,若未系安全带,则开关S2
- 如图所示装置气密性良好、要使注射器中的活塞向右移动,使用的液体M和固体N可能是()①稀盐酸和石灰石;②稀硫酸和锌;③水和
- 下列各句中,加点的词语使用恰当的一句是( ) A.储藏谷物的仓库,在稻谷入仓之前,要事先做好清洁工作。 B.与会的代
- 柳宗元在《封建论》中说:“秦有天下,裂都会而为之群邑,废侯卫而为守宰。……此其所以为得也。”这句话指的是
- 如图,在△ABC中,∠C=90°,M是AB的中点,动点P从点A出发,沿AC方向匀速运动到终点C,动点Q从点C出发,沿CB
- 将长势相同、数量相等的甲、乙两个品种的大豆幼苗分别置于两个相同的密闭透明玻璃罩内,在光照、温度等相同且适宜的条件下培养,
- After work I went to the boxoffice to buy the tickets for Ku
- 下列结构属于组织的是( ) A.皮肤 B.肌腱 C.神经纤维 D.唾液腺
- (20分)阅读下列材料 材料一:观察比较右边两幅图 材料二:(明太祖)罢丞相不设,析中书省之政归六部,以尚书任天下事,侍
- 某物理学习小组的同学设计了如图甲所示的电路测量电源的电动势和某定值电阻的阻值。其中F为电源(内阻不计).R为电阻箱(0~



