影响化学反应速率的因素探究 知识点题库
实验室常用的制取气体的发生装置如下:

-
(1) 仪器a的名称是;搭建B装置时,酒精灯应在固定仪器a之(选填“前”或“后”)放置.
-
(2) 实验室用过氧化氢溶液和二氧化锰混合制取氧气,反应的化学方程式是 .
-
(3) 在实验室制取二氧化碳的研究中,进行了如下实验:
试验编号
药品
甲
乙
丙
丁
大理石
mg,块状
mg,块状
mg,粉末状
mg,粉末状
盐酸(过量)
wg,稀盐酸
wg,浓盐酸
wg,稀盐酸
wg,浓盐酸
Ⅰ.上述实验中反应的化学方程式是 .
Ⅱ.若要研究盐酸浓度大小对反应的影响,可选择实验甲与对照(选填实验编号)
Ⅲ.除盐酸的浓度外,上述实验研究的另一个影响反应的因素是 .
Ⅳ.研究发现酸的浓度越大,产生气体的速度越快,与甲比较,对丁分析正确的是 (选填编号)
a.反应更为剧烈
b.最终剩余溶液的质量更小
c.产生二氧化碳的质量更大
d.粉末状大理石利用率更高
-
(4) 下表中的两个实验,尽管在原料状态、发生装置等方面存在差异,却都能控制气体较平稳的产生.请从实验目的、原理、原料、装置、操作等方面思考后,具体阐述每个实验中气体较平稳产生的最主要的一个原因.
目的
原料
发生装置
气体较平稳产生的最主要的一个原因
制取二氧化碳
块状大理石
稀盐酸
A
制取氧气
粉末状二氧化锰
3%的过氧化氢溶液
C
为比较相同浓度的FeCl3溶液和CuSO4溶液对H2O2分解的速率影响效果,某研究小组进行了如下探究: 
-
(1) 【定性研究】如图甲,可通过观察来定性比较两者的速率影响效果.
-
(2) 【定量研究】如图乙,实验前检查该装置气密性的方法是.要定量比较两者的速率影响效果,可测量生成等体积气体所需的.
-
(3) 【深入研究】在FeCl3溶液中,究竟是哪种粒子影响过氧化氢的分解速率?
猜想1:水分子(H2O)影响过氧化氢的分解速率;
猜想2:影响过氧化氢的分解速率;
猜想3:影响过氧化氢的分解速率;…
请设计实验,验证猜想
实验操作
实验现象
实验结论
分别取同温度同体积同浓度的H2O2溶液于2支试管中,再分别加入等质量的FeCl3和NaCl.观察现象.
加入FeCl3的试管中产生的气体快,加入NaCl的试管中产生的气体慢.
证明是Fe3+影响过氧化氢的分解速率
-
(4) 【反思与讨论】上述实验确实可以证明Fe3+可以改变过氧化氢的分解速率,但不能证明FeCl3是过氧化氢分解的催化剂.若要证明FeCl3是过氧化氢分解的催化剂,还需要通过实验证明FeCl3在反应前后.
请写出FeCl3催化H2O2分解的化学方程式.
(1)上述实验中发生反应的化学方程式有① ;② ;
(2)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验,将表中所给的混合溶液(混合前后溶液的体积变化忽略不计)分别加入到6个盛有过量等量锌粒(锌粒与溶液的接触面积相同)的反应瓶中,收集产生的气体,记录获得同样多的气体所需的时间.
实验 混合溶液 | A | B | C | D | E | F |
28%稀硫酸/m/L | 30 | V1 | V2 | V3 | V4 | V5 |
饱和CuSO4溶液m/L | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
H2O/mL | V7 | V8 | V9 | V10 | 8 | 0 |
①请完成此实验设计,其中:V1= ;V6= ;V9= ;
②反应一段时间后,实验A中的金属呈色;
③该同学最后得出的结论为:当加入少量CuSO4溶液时,生成氢气的速率会大大提高,但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降.请分析氢气生成速率下降的主要原因 .
【实验方案】常温下,在两瓶相同体积的H2O2溶液中分别加入相同质量MnO2和红砖粉,测量各生成一瓶(相同体积)O2所需要的时间.
【进行实验】如图是他们进行实验的装置图写出反应的化学方程式,实验中B处宜采用的气体收集方法是
【实验记录】
实验编号 | 1 | 2 |
反应物 | 6%H2O2 | 6%H2O2 |
催化剂 | 1g红砖粉 | 1gMnO2 |
时间 | 152秒 | 35秒 |
【结论】该探究过程中得出的结论是
【反思】H2O2生成O2的快慢还与哪些因素有关?请你帮助他们继续探究.
【假设】
【实验方案】.


 又称蓝矾,化学式:
又称蓝矾,化学式:  ,在试管中加入
,在试管中加入  胆矾,然后分别加入3mL不同浓度的硫酸,30分钟后若胆矾的颜色改变,说明硫酸具有脱水性。实验结果见表
胆矾,然后分别加入3mL不同浓度的硫酸,30分钟后若胆矾的颜色改变,说明硫酸具有脱水性。实验结果见表  资料:
资料:  蓝色晶体,
蓝色晶体,  白色晶体,
白色晶体, 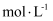 是某种浓度的单位
是某种浓度的单位 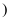
表1硫酸脱水性实验结果
| 硫酸浓度 | 16 | 15 | 14 | 13 | 12 | 11 | 10 | 9 | 8 |
| 晶体颜色 | 变化 | 变化 | 变化 | 变化 | 变化 | 变化 | 不变 | 不变 | 不变 |
-
(1) 胆矾由种元素组成。
-
(2) 将胆矾加入试管前进行研磨的原因是,实验室常用的研磨仪器是。
-
(3) 证明胆矾被浓硫酸脱水的实验现象是,实验结果表明,浓度大于等于
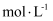 的硫酸均具有脱水性。
的硫酸均具有脱水性。
-
(4) 硫酸铜溶液不能存储在铁制品中的原因是
 用化学方程式表示
用化学方程式表示 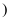 。
。
-
(5) 根据表2回答问题:
表2不同温度下各质量分数浓度的硫酸密度
 单位:
单位: 
 浓度
浓度 时密度
时密度 时密度
时密度 时密度
时密度 时密度
时密度15




20




25




 从表中数据分析,浓硫酸密度和温度的关系:。
从表中数据分析,浓硫酸密度和温度的关系:。 从表中数据分析,浓硫酸密度和浓度的关系:。
从表中数据分析,浓硫酸密度和浓度的关系:。

-
(1) 吸收塔中,用NaOH溶液吸收
 ,化学反应方程式是.NaOH溶液喷成雾状能充分吸收
,化学反应方程式是.NaOH溶液喷成雾状能充分吸收  的原因是
的原因是
-
(2) 氧化室中,化学反应方程式是.
-
(3) 已知部分原料的价格如表所示.
试剂
Ca(OH)2
NaOH
价格(元/kg)
0.36
2.90
上述工业流程中,处理相同量的
 ,双碱法所需的原料成本比用NaOH直接吸收更低,原因是.
,双碱法所需的原料成本比用NaOH直接吸收更低,原因是. -
(4) 某中学化学兴趣小组为测定工厂周围的空气中的二氧化硫含量是否符合国家标准,将
 周围空气通入一定含量碘(
周围空气通入一定含量碘(  )2.54mg的碘水中,经测定
)2.54mg的碘水中,经测定  与二氧化硫恰好完全反应,该反应的化学方程式是
与二氧化硫恰好完全反应,该反应的化学方程式是  。通过计算说明此烟气排放后周围空气中二氧化硫的浓度级别。
。通过计算说明此烟气排放后周围空气中二氧化硫的浓度级别。 [资料信息:我国空气质量标准对空气中二氧化硫的浓度级别规定如下表所示(空气中二氧化硫的浓度用单位体积的空气中所含二氧化硫的质量表示)]。
浓度级别
标准(mg·m-3)
一级
浓度≤0.15
二级
0.15<浓度≤0.50
三级
0.50<浓度≤0.70
| 实验① | 实验② | 实验③ |
| | | |

-
(1) Ⅰ.制取氧气
过氧化氢溶液与二氧化锰制取氧气的文字表达式为。
-
(2) 能用排水法收集氧气的原因是。
-
(3) 若要检验生成的气体是否为氧气,可将导管从水中取出,取带火星的木条放在导管口处,观察到,说明生成的气体是氧气。
-
(4) Ⅱ.探究过氧化氢分解速率的影响因素
实验1:取6 mL30%的过氧化氢溶液进行实验,数据如下表:
实验序号
1-1
1-2
1-3
温度/℃
20
35
55
二氧化锰的用量/g
0
0
0
收集氧气的体积/mL
0
1.9
7.8
反应时间/分
40
40
40
由此得出影响过氧化氢分解速率的因素之一是。
-
(5) 实验2:取50 mL5%的过氧化氢溶液与不同质量的二氧化锰进行实验,数据如下表:
实验序号
2-1
2-2
2-3
2-4
2-5
温度/℃
20
a
20
20
20
二氧化锰的用量/g
0.1
0.3
0.5
0.7
0.9
收集氧气的体积/mL
80
195
570
570
570
反应时间/分
1
1
1
1
1
实验2-2中,a为。
-
(6) 根据实验2判断,下列说法正确的是(填序号)。
A 在一定范围内,二氧化锰的用量越大,过氧化氢分解速率越快
B 其它条件相同时,二氧化锰对过氧化氢的催化效果与其用量有关
C 用过氧化氢溶液制取氧气时,加入的二氧化锰越多越好
[查阅资料]
Ⅰ. Fe3O4 与盐酸反应,得到FeCl2和FeCl.3的混合溶液
Ⅱ.用溶质质量分数一定的FeCl2和FeCl3溶液进行如下实验,为方案设计提供参考
|
FeCl2溶液 |
FeCl3溶液 |
|
|
加入Fe |
无明显变化 |
溶液变成浅绿色 |
|
加试剂A |
无明显变化 |
溶液变成红色 |
-
(1) [实验过程]
甲、乙两组同学分别用酒精灯和酒精喷灯作为热源进行CO还原Fe2O3的实验,检验得到的黑色固体的成分,实验记录如下:
实验操作
实验现象
结论与解释
①取少量的黑色固体于试管中,滴加适量的
②向步骤①所得的溶液中,滴加试剂A
甲组:固体溶解,无气泡冒出
加试剂A后,溶液变成红色
黑色固体的成分是
乙组:固体溶解,加试剂A后,溶液颜色无明显变化
黑色固体的成分是Fe
-
(2) [实验反思]
你认为下列说法正确的是(填序号)。
a 温度会影响反应的产物
b 试剂A用于检验FeCl3溶液
c进行CO还原Fe2O3的实验时,一定要进行尾气处理
-
(3) 小明认为乙组的实验结论有欠缺,黑色固体的成分还可能是Fe和Fe3O4的混合物。你认同小明的观点吗?请说明理由。
-
(1) 硬水是含有(写出一种离子符号)较多的水。
-
(2) 自然界中的水都不是纯水,利用沉淀、过滤、吸附和等方法可以净化水。
-
(3) 从微观角度解释:实验室将固体药品配成溶液进行化学反应,为什么能提高反应速率?。


-
(1) 写出如图所示装置中标有序号的仪器名称:②。
-
(2) 实验室用过氧化氢溶液和二氧化锰混合制取氧气,组装好仪器后,应先,反应的符号表达式为。
-
(3) 甲烷是一种无色无味,难溶于水,密度比空气小的气体,实验室常用加热无水醋酸钠和碱石灰的固体混合物制取甲烷,发生装置应选,甲烷收集完毕后集气瓶应放(填“正”或“倒”)。某气体只能用E装置收集,则该气体可能具有的性质为(填字母序号);
a能与水反应 b能与空气反应 c密度与空气接近
-
(4) 氧气是一种化学性质比较活泼的气体,它可以和许多物质发生反应。
①请写出下图两个反应的符号表达式:

甲,乙。
下述两个反应的相同点是(填序号)。
a都是化合反应 b都是氧化反应 c生成物都是固体 d都需要点燃
②在做甲实验时,事先需在集气瓶底部装有少量水,甲中的水作用是:。
-
(5) 研究性学习小组选择“H2O2生成O2的快慢与什么因素有关”的课题进行探究,以下是他们探究的主要过程:
①(假设一)H2O2生成O2的快慢与催化剂种类有关
(实验方案)常温下,在两瓶同质量、同浓度的H2O2溶液中,分别加入相同质量的MnO2和水泥块,测量各生成一集气瓶(相同体积)O2所需的时间。
(进行实验)如图是他们进行实验的装置图,气体发生装置中A仪器名称是,此实验中B处宜采用的气体收集方法是。
-
(6) (实验记录)

实验编号
1
2
反应物
5%H2O2
5%H2O2
催化剂
lg水泥块
1gMnO2
时间
165秒分
46秒
(结论)该探究过程得出的结论是。②(假设二)。
-
(7) (实验方案)同温下取2份质量相等、质量分数不同的H2O2溶液,,结果质量分数大的过氧化氢溶液生成的氧气快,先收集满集气瓶。
|
实验 序号 |
过氧化氢 溶液浓度/% |
过氧化氢 溶液质量/g |
温度 /℃ |
二氧化锰 用量/g |
氧气 体积/ml |
反应所需 时间/s |
|
① |
5 |
12 |
20 |
0.2 |
125 |
11 |
|
② |
30 |
12 |
20 |
0.2 |
125 |
2 |
|
③ |
30 |
12 |
40 |
/ |
125 |
148 |
|
④ |
30 |
12 |
90 |
/ |
125 |
82 |
-
(1) 通过实验①和②对比可知,化学反应快慢与有关,其关系是。
-
(2) 通过实验对比可知,化学反应快慢与温度的关系是。
-
(3) 除了上述的两个因素能影响化学反应快慢,你认为另一个影响因素是什么,其关系是怎样的?。
-
(4) 由上述实验可知,实验室用过氧化氢制取氧气的最合适的条件是(用文字详述)。
(查阅资料)蜡烛燃烧时,生成的CO2与CO的浓度比越大,蜡烛燃烧越充分。
(进行实验)利用下图装置完成实验(所用传感器分别为O2、CO、CO2浓度传感器)。

| 实验序号 | 容器情况 | 蜡烛位置 | O2起始浓度 | CO2与CO的浓度比 | 熄灭时O2浓度 |
| 1 | 敞口(模拟通风环节) | 如图1 | 21% | 1205.1 | 持续稳定燃烧,保持在20.4%左右不变 |
| 2 | 半敞口(模拟有烟囱的环境) | 如图1 | 21% | 1202.2 | 持续稳定燃烧,保持在20.3%左右不变 |
| 3 | 密闭 | 如图1 | 21% | 223.7 | 约16% |
| 4 | 密闭 | 如图2 | 21% | 255.6 | 约16% |
| 5 | 密闭 | 如图3 | 21% | 270.6 | 约16% |
| 6 | 密闭 | 如图3 | 22% | 344.9 | 约16% |
| 7 | 密闭 | 如图3 | 23% | x | 约16% |
-
(1) (解释与结论)
蜡烛燃烧时会生成CO2和CO,说明蜡烛中一定含有元素。
-
(2) 检验蜡烛燃烧有CO2生成,可在蜡烛火焰上方罩一个内壁涂有的烧杯。
-
(3) 对比实验2和3,蜡烛在条件下燃烧更充分(填“半敞口”或“密闭”)。
-
(4) 对比(填实验序号),可得出“其他条件相同时,蜡烛的位置越分散,燃烧越充分”。
-
(5) 实验5、6、7的目的是。
-
(6) x344.9(填“>”、“=”或“<”)。
-
(7) (反思与评价)
综合以上实验分析,下列说法正确的是___________(填字母序号)。
A . 蜡烛燃烧可以消耗尽密闭容器内氧气 B . 蜡烛充分燃烧,可减少污染 C . 实验1中氧气浓度基本不变,是因为分子在不断运动 D . 燃料在氧气浓度较高的富氧空气中燃烧,能起到节能减排的作用
-
(1) 探究影响双氧水分解制氧气速率的因素。
该小组组长在500mL软塑料矿泉水瓶中加入100mL5%的医用双氧水,将瓶子捏扁,无明显实验现象。甲、乙两位同学分别采取了以下措施:放入热水中、投入几粒红砖颗粒(如图所示),片刻,发现软塑料矿泉水瓶恢复原型且均收集满了一瓶氧气。由此得出的实验结论是:影响双氧水分解制氧气速率的因素有。写出乙同学探究实验的化学方程式。


-
(2) 探究影响铁生锈速率的因素。
①用棉线将打磨后的铁钉悬挂于甲同学制取的氧气瓶中(如图5中A),另取一相同空瓶只倒入100mL水,也悬挂铁钉(如图中B),旋紧两瓶盖,置于相同环境中。一周后发现A瓶中铁钉生锈更明显,由此得出的实验结论为。
②将B瓶中的水换成等量食盐水进行实验(如图中C),未得到预期的效果。随后他又用等量的白醋代替食盐水(如图中D),铁钉生锈明显比B、C中的快。请帮他分析一下原因。

-
(1) 表示锌粒与稀硫酸的反应是曲线(填“①”或“②”),并写出有关反应的化学方程式。
-
(2) 通过比较c、d两点,说明影响反应速率的因素是什么?。

-
(1) NH4HCO3属于(填“氮”、“磷”、“钾”或“复合”)肥。
-
(2) “造气”是利用煤、空气和水在一定条件下反应获取CO2、N2和H2 , 加快“造气”反应速率的具体措施有(写一点)。
-
(3) “合成”是指N2和H2在一定条件下反应生成氨气,反应的化学方程式为。
-
(4) “循环”是指(填物质名称)的循环利用。
- 下列几何体中,俯视图为四边形的是 A. B. C. D.
- 下图是某种伴性遗传病的家族系谱图(假设该病受一对遗传因子控制,A是显性、a是隐性,):(1)该遗传病是受
- 高安素有“新兴瓷城”的美誉。在陶瓷器制造过程中,一定发生了化学变化的是( ) A.混合 B.成型C.干燥 D.烧
- 如图,两个带电金属小球中心距离为r,带电荷量均为Q,则对于它们之间电荷的相互作用力大小F的说法正确的是( ) A.
- 到了寒冷的冬天,法国梧桐树的叶纷纷落下,而松树依然郁郁葱葱。这表明 ( ) A、法国梧桐不适应寒冷的环境
- ---How did it _________ that all the flowers died ? ---I
- 三个不同的实数成等差数列,且成等比数列,则_________
- 如果□ABCD的对角线相交于点O,那么在下列条件中,能判断□ABCD为菱形的是 (A)∠OAB=∠OBA
- 下列句中加线的词解释错误的一项 A 沛公军霸上(驻军) B 妇女无所幸(封建君主对妇女的宠爱) C 范增说项羽曰(劝说)
- 光合作用过程中,将植物突然从光下移到黑暗中,下图中能表示植物叶绿体中五碳分子含量变化曲线的是()
- Not only interested in football but beginning
- 在某体系内有反应物和生成物5种物质:H2S、S、FeCl3、FeCl2、HCl。已知H2S为反应物,则另一反应物是 (
- 对体液免疫和细胞免疫的表述,不正确的是( ) A.体液免疫中,抗体和抗原发生特异性结合发挥免疫效应 B.细胞免疫中,
- 与北宋签订澶渊之盟的少数民族政权是 A.西夏 B.金
- 如图所示,a、b两个带电小球,质量分别为ma、mb,用绝缘细线悬挂,两球静止时,它们距水平地面的高度均为h(h足够大),
- 与朱元思书 (14分,每题2分,14题4分)①风烟俱净,天山共色。从流飘荡,任意东西。自富阳至桐庐一百许里,奇山异水,天
- 现定义运算“”,对于任意实数a、b,都有如:,若则实数的值是 .
- 矩形内有一点P到各边的距离分别为1、3、5、7,则该矩形的最大面积为 平方单位.
- 下列骨骼肌附着骨的模式图中,正确的是() A. B.
- 下列各句中,加线词语使用不恰当的一句是( ) A.虽然电脑病毒猖獗,但电脑公司总能在第一时间推出新的杀毒软件及时杀毒







