过滤的原理、方法、操作及其应用 知识点题库
下列是实验室中常见的几项化学实验基本操作,其中正确的是( )
A . 测溶液pH
B . 检查装置气密性
B . 检查装置气密性
C . 稀释浓硫酸
C . 稀释浓硫酸
D . 过滤
D . 过滤

B . 检查装置气密性
B . 检查装置气密性
C . 稀释浓硫酸
C . 稀释浓硫酸
D . 过滤
D . 过滤
如图的实验基本操作正确的是( )
A . 称氢氧化钠质量 B . 过滤
B . 过滤 C . 点燃酒精灯
C . 点燃酒精灯 D . 取用液体药品
D . 取用液体药品
 B . 过滤
B . 过滤 C . 点燃酒精灯
C . 点燃酒精灯 D . 取用液体药品
D . 取用液体药品
下图为精制粗盐的示意图,回答:

-
(1) 写出仪器名称①②
-
(2) 蒸发滤液时,玻璃棒起的作用是,图中玻璃棒的作用是.
-
(3) 漏斗中的液面应(填“高”或“低”)于滤纸边缘
-
(4) 粗盐提纯时正确顺序是( )A . 溶解、蒸发、过滤 B . 过滤、蒸发 C . 溶解、过滤、冷却 D . 溶解、过滤、蒸发
下列实验能达到目的的是( )

A . ①检验 CO2 是否收集满
B . ②分离出氯化钠溶液中的氯化钠
C . ③检验蜡烛燃烧生成的水
D . ④用红磷探究空气中氧气的体积分数
硫酸铜晶体是常用于农业和渔业的杀虫剂、杀菌剂。某科学兴趣小组在制备该晶体前通过查阅相关资料,筛选后得到下图所示的两种途径。

(提示:途径Ⅱ的反应为:Cu+2H2SO4(浓)  CuSO4+SO2↑+2H2O)
CuSO4+SO2↑+2H2O)
-
(1) 操作Ⅰ为;
-
(2) 从环保和经济两个角度分析,途径Ⅰ优于途径Ⅱ的原因是:。
-
(3) 该兴趣小组的同学在查阅资料时还发现,锌在常温下也能够和浓硫酸反应。现取足量的锌与一定量的浓硫酸发生反应产生SO2 , 一段时间后,会产生另一种气体A。根据锌的化学性质,推断A气体可能是。
粽子是端午节极具代表性的传统美食之一,乐清人民多习惯食用“碱水粽”,即在制作粽子的过程中加入“碱水”。这不仅让粽子有谷壳般的金黄色泽,味道更是清香软糯。以下是两种制作“碱水”的方法:
【方法一】将纯碱与水的质量按1:99配制,得到“碱水”;
【方法二】收集秸秆放入铁质器皿中燃烧,烧至发黑后灭火,得到草木灰;往草木灰中加入开水溶解,一段时间后,慢慢将浊液倒在盖有纱布的竹篓上,用容器接住流下的水,得到“碱水”。制作流程如下图所示:

-
(1) 方法一中配制的“碱水”溶质质量分数为;
-
(2) 方法二中用盖有纱布的竹篓来得到“碱水”的方法类似于物质分离方法中的法;
-
(3) 在方法二得到的“碱水”中加入稀盐酸,发现有气体产生。请判断该种气体,并写出检验方法:。
分离和提纯的方法很多,常用的方法有过滤、蒸发结晶、蒸馏等,请用以上分离方法填空。除去河水的泥沙可用的方法,从食盐水中得到食盐晶体可用的方法,从自来水中得到蒸馏水可用的方法。
自然界中获取的粗盐含有较多的杂质,需要精制。为了除去粗盐中泥沙等不溶性杂质,设计了如图所示的A、B、C三个步骤。

-
(1) B步骤称为,玻璃棒的作用是。
-
(2) C步骤中,当蒸发皿内出现较多固体时,应该 。( )(填字母)A . 移去酒精灯,停止搅拌 B . 移去酒精灯,用玻璃棒继续搅拌 C . 继续加热蒸干水分,再移去酒精灯
将质量为44.4克含有少量NaCl的纯碱晶体(Na2CO3·nH2O)样品,平均分成A、B、C三份,进行如图实验(Na2CO3受热不分解)。

-
(1) 将A样品与BaCl2溶液反应生成的白色沉淀分离出来的方法是。
-
(2) A样品中与BaCl2溶液反应的Na2CO3的质量是克。
-
(3) B样品中含有结晶水的质量是克。
-
(4) 化学式Na2CO3·nH2O中n是多少?(写出计算过程)
-
(5) 对C样品的操作结束后,所得NaCl溶液中的溶质质量是多少?
如图为精制粗盐的示意图,回答:

-
(1) 写出仪器名称②
-
(2) 漏斗中的液面应(填“高”或“低”)于滤纸边缘。
在治疗新冠肺炎中,中药发挥了重要作用。下列中药煎制步骤与实验室过滤操作原理相同的是( )
A . 冷水浸泡  B . 加热煎制
B . 加热煎制  C . 取液弃渣
C . 取液弃渣  D . 装袋保存
D . 装袋保存 
 B . 加热煎制
B . 加热煎制  C . 取液弃渣
C . 取液弃渣  D . 装袋保存
D . 装袋保存 
秀秀想分离KCl和BaCl2的混合粉末,加入足量的蒸馏水对其进行溶解后,进行如下的实验操作:

-
(1) 操作①中,过滤需要用到的器材有 (可多选)。

-
(2) 为了确定操作②中沉淀A表面是否还有K2CO3和KCl残留,取最后一次洗涤后的液体,加入(填化学式),若没有任何现象,则说明已洗涤干净。
-
(3) 操作⑤中,随着水分的不断蒸发,KCI固体逐渐从溶液中析出,下列表示KCl溶液的溶质质量分数与蒸发水的质量关系正确的是。

某NaCl样品中含有少量BaCl2 , 其提纯流程如下:

-
(1) 写出溶液A中与Na2CO3溶液发生反应的化学方程式:。
-
(2) 操作a的名称是。
-
(3) 溶液B中加适量盐酸的目的是。
实验室要从X、银、铜、锌四种金属混合物中分离它们。流程如下:

请回答:
-
(1) 过滤操作中用到的玻璃仪器有烧杯、漏斗和。
-
(2) 请写出滤液A中加入加入过量的锌,过滤后,所得滤液B中溶质的化学式。
-
(3) 为了检验滤液C中的溶质成分:向其中加入稀盐酸,有白色沉淀产生,则滤液C中一定含有的阳离子。
实验操作,不仅要科学规范,还要关注环保、安全等问题。下列实验操作正确的是( )
A . 装入固体粉末  B . 倾倒液体
B . 倾倒液体  C . 过滤杂质
C . 过滤杂质  D . 获得食盐晶体
D . 获得食盐晶体 
 B . 倾倒液体
B . 倾倒液体  C . 过滤杂质
C . 过滤杂质  D . 获得食盐晶体
D . 获得食盐晶体 
为了确定某含杂质的硝酸钠溶液中所含杂质的成分,某同学设计了如下实验:
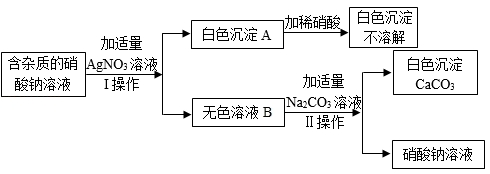
请回答下列问题:
-
(1) I,Ⅱ为操作。
-
(2) 经分析,原溶液中的杂质可能由一种或几种物质组成。杂质的成分可能是:若原溶液中的杂质由一种物质组成,则该杂质是。
我国将力争2060年前实现碳中和,CO2的捕捉可减少碳排放。
-
(1) 下左图是利用NaOH溶液“捕捉”(吸收)CO2部分流程图:


①操作①的名称是。
②捕捉室中NaOH溶液常喷成雾状,优点是。
-
(2) CaO固体也可以捕捉回收CO2 , 化学方程式为CaO+CO2
 CaCO3。研究表明CaC2O4⋅H2O热分解制得的CaO疏松多孔,具有良好的CO2捕捉性能。取1.46gCaC2O4⋅H2O进行加热,固体质量随温度变化如上右图。
CaCO3。研究表明CaC2O4⋅H2O热分解制得的CaO疏松多孔,具有良好的CO2捕捉性能。取1.46gCaC2O4⋅H2O进行加热,固体质量随温度变化如上右图。 ①写出400~600℃范围内分解反应的化学方程式: (CaC2O4⋅H2O的相对分子质量:146)。
②据图分析,CaO捕捉CO2的反应温度应(填“高于”或“低于”)800℃。
某白色固体可能由氯化钠、硫酸钠、碳酸钠中的一种或几种组成。为了确定其成分某同学取适量该白色固体,加水配成溶液后,进行如下实验。

-
(1) 上述中“操作A”的名称是。
-
(2) 根据以上实验结果,白色固体中一定有的物质是。
-
(3) 小明认为,上述实验设计还不能完全确定该白色固体的成分,为了能明确确定白色固体的所有成分,建议换取上述实验中的一种试剂。请问小明建议换取哪种试剂,并说明原因。。
丢弃的废铜屑(其中混有少量铁屑),活动小组的同学欲利用其制取胆矾晶体(CuSO4•5H2O),他们设计了下面的两种制取流程。已知:①Cu+2H2SO4(浓)  CuSO4+SO2↑+2H2O;②2Cu+2H2SO4(稀)+O2
CuSO4+SO2↑+2H2O;②2Cu+2H2SO4(稀)+O2  2CuSO4+2H2O
2CuSO4+2H2O
 CuSO4+SO2↑+2H2O;②2Cu+2H2SO4(稀)+O2
CuSO4+SO2↑+2H2O;②2Cu+2H2SO4(稀)+O2  2CuSO4+2H2O
2CuSO4+2H2O 
请回答:
-
(1) 操作①名称是。
-
(2) 溶液A的溶质有。(写化学式)。
-
(3) 比较上述两种方法,符合绿色化学要求的是方法 (填“Ⅰ”或“Ⅱ”)。
实验室有氧化铜和铁的混合物粉末,为提炼其中的铜,现进行如下操作:

-
(1) 步骤II所需用到的仪器有铁架台、烧杯、。(请再写出两种玻璃仪器)。
-
(2) 溶液C中溶质的化学式为。
-
(3) 现有20g溶质质量分数为98%的浓硫酸,要将其稀释成质量分数为9.8%的稀硫酸,需加水多少毫升?
最近更新
- 2011年5月份,美国密西西比河沿岸多个州市遭遇洪水威胁,造成重大财产损失。为保证“大灾之后无大疫”,防疫人员通过喷洒含
- “三个代表”重要思想的地位和意义在于() ①是新时期党的建设的根本指导思想 ②是对党的性质、宗旨和根本任务的高度概括,发
- 一元二次方程x2+4x=0的解是() A.x=﹣4 B.x1=0,x2=﹣4 C.x=4 D.x1=0,x
- 下面四幅图中等高距相同,则a、b、c、d四处坡度由大到小排列正确的是A.a=b=c=d B.a
- 如图所示,光滑水平面上,一物体以速率向右做匀速直线运动,当物体运动到点时,对它施加一水平向左的恒力.过一段时间,物体向反
- 1......
- 在短文的空格内填入适当的词,使其内容通顺,每空格限填一词,词首字母已给。Abraham Lincoln, the 16t
- 一名维修工需维护三台机器,在一个月内,甲、乙、丙三台机器需维护的概率分别是0.8,0.7,0.6,在一个月中,求:(Ⅰ)
- 已知元素R有某种同位素的氯化物RClX,该氯化物中R微粒核内中子数为Y,核外电子数为Z,该同位素的符号为(
- 下列说法正确的是
- 1837—1901年被英国历史上称为“维多利亚时代”,是他们认为的巅峰时期,下面关于这一历史时期的描述错误的是【
- 为了有效控制酒后驾车,交警的巡逻汽车在一条东西方向的公路上巡逻,如果规定向东为正,向西为负,从出发点开始所走的路程为:
- 要除去混在CO2中的气体杂质:HCl、SO2、H2O等,依次通过的试剂正确的是( ) A.碳酸氢钠溶液、浓硫酸
- 定义:从数列{an}中取出部分项,并将它们按原来的顺序组成一个数列,称为数列{an}的一个子数列.设数列{an}是一个公
- 24.有关单克隆抗体的制备和应用的描述,错误的是: A.对小动物注射特定抗原以获取所需的B淋巴细胞 B.单克隆抗体最广泛
- 二战结束后初期,美国《芝加哥太阳报》指出:“紧接着这位伟大而盲目的贵族所高举的大旗,就会使我们投入这个世界最恐怖的战争中
- 如图是一杯泡好的茶,用手转动茶杯时,我们往往会看见“杯动茶不动”的现象,其原因是
- 我国将试行普通高校、高职院校、成人高校之间学分转换,拓宽终身学习通道。从文化角度看,拓宽终身学习通道是基于( ) A.
- x,y分别为8-的整数部分和小数部分,则2xy-y2=____________.
- she has been to the Summer Palace before. (变反意疑问句) she has



