第2节 电解质的电离 离子反应 知识点题库
能在溶液中大量共存的一组离子是( )
A . Ag+、SO42﹣、Cl﹣
B . Fe2+、H+、NO3﹣
C . K+、Na+、NO3﹣
D . Mg2+、SO42﹣、CO32﹣
能正确表示下列反应的离子方程式的是( )
A . Cl2通入NaOH溶液:Cl2+OH﹣═Cl﹣+ClO﹣+H2O
B . NaHCO3溶液中加入稀HCl:CO32﹣+2H+═CO2↑+H2O
C . AlCl3溶液中加入过量稀氨水:Al3++4NH3•H2O═AlO2﹣+4NH4++2H2O
D . Cu溶于稀HNO3:3Cu+8H++2NO3﹣═3Cu2++2NO↑+4H2O
某溶液能与Al粉反应放出H2 , 该溶液中可能大量共存的离子组是( )
A . NH4+、Ba2+、HCO3-、Cl-
B . K+、Al3+、S2-、ClO-
C . Na+、Fe3+、Cl-、SO42-
D . H+、Mg2+、SO42-、NO3-
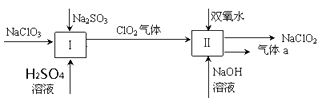
亚氯酸钠(NaClO2)是一种强氧化性漂白剂,广泛用于纺织、印染和食品工业。它在碱性环境中稳定存在。某同学查阅资料后设计生产NaClO2的主要流程如下。(部分产品未标出)
-
(1) Ⅰ中发生反应的还原剂是、Ⅱ中的氧化剂是(填化学式)。
-
(2) Ⅱ中反应的离子方程式是。
-
(3) ClO2是一种高效水处理剂,可用亚氯酸钠和稀盐酸为原料制备:5NaClO2 + 4HCl = 5NaCl + 4ClO2↑+ 2H2O。
①该反应中氧化剂和还原剂的物质的量之比是。
②研究表明:在上述过程中会发生副反应:NaClO2 + 4HCl = NaCl + 2Cl2↑+ 2H2O,若反应开始时盐酸浓度越大,则气体产物中Cl2的含量越大。请推测其原因是。
向某NaOH溶液中通入CO2气体后得到溶液M,因CO2通入的量不同,溶液M的组成也不同,若向溶液M中逐滴加入盐酸,产生的气体体积V(CO2)与加入盐酸的体积V(HCl)的关系如图所示。则下列分析与判断错误的是(不计CO2溶解)( )
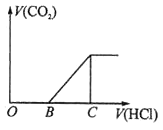
A . 若OB=0,则形成溶液的过程中所发生反应的离子方程式为OH―+CO2═HCO3―
B . 若OB=BC,则溶液M为Na2CO3溶液
C . 若OB>BC,则溶液M中大量存在的阴离子为CO32―和HCO3―
D . 若3OB=BC,则溶液M中c(NaHCO3)=2c(Na2CO3)
下列离子方程式能正确描述实验事实的是( )
A . 镁粉加到氯水中,氯水褪色:Mg+2H+=Mg2++H2↑
B . 双氧水和稀硫酸同时加到84消毒液中,产生大量气泡:ClO-+H2O2=Cl-+H2O+O2↑
C . Na2S、Na2SO3、H2SO4混和溶液中产生淡黄色沉淀:3S2-+SO42-+8H+=4S↓+4H2O
D . 在Fel2溶液中通入Cl2气,溶液颜色变深:2Fe2++Cl2=2Fe3++2Cl-
下列有关离子方程式正确的是( )
A . 稀硝酸和过量的铁屑反应:Fe+4H++NO3-=Fe3++NO↑+2H2O
B . 向硫酸氢钠溶液中加入氢氧化钡溶液至中性,则离子方程式为:2H++SO42-+2OH-+Ba2+=BaSO4↓+2H2O
C . 氯气溶于水:Cl2+H2O⇌2H++Cl-+ClO-
D . 向NaAlO2溶液中通入过量的CO2:2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-
不列离子方程式书写正确的是( )
A . 铜片与稀硝酸反应:3Cu+2NO3-+8H+=3Cu2++2NO2↑+4H2O
B . 将磁性氧化铁溶于盐酸:Fe3O4+8H+=3Fe3++4H2O
C . 碳酸氢钙溶液中加入少量的氢氧化钠溶液:Ca2++HCO3-+OH-=CaCO3↓+H2O
D . 用浓氢氧化钠溶液检验溶液中的NH4+:NH4++OH-  NH3·H2O
NH3·H2O
 NH3·H2O
NH3·H2O
下列物质溶于水中能导电,但不属于电解质的是( )
A . Fe(OH)3
B . Cl2
C . H2SO4
D . C2H5OH
最近《科学》杂志评出“十大科技突破”,其中“火星上‘找’到水的影子”名列第一。下列关于水的说法中正确的是( )
A . 加入电解质一定会破坏水的电离平衡,其中酸和碱通常都会抑制水的电离
B . 水的电离和电解都需要电,常温下都是非自发过程
C . 水电离出的c(H+)=10-7mol/L的溶液一定呈中性
D . 水的离子积不仅只适用于纯水,升高温度一定使水的离子积增大
已知H2S能定量完成下列反应:R-+H2S(少量)  HR + HS- , 2Z-+ H2S(少量)
HR + HS- , 2Z-+ H2S(少量)  2HZ + S2-。下列叙述正确的是
2HZ + S2-。下列叙述正确的是
 HR + HS- , 2Z-+ H2S(少量)
HR + HS- , 2Z-+ H2S(少量)  2HZ + S2-。下列叙述正确的是
2HZ + S2-。下列叙述正确的是
A . 相同温度下电离平衡常数:Ki1(H2S)>Ki(HZ)>Ki2(H2S)>Ki(HR)
B . 结合H+的能力:Z->S 2->R->HS-
C . 同温同浓度下,溶液的pH值:NaHS>NaR>Na2S>NaZ
D . HZ与Na2S反应的离子方程式:HZ +S2-  HS-+ Z-
HS-+ Z-
 HS-+ Z-
HS-+ Z-
下列各组离子在溶液中能大量共存的是( )
A . NH 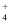 、K+、H+、Ba2+、Cl-、NO
、K+、H+、Ba2+、Cl-、NO  B . Mg2+、Na+、OH-、K+、CO
B . Mg2+、Na+、OH-、K+、CO 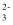 C . Ag+、Fe3+、Cl-、H+、Ca2+
D . K+、CO
C . Ag+、Fe3+、Cl-、H+、Ca2+
D . K+、CO 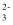 、H+、Na+、NH
、H+、Na+、NH 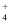
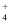 、K+、H+、Ba2+、Cl-、NO
、K+、H+、Ba2+、Cl-、NO  B . Mg2+、Na+、OH-、K+、CO
B . Mg2+、Na+、OH-、K+、CO 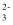 C . Ag+、Fe3+、Cl-、H+、Ca2+
D . K+、CO
C . Ag+、Fe3+、Cl-、H+、Ca2+
D . K+、CO 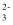 、H+、Na+、NH
、H+、Na+、NH 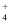
有M、N两溶液,各含下列12种离子中的6种:  、
、  、
、 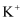 、
、  、
、 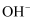 、
、 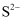 、
、  、
、  、
、  、
、  、
、  、
、  。已知两溶液所含离子各不相同,N溶液里的阳离子只有两种,则M溶液中的阴离子应该是
。已知两溶液所含离子各不相同,N溶液里的阳离子只有两种,则M溶液中的阴离子应该是 

 、
、  、
、 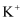 、
、  、
、 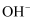 、
、 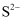 、
、  、
、  、
、  、
、  、
、  、
、  。已知两溶液所含离子各不相同,N溶液里的阳离子只有两种,则M溶液中的阴离子应该是
。已知两溶液所含离子各不相同,N溶液里的阳离子只有两种,则M溶液中的阴离子应该是 

A .  、
、  、
、  B .
B . 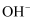 、
、 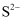 、
、  C .
C . 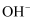 、
、  、
、  D .
D .  、
、  、
、 
 、
、  、
、  B .
B . 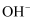 、
、 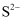 、
、  C .
C . 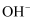 、
、  、
、  D .
D .  、
、  、
、 
有以下10种物质,请回答下列问题:
①干冰 ②氯化钠 ③蔗糖 ④稀硫酸 ⑤NaHSO4溶液 ⑥碳酸氢钠 ⑦氢氧化钡溶液 ⑧冰醋酸 ⑨氯化氢 ⑩NH3
-
(1) 其中能导电的是 (填写符号,下同); 属于电解质的是 ;属于非电解质的是 。
-
(2) 分别写出物质⑤在水中的电离方程式:。
-
(3) 写出物质④和⑦反应的离子方程式:。
-
(4) 写出物质⑤和⑥在水中发生反应的离子方程式:。
-
(5) 写出少量物质⑦和过量的物质⑥发生反应的离子方程式:。
已知:  ,室温下,向
,室温下,向 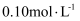 的
的 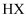 溶液中滴加
溶液中滴加 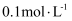 的
的  溶液,溶液
溶液,溶液  随P的变化关系如图,下列说法正确的是( )
随P的变化关系如图,下列说法正确的是( )
 ,室温下,向
,室温下,向 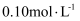 的
的 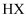 溶液中滴加
溶液中滴加 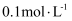 的
的  溶液,溶液
溶液,溶液  随P的变化关系如图,下列说法正确的是( )
随P的变化关系如图,下列说法正确的是( ) 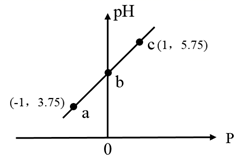
A . a点溶液中: 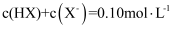 B . b点坐标为
B . b点坐标为 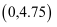 C . c点溶液中:
C . c点溶液中:  D . 溶液中水的电离程度:
D . 溶液中水的电离程度: 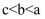
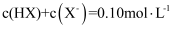 B . b点坐标为
B . b点坐标为 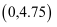 C . c点溶液中:
C . c点溶液中:  D . 溶液中水的电离程度:
D . 溶液中水的电离程度: 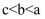
下列离子方程式中正确的是( )
A . 铜与稀硫酸: B . 氯化亚铁与氯气的反应:
B . 氯化亚铁与氯气的反应: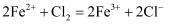 C . 醋酸与NaOH溶液:
C . 醋酸与NaOH溶液: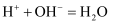 D . 碳酸氢钙溶液与过量烧碱溶液混合:
D . 碳酸氢钙溶液与过量烧碱溶液混合: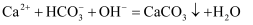
 B . 氯化亚铁与氯气的反应:
B . 氯化亚铁与氯气的反应: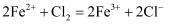 C . 醋酸与NaOH溶液:
C . 醋酸与NaOH溶液: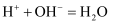 D . 碳酸氢钙溶液与过量烧碱溶液混合:
D . 碳酸氢钙溶液与过量烧碱溶液混合: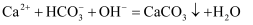
在含有大量Fe3+、H+、SO 的溶液中,一定能大量共存的离子是( )
的溶液中,一定能大量共存的离子是( )
 的溶液中,一定能大量共存的离子是( )
的溶液中,一定能大量共存的离子是( )
A . SCN-
B . Cl-
C . CO D . Ba2+
D . Ba2+
 D . Ba2+
D . Ba2+
向  溶液中滴入几滴酚酞溶液后,匀速逐滴加入
溶液中滴入几滴酚酞溶液后,匀速逐滴加入  溶液,过程中测得混合溶液的电导率变化如下图所示。下列有关说法正确的是( )
溶液,过程中测得混合溶液的电导率变化如下图所示。下列有关说法正确的是( )
 溶液中滴入几滴酚酞溶液后,匀速逐滴加入
溶液中滴入几滴酚酞溶液后,匀速逐滴加入  溶液,过程中测得混合溶液的电导率变化如下图所示。下列有关说法正确的是( )
溶液,过程中测得混合溶液的电导率变化如下图所示。下列有关说法正确的是( ) 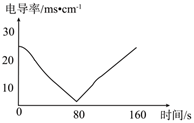
A . 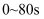 间溶液中仅
间溶液中仅  降低
B . 该反应的离子方程式为
降低
B . 该反应的离子方程式为  C . 溶液颜色逐渐变浅说明
C . 溶液颜色逐渐变浅说明 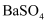 是难溶电解质
D . 由
是难溶电解质
D . 由 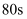 时溶液的导电率数值可推理知
时溶液的导电率数值可推理知  不是强电解质
不是强电解质
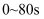 间溶液中仅
间溶液中仅  降低
B . 该反应的离子方程式为
降低
B . 该反应的离子方程式为  C . 溶液颜色逐渐变浅说明
C . 溶液颜色逐渐变浅说明 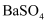 是难溶电解质
D . 由
是难溶电解质
D . 由 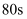 时溶液的导电率数值可推理知
时溶液的导电率数值可推理知  不是强电解质
不是强电解质
下列实验中,实验设计或所选装置合理的是 ( )
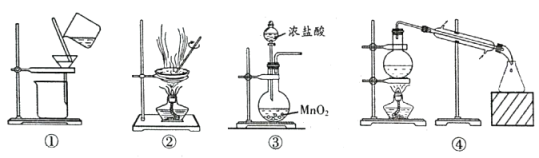
A . 用图①和图②所示装置进行粗盐提纯
B . 用图②所示装置在通风橱中高温灼烧 制取
制取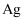 C . 用图③所示装置制备氯气
D . 用图④所示装置进行石油分馏实验制取汽油
C . 用图③所示装置制备氯气
D . 用图④所示装置进行石油分馏实验制取汽油
 制取
制取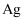 C . 用图③所示装置制备氯气
D . 用图④所示装置进行石油分馏实验制取汽油
C . 用图③所示装置制备氯气
D . 用图④所示装置进行石油分馏实验制取汽油
在两份相同的 溶液中,分别滴入物质的量浓度相等的
溶液中,分别滴入物质的量浓度相等的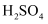 、
、 溶液,其导电能力随滴入溶液体积变化的曲线如图所示。下列说法正确的是( )
溶液,其导电能力随滴入溶液体积变化的曲线如图所示。下列说法正确的是( )
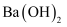 溶液中,分别滴入物质的量浓度相等的
溶液中,分别滴入物质的量浓度相等的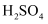 、
、 溶液,其导电能力随滴入溶液体积变化的曲线如图所示。下列说法正确的是( )
溶液,其导电能力随滴入溶液体积变化的曲线如图所示。下列说法正确的是( )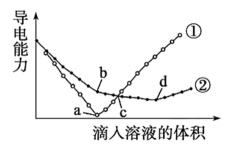
A . ①代表滴加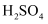 溶液的变化曲线
B . a处溶液的导电能力几乎为0,所以
溶液的变化曲线
B . a处溶液的导电能力几乎为0,所以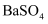 是非电解质
C . c点两溶液中
是非电解质
C . c点两溶液中 的物质的量关系:①
的物质的量关系:①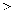 ②
D . b~d的离子方程式为
②
D . b~d的离子方程式为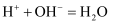
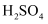 溶液的变化曲线
B . a处溶液的导电能力几乎为0,所以
溶液的变化曲线
B . a处溶液的导电能力几乎为0,所以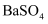 是非电解质
C . c点两溶液中
是非电解质
C . c点两溶液中 的物质的量关系:①
的物质的量关系:①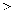 ②
D . b~d的离子方程式为
②
D . b~d的离子方程式为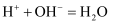
最近更新
- 甲、乙两坩埚内均分别装入NaHCO3粉末,甲中装入纯净的NaHCO3,乙中混有少量Na2CO3杂质,两者固体总质量相等。
- 与流入肾脏的血液相比,从肾脏流出的血液所含的成分特点是( ) A.二氧化碳减少了
- ,长河落日圆。 (王维《使至塞上》)
- 爱国主义是中华民族精神的核心,爱国是具体而不是抽象的。因此,从哲学角度看,弘扬和培育民族精神,应当 ①集中力量解决主要矛
- 下列不属于蛋白质功能的是( ) A.具有免疫功能 B.起信息传递作用调节
- 若函数f(x)=在x=x0处取得极值,则x0=.
- 下列哪种反射是人类特有的( ) A.眨眼反射
- 右图为水盐平衡调节机理,请据图判断A、B、C依次是( ) A.抗利尿激素、大脑皮层、肾小管和集合管 B.大脑皮层、抗利
- 生产力和生产关系、经济基础和上层建筑的矛盾之所以是社会基本矛盾,是因为它们 ①影响和制约其他社会矛盾
- 实验室用乙酸、乙醇、浓硫酸制取乙酸乙酯,加热蒸馏后,在饱和Na2CO3溶液上面得到无色油状液体,当振荡混合时,有气泡产生
- 在以下史诗中,描写爱琴海附近海域发生战争的是 A.《吉尔伽美什》
- 如图,由4个相同的小立方块组成一个立体图形,它的主视图是 A. B.
- 在我国,要经国家有关部门的批准才能调整税率。由此可以看出税收具有 的基本特征。 A.强制性 B.无偿性 C.固定性 D.
- When we get onthe bus, we should wait ________.
- 根据上面实验装置图,回答下列问题。 (1)请写出图中a、b的名称:a ;b 。
- 阅读下面的文字,完成后面题。
- 由九三学社、云南省委组织专家学者历时一年完成了《昆明市城市生活垃圾现状及治理对策 调研报告》,《报告》提出:要用市场经济
- 计算:;
- 为虚数单位,若,则的值为 ( ) A
- “九鼎既成,迁于三国。夏后氏失之,殷人受之;殷人失之,周人受之。”其中所说的“九鼎”之所以被广泛重视并在夏商周流转,主要



