第2节 电解质的电离 离子反应 知识点题库
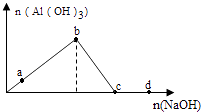
 =10-12的溶液中:Na+、K+、NO3-、ClO-
C . pH=12的无色溶液:K+、Na+、CH3COO-、Br-
D . 含Na2SO3的溶液中:K+、H+、Cl-、NO3-
=10-12的溶液中:Na+、K+、NO3-、ClO-
C . pH=12的无色溶液:K+、Na+、CH3COO-、Br-
D . 含Na2SO3的溶液中:K+、H+、Cl-、NO3-
-
(1) 下列物质中含原子数最多的是(填序号,下同)
①9g H2O ②3.01×1023个CH4分子 ③0.3mol NH3④11.2L CO2(标况)
-
(2) 下列物质中属于电解质的是
①盐酸 ② Fe ③ 熔融NaCl ④ 蔗糖 ⑤KNO3晶体 ⑥Na2SO4溶液
-
(3) 除去KNO3固体中少量的KCl,选择正确的操作并排序
①过滤 ②萃取 ③固体溶于水 ④冷却结晶 ⑤蒸发浓缩
⑥干燥 ⑦洗涤 ⑧分液
 B .
B .  C .
C . 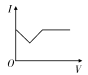 D .
D . 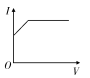
| 弱酸 | CH3COOH | H2CO3 | HClO |
| 电离常数 | K=1.75×10-5 | K1=4.4×10-7 K2=4.7×10-11 | K=3.0×10-8 |
下列叙述错误的是( )
 D . CH3COOH和ClO-可以大量共存
D . CH3COOH和ClO-可以大量共存
-
(1) 常温下,某水溶液M中存在的离子有Na+、A2-、HA-、H+、OH- , 存在的分子只有H2O,根据题意回答下列问题。
①写出酸H2A的电离方程式:
②若溶液M由10 mL 2 mol∙L-1 NaHA 溶液与10 mL2 mol∙L-1 NaOH溶液混合而得,则溶液M的pH(填“>”“<”或“=”)7,溶液M中各粒子的浓度关系正确的是(填序号)。
A.c(Na+)>c(A2-)>c(OH-)>c(H+)
B.c(HA-)+2c(H2A)+c(H+)=c(OH-)
C.c(A2-)+c(HA-)+c(OH-)=c(Na+)+c(H+)
D.c(A2-)+c(HA-)=1mol∙L-1
-
(2) 实验室可用NaOH溶液吸收NO2 , 反应为2NO2+2NaOH=NaNO3+NaNO2+H2O。含0.2 mol NaOH的水溶液与0.2 mol NO2恰好完全反应得1L溶液A,溶液B为0.1 mol∙L-1的CH3COONa溶液,则两溶液中c(
 )、c(
)、c(  )和c(CH3COO-)由大到小的顺序为(已知HNO2的电离常数Ka=7.1×10-4 , CH3COOH的电离常数Ka=1.7×10-5)。可使溶液A和溶液B的 pH相等的方法是(填序号)。
)和c(CH3COO-)由大到小的顺序为(已知HNO2的电离常数Ka=7.1×10-4 , CH3COOH的电离常数Ka=1.7×10-5)。可使溶液A和溶液B的 pH相等的方法是(填序号)。 a.向溶液A中加适量水 b.向溶液A中加适量 NaOH
c.向溶液B中加适量水 d.向溶液B中加适量NaOH
-
(3) 直接排放含SO2的烟气会形成酸雨,危害环境。利用钠碱循环法可脱除烟气中的SO2.吸收液(NaOH溶液)吸收SO2的过程中,pH随n(
 ):n(
):n(  )的变化关系如下表:
)的变化关系如下表: n(
 ):n(
):n(  )
)91:9
1:1
9:91
pH
8.2
7.2
6.2
①由上表判断 NaHSO3溶液显性。
②当吸收液呈中性时,溶液中离子浓度的大小关系为
 B . FeI2溶液与足量溴水反应:
B . FeI2溶液与足量溴水反应: 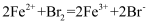 C . NaOH溶液与过量H2C2O4溶液反应:
C . NaOH溶液与过量H2C2O4溶液反应:  D . Na与水反应: 2Na + 2H2O = 2Na+ +2OH- + H2↑
D . Na与水反应: 2Na + 2H2O = 2Na+ +2OH- + H2↑
①过滤
②加过量NaOH溶液
③加适量盐酸
④加过量Na2CO3溶液
⑤加过量BaCl2溶液
正确的操作顺序是( )
 + 3H2O
C . 向NaH2PO2溶液中滴加浓硝酸反应的离子方程式为:
+ 3H2O
C . 向NaH2PO2溶液中滴加浓硝酸反应的离子方程式为:  + H+=H3PO2
D . 利用 (H3PO2)进行化学镀银反应中,1molH3PO2 最多还原 4 mol Ag+离子
+ H+=H3PO2
D . 利用 (H3PO2)进行化学镀银反应中,1molH3PO2 最多还原 4 mol Ag+离子
-
(1) K2FeO4的制备:

①i中反应的离子方程式是。
②将ii中反应的离子方程式补充完整:Fe3++OH-+ClO-=FeO42-++
③iii中反应说明溶解度:Na2FeO4K2FeO4(填“>”或“<”)。
-
(2) K2FeO4的性质:
i.将K2FeO4固体溶于蒸馏水中,有少量无色气泡产生,经检验为O2 , 液体有丁达尔效应。
ii.将K2FeO4固体溶于浓KOH溶液中,放置2小时无明显变化。
iii.将K2FeO4固体溶于硫酸中,产生无色气泡的速率明显比i快。
①K2FeO4溶于蒸馏水的化学反应方程式是。
②K2FeO4的氧化性与溶液pH的关系是。
-
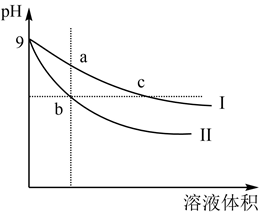
(3) K2FeO4的应用。K2FeO4可用于生活垃圾渗透液的脱氮(将含氮物质转化为N2)处理。K2FeO4对生活垃圾渗透液的脱氮效果随水体pH的变化结果如下:
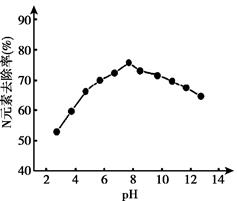
①K2FeO4脱氮的最佳pH是。
②根据图推测,pH=4时生活垃圾渗透液中含氮物质主要以形式存在。
③pH大于8时,脱氮效果随pH的升高而减弱,分析可能的原因:。
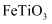 , 含杂质
, 含杂质 )为原料制取偏钛酸的流程如图。
)为原料制取偏钛酸的流程如图。
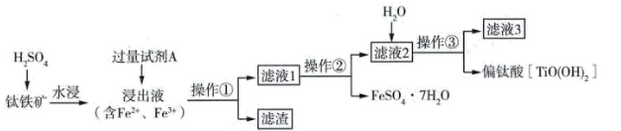
已知:向钛铁矿中加入硫酸得到硫酸氧钛(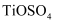 ),硫酸氧钛在加热的条件下水解得到偏钛酸,偏钛酸为难溶于水的白色沉淀。
),硫酸氧钛在加热的条件下水解得到偏钛酸,偏钛酸为难溶于水的白色沉淀。
下列叙述错误的是( )
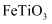 中,Ti的化合价为+4价
B . 过量试剂A为铁粉,仅起还原浸出液中
中,Ti的化合价为+4价
B . 过量试剂A为铁粉,仅起还原浸出液中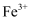 的作用
C . 操作②主要是蒸发浓缩、冷却结晶、过滤
D . 硫酸氧钛水解的离子方程式为:
的作用
C . 操作②主要是蒸发浓缩、冷却结晶、过滤
D . 硫酸氧钛水解的离子方程式为:
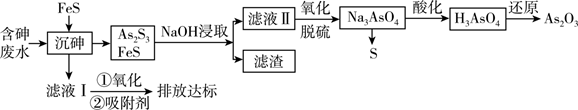
已知:Ⅰ. As2S3+ 6NaOH = Na3AsO3 + Na3AsS3+ 3H2O
Ⅱ. As2S3(s) + 3S2-(aq)  2
2  (aq)
(aq)
Ⅲ.砷酸(H3AsO4)在酸性条件下有强氧化性,能被SO2、氢碘酸等还原。
-
(1) As2S3中砷元素的化合价为价。
-
(2) “沉砷”过程中FeS是否可以用过量的Na2S替换(填“是”或“否”);请从平衡移动的角度解释原因:。
-
(3) 向滤液Ⅱ中通入氧气进行“氧化脱硫”,写出脱硫的离子反应方程式。
-
(4) 用SO2“还原”过程中,发生反应的化学方程式为。若需检验还原后溶液中是否仍存在砷酸。则还需要的实验试剂有。
-
(5) “还原”后加热溶液,H3AsO3分解为As2O3 , 同时结晶得到粗As2O3 , As2O3在不同温度和不同浓度硫酸中的溶解度(S)曲线如图所示。为了提高粗As2O3的沉淀率,“结晶”需要控制的具体条件是。
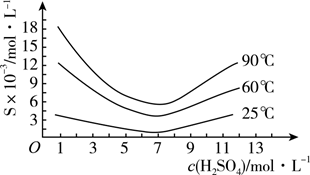
-
(6) 含砷废水也可采用另一种化学沉降法处理:向废水中先加入适量氧化剂,再加入生石灰调节pH,将砷元素转化为Ca3(AsO4)2沉淀。若沉降后上层清液中c(Ca2+)为2×10-3mol/L,则溶液中
 的浓度为mol/L。(已知Ksp[Ca3(AsO4)2]=8×10-19)
的浓度为mol/L。(已知Ksp[Ca3(AsO4)2]=8×10-19)
 C .
C . 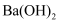 D . 氯化氢气体
D . 氯化氢气体
- 下列分子的比例模型中,中心原子上存在孤电子对的是 A. B. C. D.
- 研究列车在不同气候条件下车厢内的情况,工程设计人员获得相关数据,是列车达到安全舒适要求的先决条件。目前,设在奥地利维也纳
- 分子间有相互作用的势能,规定两分子相距无穷远时两分子间的势能为零.设分子a固定不动,分子b以某一初速度从无穷远处向a运动
- ______ in papers, he didn’t notice my coming. A. Having ab
- 下列各句中,标点符号使用正确的一项是(3分) A.走到一个十字路口,左拐;继续向前,走到第二个十字路口,还是左拐,跨过马
- 用质量相等的锌粉和铁粉,分别与溶质质量分数相同、等质量的稀盐酸充分反应.产生氢气的质量和反应所用时间的关系如图所示.则下
- 若抛物线的准线方程为,则抛物线的标准方程为( ) A. B. C.
- 浓硝酸和浓硫酸是实验室常用的试剂,下列关于浓硝酸和浓硫酸的叙述正确的是( ) A.分别向其中滴加紫色的石蕊试液,现
- 如下图所示装置中,a、b都是惰性电极,通电一段时间后,b电极附近溶液呈红色。下列说法正确的是() A.X是负极,Y是正极
- 阅读下面的文言文,完成小题。 (张)良尝闲从容步游下邳圯(音yí,桥)上。有一老父,衣褐,至良所,直堕其履圯下。顾谓良曰
- 下列选项中,为打开原子时代的大门奠定了理论基础的是 A.万有引力定律 B.微积分
- 下面是某同学向家人介绍的南极地区的情况,其中有误的一项是( )A.南极地区多狂风
- 2010年5月1日至10月31日在上海召开的世界博览会主题是“城市,让生活更美好”。阅读材料,结合所学知识回答下列问题。
- 氢气在氯气中燃烧时产生苍白色火焰。在反应过程中,破坏1molH2中的化学键消耗的能量为Q1kJ,破坏1molCl2中的化
- 小明翻阅家谱时看到“十一世长房:伯爵公,忠厚无华,勤力本业,家族有事,无不勉赴,不失为祖宗纯孙。”材料中的“伯爵公”最有
- 美国1787年宪法规定:国会有权宣战,招募陆军,建立和维持一支海军,有权征召民兵,以执行联邦法律、镇压叛乱和击退入侵;总
- 下图为四种不同的育种方法,请回答:(1)图中A、D途径表示杂交育种,一般从F2开始选种,这是因为 。 (2
- 2.下列各句中,没有语病的一句是( ) A.哈大高铁施行新的运行计划后,哈尔滨至北京、上海等地的部分列车也将进
- No one noticed him _____ in. A. to come B. came C. come D. h
- 下列推断正确的是 A.SiO2 是酸性氧化物,能与NaOH溶液反应 B.Na2O、Na2O2组成元素相同,与 CO2反应



