专题5 微观结构与物质的多样性 知识点题库
在元素周期表中,金属性最强的元素(不包括放射性元素)是(填元素符号,下同);最活泼的非金属元素是;最高价氧化物对应水化物的酸性最强的元素是;原子半径最小的元素是.
下列排列顺序正确的是( )
A . 热稳定性:H2O>HF>H2S
B . 原子半径:Na>Mg>O
C . 酸性:H3PO4>H2SO4>HClO4
D . 金属性:Na>Mg>Ca
下列说法正确的是( )
A . Na2O2、NaClO中所含化学键类型完全相同
B . 只有活泼金属与活泼非金属元素之间才能形成离子键
C . D2O和T2O是同一物质
D . 氯气与NaOH反应的过程中,同时又离子键、极性键和非极性键的断裂和形成
已知A,B,C,D,E五种元素为周期表前20号元素且原子序数依次增大,其中只有A,D为非金属元素。A的气态氢化物溶于水得到的溶液能使酚酞溶液变红。B,C,D的最高价氧化物对应水化物相互之间能够两两反应,且D原子最外层电子数是C原子最外层电子数的2倍。B、E元素同主族。
-
(1) E在元素周期表中的位置:,写出E的最高价氧化物对应水化物与C的单质反应的化学方程式:。
-
(2) A的气态氢化物溶于水后的电离方程式为。
-
(3) B单质在空气中燃烧后的产物的电子式为,产物中存在的化学键类型有。
短周期主族元素W、X、Y、Z的原子序数依次增大,W的简单氢化物可用作制冷剂,Y的原子半径是所有短周期主族元素中最大的。由X、Y和Z三种元素形成的一种盐溶于水后,加入稀盐酸,有黄色沉淀析出,同时有刺激性气体产生。下列说法正确的是( )
A . 原子半径:Y>Z>X>W
B . 简单氢化物的热稳定性:W>X>Z
C . Y、Z形成的化合物溶于水会促进水的电离
D . 上述刺激性气体通入紫色石蕊溶液,溶液先变红后褪色
短周期主族元素a、b、c、d原子序数依次增大,b、c、d与a均可以形成二元化合物X、Y、Z,且X能分别与Y、Z发生化合反应生成离子化合物,c的L层电子数等于K层电子数和M层电子数之和,下列判断正确的是( )
A . 简单阴离子半径:c<d
B . b元素可以形成一种常见的熔点很高的单质
C . 氢化物稳定性:c>d
D . 最高价氧化物对应水化物的酸性:b<d
短周期元素W、X、Y、Z的原子序数依次增大。W的单质与H2在暗处能化合并发生爆炸,X是同周期中金属性最强的元素,Y原子的最外层电子数等于电子层数,W和Z原子的最外层电子数相同。下列说法错误的是( )
A . 单质的沸点:Z>W
B . 简单离子半径:X>W
C . 元素X与氧可形成既含离子键又含非极性共价键的化合物
D . X、Y、Z的最高价氧化物对应的水化物两两之间能相互反应
下列表示错误的是( )
A . 水的比例模型: 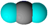 B . 苯酚的结构简式:C6H5OH
C . 乙酸乙酯的键线式:
B . 苯酚的结构简式:C6H5OH
C . 乙酸乙酯的键线式: 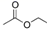 D . 羟基的电子式:
D . 羟基的电子式: 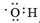
W、X、Y、Z 四种短周期元素在元素周期表中的相对位置如图所示,Z 的原子序数是 X 的 2倍。下列说法错误的是( )
![]()
A . X 元素形成的氢化物沸点比 W 的高
B . 四种元素原子半径从大小的排列顺序 Y>Z>X>W
C . X 的一种氢化物和 X、Z 形成的一种化合物具有相同原理的漂白作用
D . Y 的氧化物能与 W 的氢化物反应
现有甲、乙、丙、丁四种短周期元素,它们之间的关系如下:
Ⅰ.原子半径:甲<丙<乙<丁
Ⅱ.原子的最外层电子数:甲+丙=乙+丁=8
Ⅲ.原子的核外电子层数:丁>乙=丙=2甲
Ⅳ.乙元素的主要化合价:最高正价+最低负价=2
则下列说法错误的是( )
A . 乙元素的最外层有5个电子,其氢化物含有极性键
B . 四种元素中丙的非金属性最强,其最高价氧化物对应的含氧酸酸性最强
C . 丁元素的氧化物对应的水化物与乙元素最高价氧化物对应水化物恰好完全反应形成的盐溶液显酸性
D . 乙、丙两元素形成的简单氢化物稳定性丙的强于乙
下表是元素周期表的一部分,回答下列有关问题(用化学符号回答):
|
族 周期 |
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
0 |
|
2 |
① |
② |
③ |
|||||
|
3 |
④ |
⑤ |
⑥ |
⑦ |
⑧ |
⑨ |
||
|
4 |
⑩ |
-
(1) 在①~⑩元素中,最活泼的金属元素是,最活泼的非金属元素是,最不活泼的元素是。
-
(2) 在①~⑩元素的最高价氧化物对应的水化物中,酸性最强的是,碱性最强的是,呈两性的是。写出在水溶液中三者之间相互反应的离子方程式:,,
。
下列变化过程需破坏离子键的是( )
A . 干冰升华
B . 电解水
C . 食盐熔化
D . 氯化氢溶于水
X、Y、Z、W四种短周期元素位于三个不同的周期,且原子序数依次增大。它们能形成结构如图所示的分子,下列推断错误的是( )
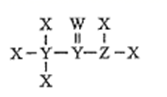
A . X、Z原子之间形成的是极性共价键
B . 气态氢化物的沸点:W>Z
C . 右图分子中Y满足最外层8电子稳定结构
D . 最高价含氧酸的酸性:W>Y
五种短周期主族元素a、b、c、d、e在周期表中的相对位置如表所示,下列说法错误的是( )
| a | b | c |
| d | e |
A . 五种元素可能都是非金属元素
B . 五种元素原子的最外层电子数之和可能为30
C . 若a的一种单质是自然界最硬的物质,则五种元素中最高价氧化物的水化物为强酸的只有e
D . 若五种元素中只有一种是金属元素,则c的最高价氧化物的水化物能与其简单氢化物反应
据文献报道,金红石  表面催化氮气固定机理如图所示,下列叙述错误的是( )
表面催化氮气固定机理如图所示,下列叙述错误的是( )
 表面催化氮气固定机理如图所示,下列叙述错误的是( )
表面催化氮气固定机理如图所示,下列叙述错误的是( ) 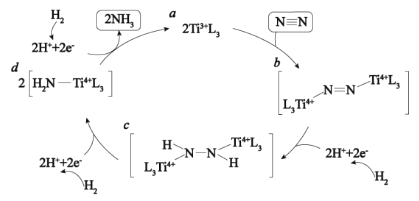
A . 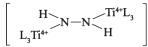 是反应中间体
B . 该催化固氮总反应为
是反应中间体
B . 该催化固氮总反应为  C . 整个催化过程中存在
C . 整个催化过程中存在 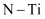 键的断裂和生成
D . 催化剂可以提高固氮速率的原因是改变该反应的△H
键的断裂和生成
D . 催化剂可以提高固氮速率的原因是改变该反应的△H
 C . 整个催化过程中存在
C . 整个催化过程中存在 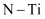 键的断裂和生成
D . 催化剂可以提高固氮速率的原因是改变该反应的△H
键的断裂和生成
D . 催化剂可以提高固氮速率的原因是改变该反应的△H
下列叙述错误的是( )
①热稳定性: 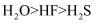
②最外层两个电子的元素不一定在第ⅡA族
③  晶体溶于水时,离子键被破坏,共价键不受影响
晶体溶于水时,离子键被破坏,共价键不受影响
④元素周期表中从ⅢB族到ⅡB族10个纵行的元素都是金属元素
⑤金刚石和石墨互为同素异形体,熔点和硬度都很高
⑥氯的各种含氧酸的酸性由弱到强排列为 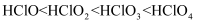
⑦两个非金属元素原子间只可能形成共价键,而含金属元素的化合物中一定含离子键
A . ②④⑥⑦
B . ①⑤⑥⑦
C . ②③④⑤
D . ①③⑤⑦
我国嫦娥五号探测器带回1.731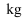 的月球土壤,经分析发现其构成与地球土壤类似。土壤中含有的短周期元素W、X、Y、Z,原子序数依次增大,W元素基态原子2p能级仅有一对成对电子。基态X原子的价电子排布式为
的月球土壤,经分析发现其构成与地球土壤类似。土壤中含有的短周期元素W、X、Y、Z,原子序数依次增大,W元素基态原子2p能级仅有一对成对电子。基态X原子的价电子排布式为 。基态Z元素原子最外电子层上s、p电子数相等,下列结论正确的是( )
。基态Z元素原子最外电子层上s、p电子数相等,下列结论正确的是( )
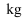 的月球土壤,经分析发现其构成与地球土壤类似。土壤中含有的短周期元素W、X、Y、Z,原子序数依次增大,W元素基态原子2p能级仅有一对成对电子。基态X原子的价电子排布式为
的月球土壤,经分析发现其构成与地球土壤类似。土壤中含有的短周期元素W、X、Y、Z,原子序数依次增大,W元素基态原子2p能级仅有一对成对电子。基态X原子的价电子排布式为 。基态Z元素原子最外电子层上s、p电子数相等,下列结论正确的是( )
。基态Z元素原子最外电子层上s、p电子数相等,下列结论正确的是( )
A . 原子半径大小顺序为X
下列物质含有离子键的是( )
A . N2
B . NH3
C . NH4Cl
D . NO
2020年12月17日凌晨1时59分,“嫦娥五号”首次实现了我国地外天体采样返回目标,标志着我国航天事业迈出了一大步。带回的月壤中包含了H、O、N、Al、S、Cd、Zn、Ti、Cu、Au、Cr等多种元素。回答下列问题:
-
(1) 一些氧化物的熔点如表所示:
氧化物
Li2O
MgO
P4O6
SO2
熔点/℃
1570
2800
23.8
-75.5
解释表中氧化物之间熔点差异的原因:。
-
(2) Cr2O
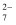 的结构如图所示。则该离子中σ键与π键的个数比为。
的结构如图所示。则该离子中σ键与π键的个数比为。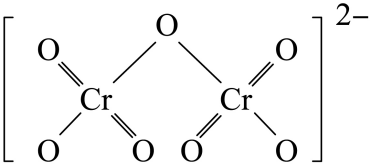
-
(3) [Cr(NH3)3(H2O)2Cl]2+中配体分子NH3、H2O的空间结构和相应的键角如图所示。
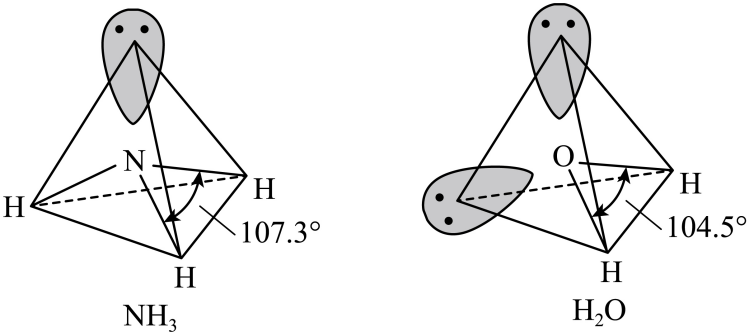
H2O的键角小于NH3的键角,原因是。
-
(4) 钛某配合物可用于催化环烯烃聚合,其结构如图所示。
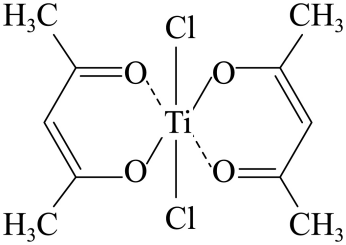
该配合物中存在的化学键有____(填字母代号)。
A . 离子键 B . 配位键 C . 金属键 D . 共价键 E . 氢键 -
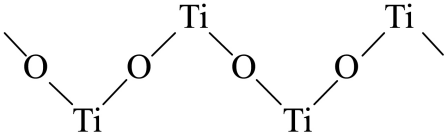
(5) 已知TiO2与浓硫酸反应生成硫酸氧钛,硫酸氧钛晶体中阳离子为链状聚合形式的离子,结构如图所示,该阳离子的化学式为,阴离子的空间构型为。
-
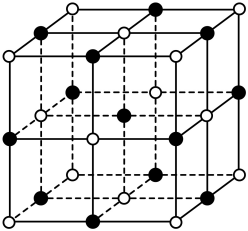
(6) 已知TiN晶体的晶胞结构如图所示,若该晶胞中Ti原子与N原子的最近距离为apm,阿伏加德罗常数的值为NA , 则晶胞的密度为g·cm-3。[M(TiN)=62g·mol-1 , 用含a、NA的代数式表示]。
冠醚是皇冠状的分子,可有不同大小的空穴适配不同大小的碱金属离子。18—冠—6可与钾离子作用,如图是18—冠—6与钾离子以配位键结合形成的超分子结构示意图。下列说法错误的是( )
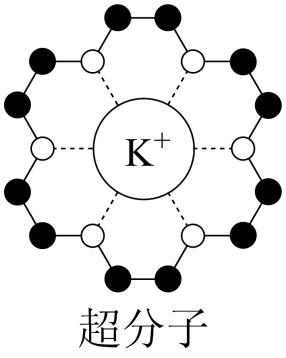
A . 超分子具有分子识别和自组装的特征
B . 该超分子中K+的配位数为6
C . 利用超分子的分子识别特征,还可以分离C60、C70
D . 冠醚与碱金属离子形成的配合物属于“超分子”,其形成的晶体是分子晶体
最近更新
- 下列有关遗传信息的叙述,错误的是: ( ) A.遗传信息可以通过DNA复制传递给后代
- 已知正方形的边长为,为的中点,则_______.
- 实验室制取氧气的装置如右图所示,下列有关叙述合理的是( )A.锥形瓶里加入少量MnO2粉末,分液漏斗里盛放6%双氧
- 已知家鸡的无尾(A)对有尾(a)是显性。现用有尾鸡(甲群体)自交产生的受精卵来孵小鸡,在孵化早期向卵内注射微量胰岛素,孵
- 如图1,在正方形中,是对角线上的一点,点在AD的延长线上,且,交于 (1)证明:. (2)求的度数. (3)如图2,把正
- 工业上制备纯硅反应的热化学方程式如下: SiCl4(g)+2H2(g)=Si(s)+4HCl(g) △H=+QkJ/mo
- 《孟子》是 ① 家经典之一,它是孟子及其门人所作。孟子是战国时期伟大的思想家。他认为在“生”与“义”不能兼顾
- 在体积均为1L,pH均等于2的盐酸和醋酸中,分别投入0.28g Fe,则下图中的曲线符合反应事实的是( )
- 在山东刘公岛有一座甲午战争纪念馆,如果你是一名解说员,你将向参观的人们介绍哪些内容?( ) ①林则徐率军抵
- 某同学的实验报告中,有以下实验数据,其中合理的是 A.用托盘天平称得11.7g食盐 B.排空气法收集氧气的纯度可以达到1
- 短周期元素的离子aA2+、 bB+、cC2-、dD- 都具有相同电子层结构,则下列叙述正确的是
- 用一机械将一批货箱吊上离地12m高的平台,每个货箱的质量为5Kg,这个机械在吊箱子时所能提供的功率,取决于所吊物体质量的
- 小明学习物理后,对抽烟的爸爸说:“吸烟有害健康.我和妈妈都在被动吸烟”.小明这样说的科学依据是 A、分子很小 B、分子在
- One morning, Istepped out of bed and put my feet on the floo
- 某燃料电池所用燃料为H2和空气,电解质为熔融的K2CO3.该电池的总反应为2H2+O2==2H2O,负极反应为H2+CO
- —Iwonder ____________ in Guangzhou in two hours. —Of course.
- — Excuse me.Is this the right way to the Summer Palace? — So
- 下列现象中,属于生物因素影响的是() A.小麦、玉米等植物只有在强光下才能生长得好 B.作物在水、肥充足的土壤中生长良好
- 宋、元、明、清时期,赋税征收货币,是当时国家财政的一个大势。1581年,明朝实行一条鞭法,改革赋役制度,下列有关这一制度
- 阅读下面一段文字,完成下列问题好一派生机àng( )然的蓬莱仙境啊!这里有身材秀qí( )的毛白杨,伸着绿如f



