专题5 微观结构与物质的多样性 知识点题库
下列是说法正确的是( )
A . 在水蒸气分子中因存在氢键,所以水的沸点很高
B . 用电子式表示H2O的形成过程: 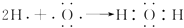 C . 碱金属的熔点、沸点随原子序数的递增而升高,卤素单质的熔点、沸点随原子序数的递增而降低
D . 卤素单质的氧化性随原子序数的逐渐增大而增强,其卤化氢的沸点依次升高
C . 碱金属的熔点、沸点随原子序数的递增而升高,卤素单质的熔点、沸点随原子序数的递增而降低
D . 卤素单质的氧化性随原子序数的逐渐增大而增强,其卤化氢的沸点依次升高
下列化学用语表示正确的是( )
A . 钾离子结构示意图: 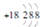 B . N2H4的电子式:
B . N2H4的电子式: 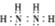 C . 聚丙烯的结构简式:
C . 聚丙烯的结构简式: 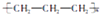 D . 中子数为79、质子数为55的铯(Cs)原子:
D . 中子数为79、质子数为55的铯(Cs)原子: 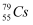
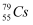
下列物质的电子式正确的是( )
A . 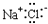 B .
B . 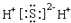 C .
C . 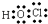 D .
D . 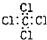
下列表达方式正确的是( )
A . Na+的电子排布图: 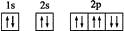 B . 硫离子的核外电子排布式:1s22s22p63s23p4
C . 碘化铵的电子式:[H
B . 硫离子的核外电子排布式:1s22s22p63s23p4
C . 碘化铵的电子式:[H 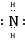 H]+I-
D . H2O电子式:H∶
H]+I-
D . H2O电子式:H∶ 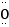 ∶H
∶H
Ⅰ、单质硅由于其成熟的生产工艺, 丰富的生产原料及优异的性能被广泛用于电子行业及太阳能电池的生产等,在二氧化碳氛围中通过利用金属钠来还原二氧化硅可在较低的温度条件下得到硅,同时生成一种盐X,这相比起现有的生产工艺具有节约能耗的优势。
-
(1) 写出上述制备硅的化学反应方程式。
-
(2) 二氧化硅与二氧化碳物理性质差别很大,原因是。
-
(3) 盐X的溶液能与Al2(SO4)3溶液反应生成一种白色沉淀和气体。写出此反应的离子反应方程式。
-
(4) Ⅱ、某盐A有3种元素组成,易溶于水。将A加热,生成既不助燃,也不使湿润的红色或蓝色石蕊试纸变色的气体B和H2O。将A溶于水,进行下列实验:①酸性条件下与H2S作用生成淡黄色沉淀C,同时放出无色气体D,D在空气中转变为红棕色气体E;②当通入足量Cl2时,无明显现象,但将所得溶液浓缩后即可得到无色晶体盐F。请回答下列问题:
写出A的化学式:; B的电子式:。
-
(5) 写出上述实验①、②所发生的离子反应方程式:①;②。
-
(6) D、E对环境有危害,可用NaOH溶液来吸收等物质的量的D、E混合气体,写出其化学反应方程式。
-
(7) 判断盐F的可能成分;设计实验方案确定F的成分。
短周期元素x、y、z、m、n在元素周期表中的位置如图所示,则下列说法中错误的是( )
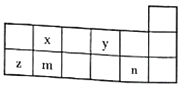
A . 最高价氧化物的水化物的酸性由弱到强的顺序是m、x、n
B . y、n分别与金属钠形成的化合物中均只含有离子键
C . y、z、n分别形成的简单离子半径的大小为n>y>z
D . x、z、m、n的最高价氧化物对应水化物均能与强碱反应
下列说法错误的是( )
A . N2的电子式是  B . 金刚石和石墨是同位素
C . 1mol14NH4+含有中子7mol
D . 周期表中第13纵行是ⅢA元素
B . 金刚石和石墨是同位素
C . 1mol14NH4+含有中子7mol
D . 周期表中第13纵行是ⅢA元素
下列叙述错误的是( )
A . 用电子式表示HCl的形成过程: 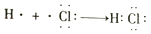 B .
B . 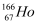 中的原子核内的中子数与核外电子数之差是99
C . 在空气中加热金属锂:4Li+O2
中的原子核内的中子数与核外电子数之差是99
C . 在空气中加热金属锂:4Li+O2  2Li2O
D . (CH3)2CHC2H5和CH3CH2CH(CH3)2属于同种物质
2Li2O
D . (CH3)2CHC2H5和CH3CH2CH(CH3)2属于同种物质
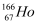 中的原子核内的中子数与核外电子数之差是99
C . 在空气中加热金属锂:4Li+O2
中的原子核内的中子数与核外电子数之差是99
C . 在空气中加热金属锂:4Li+O2  2Li2O
D . (CH3)2CHC2H5和CH3CH2CH(CH3)2属于同种物质
2Li2O
D . (CH3)2CHC2H5和CH3CH2CH(CH3)2属于同种物质
下列物质为含有共价键的离子化合物的是( )
A . Na2O
B . CaCl2
C . NH3·H2O
D . NaOH
短周期元素A,B,C在周期表中所处的位置如图所示。A,B,C三种元素原子的质子数和为32。D元素原子的最外层电子数是其次外层电子数的2倍。则下列说法正确的是( )
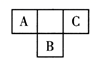
A . 四种元素形成的气态氢化物中,C元素的氢化物的稳定性最强
B . 元素D的某种同位素质量数为14,则其中子数为6
C . B,C两种元素可形成BC6型化合物,该化合物属于离子化合物
D . A,B两种元素的气态氢化物均能与它们对应的最高价氧化物对应的水化物发生反应,且都属于氧化还原反应
A、B、C、D、E均为短周期元素,原子序数依次增大,请根据表中信息回答下列问题:
|
元素 |
元素性质或结构 |
|
A |
最外层电子数是其内层电子数的2倍 |
|
B |
B元素的单质在空气中含量最多 |
|
C |
C元素在地壳中含量最多 |
|
D |
D元素在同周期中金属性最强 |
|
E |
常温常压下,E元素形成的单质是淡黄色固体,常在火山口附近沉积 |
-
(1) E在元素周期表中的位置.
-
(2) D的最高价氧化物的水化物电子式,所含化学键类型.
-
(3) B、C、D、E简单离子半径由大到小顺序为(用离子符号表示).
-
(4) 由A、B、C与氢元素组成的一种常见酸式盐与过量D的最高价氧化物的水化物反应的离子方程式:.
下列化学用语正确的是( )
A . 乙酸根离子的结构式: 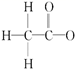 B . CO2的球棍模型:
B . CO2的球棍模型: 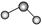 C . 3-甲基-1-丁烯的结构简式:(CH3)2CHCH=CH2
D . 醛基的电子式:
C . 3-甲基-1-丁烯的结构简式:(CH3)2CHCH=CH2
D . 醛基的电子式: 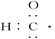
 B . CO2的球棍模型:
B . CO2的球棍模型:
第三周期元素X、Y、Z、W的最高价氧化物溶于水可得四种溶液,0.01mol/L的这四种溶液pH与该元素原子半径的关系如下图所示。下列说法正确的是( )
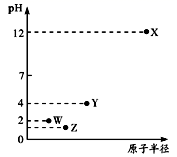
A . 简单离子半径: X>Y>Z>W
B . W的单质在常温下是黄绿色气体
C . 气态氢化物的稳定性: Z>W>Y
D . X和Y的最高价氧化物对应的水化物恰好中和时,溶液中的微粒共有2种
下列化学用语表述正确的是( )
A . 次氯酸的结构式 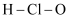 B . CH4的球棍模型
B . CH4的球棍模型  C . 乙烯的结构简式 CH2CH2
D . S2-的结构示意图
C . 乙烯的结构简式 CH2CH2
D . S2-的结构示意图 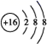
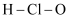 B . CH4的球棍模型
B . CH4的球棍模型
下列物质属于离子化合物的是( )
A . HCl
B . CO2
C . K2O
D . N2
图是某元素M的价类二维图,其中X是一种强碱,A为正盐,通常条件下Z是无色液体,D的相对分子质量比E小16,图中呈现了各物质的转化关系。下列说法正确的是( )
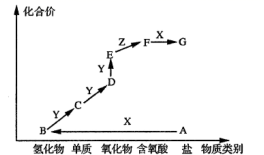
A . A中只含有离子键
B . B物质可以和Y反应直接转化为E
C . D,E均可以用向上排空气法收集
D . 通过氢氧化钠溶液可以除去D中含有的少量E
下列化学用语表示正确的是( )
A . CO2的结构式:O=C=O
B . H2O2的电子式: 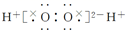 C . 纯碱的化学式:NaHCO3
D . 氯原子的结构示意图:
C . 纯碱的化学式:NaHCO3
D . 氯原子的结构示意图: 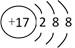
现有属于前四周期的A、B、C、D、E、F、G七种元素,原子序数依次增大。A元素的基态原子价电子排布为nsnnpn+1;C元素为最活泼的非金属元素;D元素原子核外有三个电子层,最外层电子数是核外电子总数的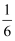 ;E元素正三价离子的3d轨道为半充满状态;F元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子;G元素与A元素位于同一主族,其某种氧化物有剧毒。
;E元素正三价离子的3d轨道为半充满状态;F元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子;G元素与A元素位于同一主族,其某种氧化物有剧毒。
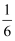 ;E元素正三价离子的3d轨道为半充满状态;F元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子;G元素与A元素位于同一主族,其某种氧化物有剧毒。
;E元素正三价离子的3d轨道为半充满状态;F元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子;G元素与A元素位于同一主族,其某种氧化物有剧毒。
-
(1) G的元素名称为 。
-
(2) A、B、C三种元素电负性由大到小的顺序为(用元素符号表示),第一电离能:DAl(填”>”“<”或“=”),其原因是
-
(3) E3+的离子符号为。
-
(4) F元素基态原子的电子排布式为 。
-
(5) G元素可能的性质为____。(填序号)。A . 其单质可用于生产半导体材料 B . 其电负性大于磷 C . 其最高价氧化物对应的水化物是强酸 D . 其第一电离能较小
下列关于晶体的说法中,错误的是( )
①晶体中微粒呈周期性有序排列,有自范性;而非晶体中微粒排列相对无序,无自范性
②晶胞是晶体中最小的“平行六面体'
③呈粉末状的固体物质没有规则的晶体外形,均不属于晶体
④晶体内部的微粒按一定规律做周期性排列
⑤晶胞是晶体结构的基本重复单元
⑥晶体尽可能采取紧密堆积的方式,以使其更稳定
A . ①②③
B . ②③④
C . ④⑤⑥
D . ②③
解痉药物奥昔布宁的结构简式如图所示。下列关于奥昔布宁的说法正确的是( )
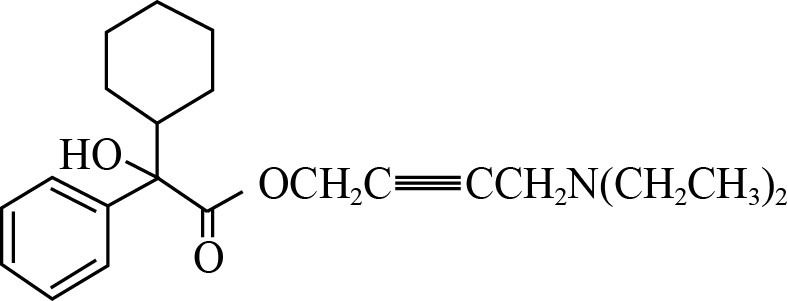
A . 组成元素均位于元素周期表的p区
B . 基态原子第一电离能:N>O>H>C
C . 分子中碳原子杂化轨道类型有2种
D . 分子中两个六元环的成环原子均各自共面
最近更新
- 下表是KNO3 、NaCl在不同温度下的溶解度(单位:g/100g水)温度(℃) 0 10 20 30 40 50 60
- 已知长方形ABCD,AB=4,BC=3,则以A、B为焦点,且过C、D两点的椭圆的离心率为______.
- 下列实验现象描述错误的是() A.硫在氧气中燃烧:发出蓝紫色火焰,产生有刺激性气味的气体,放热 B.研磨熟石灰与铵盐的混
- 在密闭容器中于一定条件下进行下列反应:2SO2+ O22SO3当到达平衡时通入18O2,再次平衡时,18O存在于(
- 阅读理解。 One day, I had a bad toothache. I couldn’t eat anyt
- 如图,在菱形ABCD中,AB=2,∠DAB=60°,点E是AD边的中 点,点M是AB边上的一个动点(不与点A重合),延长
- Cultural rulesdetermine every aspect of food consumption. Wh
- (一)阅读《人民解放军百万大军横渡长江》(节选),完成5—7题。(14分)和中路军所遇敌情一样,我西路军当面之敌亦纷纷溃
- 下列化学反应中既不属于化合反应也不属于分解反应的是() A.镁+氧气氧化镁 B.锌+硫酸硫酸锌+氢气 C.碳酸氢铵氨气+
- All of us burst into laughterwe saw Mr. Bean’s funny appeara
- 随着“神州7号”载人飞船发射成功,我国已实现三次载人航天飞行,在火箭推动飞船上升的阶段,航天员是被固定在飞船座舱内的,相
- 下列句子中,没有语病的一项是( )(3分)A.不但作为首位由学者出任的“内政部长”,江宜桦有效且快速地在政策上落实
- 在数3.8,-10, ,,0,1.2131415……,中无理数的个数是( ) A.1
- 下列物质一定属于纯净物的是A.净化后的空气 B.部分结冰的蒸馏水 C.加工门窗的铝合金
- 布拉风是一种从山地或高原经过低矮隘道向下倾落的寒冷暴风。这种风是因为在不太高的寒冷高原上的严寒空气,受暖海面上暖低压的吸
- What would happen if he ______ back home? A. go
- 常温下,下列各组离子在指定溶液中一定能大量共存的是 A、0.1 mol•L﹣1的KI溶液:Na+、Ag+、NO3﹣、SO
- 蚕吐丝的阶段为 A.卵 B.幼虫 C.蛹 D.成虫
- 雨后的晚上,人在月光下行走,为了不踩到水坑里,人们根据镜面反射和漫反射规律总结出,当迎着月光走时,地面发________
- 二战后,世界殖民体系逐渐瓦解,但以前的殖民国家并未衰落,其原因不包括 A.旧的国际秩序仍然存在 B



