第三单元 海洋化学资源的综合应用 知识点题库
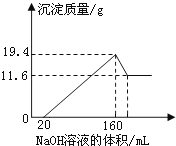
将一定质量的镁铝合金样品全部溶于100mL某浓度的盐酸中.向所得溶液中滴加5.0mol/L的NaOH溶液,生成沉淀质量与加入的NaOH溶液体积关系如图所示.
(1)19.4g沉淀中含有Al(OH)3的质量为 ;
(2)盐酸的物质的量浓度为 .
完成下列填空:
-
(1) 步骤一:灼烧干海带,使其灰化后用热水浸泡、过滤,制得原料液,含有氯化钾等物质.实验室灼烧海带应放在(填写仪器名称)中加热,选用热水而不是冷水浸泡海带灰的目的是.
-
(2) 步骤二:原料液经结晶过滤分离出氯化钾后,向滤液中通适量氯气氧化I﹣ , 制得富碘溶液.实验室模拟氧化过程的实验装置如图所示.
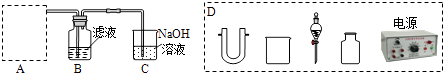
装置中A部分用于制取氯气,实验室制取氯气通常有两种方案:一是在强酸性条件下用氧化剂氧化Cl﹣;二是电解法.限用图D中的仪器(支撑仪器、导管、导线、石墨棒和橡皮塞除外),能实现的反应是(选填编号).
a.2NaCl(s)+MnO2+2H2SO4(浓)
 MnSO4+Cl2↑+Na2SO4+2H2O
MnSO4+Cl2↑+Na2SO4+2H2Ob.2KMnO4+16HCl(浓)→2MnCl2+2KCl+5Cl2↑+8H2O
c.2NaCl+2H2O
 2NaOH+Cl2↑+H2↑
2NaOH+Cl2↑+H2↑d.4HCl(浓)+MnO2
 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O广口瓶B中发生反应的离子方程式是.装置C中NaOH的作用是.
-
(3) 步骤三:取100mL B中富碘溶液,按如下流程分离碘单质.
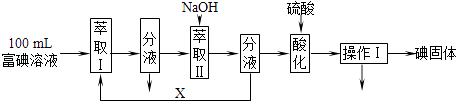
萃取Ⅱ和酸化过程发生的反应分别是:
3I2+6OH﹣→5I﹣+IO3﹣+3H2O;
5I﹣+IO3﹣+6H+→3I2+3H2O;
萃取剂X应选择(选填编号).
a.100mL苯b.10mL乙醇c.10mLCCl4d.10mL己烯
实验室进行萃取操作的仪器是.操作Ⅰ的名称是.
-
(4) 分离出的KCl样品中常含有少量NaCl和K2CO3等物质,设计实验用沉淀法测定氯化钾样品中K2CO3的质量分数:
①要用到的化学试剂是(填写化学式);
②要测定的物理量是.
 ,而又不引入新的杂质离子,应依次加入( )
,而又不引入新的杂质离子,应依次加入( )
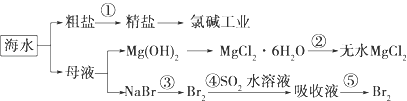
下列有关说法正确的是( )
 可将粗盐溶于水,然后进行下列五项操作:①过滤;②加过量氢氧化钠;③加适量盐酸;④加足量碳酸钠溶液;⑤加过量氯化钡溶液.下列操作顺序正确的是( )
可将粗盐溶于水,然后进行下列五项操作:①过滤;②加过量氢氧化钠;③加适量盐酸;④加足量碳酸钠溶液;⑤加过量氯化钡溶液.下列操作顺序正确的是( )
①优氯净中氯元素的化合价为.
②亚硫酸钠将水中多余次氯酸除去的化学反应方程式为.
-
(1) 精制食盐是制备小苏打的原料之一。粗盐中含有少量Ca2+、Mg2+、SO42- , 粗盐精制的步骤顺序是:溶解→→→→ (填字母编号)。
a.加盐酸调pH
b.加Ba(OH)2溶液
c.加Na2CO3溶液
d.过滤
-
(2) NH3、CO2先后通入饱和食盐水中,反应的离子方程式。
-
(3) 侯氏制碱法中,母液的处理方法是通入氨气,再加入细小食盐颗粒,最后冷却析出的副产品是;简述通氨气的作用。
-
(4) 称取2.640 g小苏打样品(含少量NaCl),配置成250 mL溶液,准确取出20.00 mL溶液于锥形瓶中,滴加作指示剂,滴定时消耗0.1000 mol/L盐酸的体积为20.67 mL。则该样品中碳酸氢钠的质量分数为(保留两位小数)。若装标准溶液的滴定管没有润洗,则测得的结果会(填“偏大”、“偏小”或“不变”)。
-
(5) 测定上述样品中碳酸氢钠的质量分数还可通过如图装置进行测定。实验需使用的定量仪器是;写出涉及的化学方程式。
|
序号 |
操作及现象 |
|
实验1 |
取放置一段时间后依然无色的0.1mol/LKI溶液,加入淀粉溶液,溶液不变蓝;向溶液中继续加入2滴6mol/L的稀硫酸,溶液立即变蓝 |
|
实验2 |
取新制的0.1mol/LKI溶液,加入淀粉溶液,溶液不变蓝;向溶液中继续加入2滴6mol/L的稀硫酸,溶液10s后微弱变蓝 |
-
(1) 溶液变蓝,说明溶液中含有 。结合实验1和实验2,该小组同学认为酸化能够加快I-氧化反应的速率。
-
(2) 同学甲对滴加稀硫酸后溶液变蓝速率不同的原因提出猜想:放置一段时间后的0.1mol/LKI溶液成分与新制0.1mol/LKI溶液可能存在差异,并继续进行探究。
实验3:取新制0.1mol/LKI溶液在空气中放置,测得pH如下:
时间
5分钟
1天
3天
10天
pH
7.2
7.4
7.8
8.7
资料:
ⅰ.pH<11.7时,I-能被O2氧化为I。
ⅱ.一定碱性条件下,I2容易发生歧化,产物中氧化产物与还原产物的物质的量之比为1∶5。
①用化学用语,解释0.1mol/LKI溶液放置初期pH升高的原因:。
②对比实验1和实验2,结合化学用语和必要的文字,分析实验1中加稀硫酸后“溶液立即变蓝”的主要原因可能是。
-
(3) 同学甲进一步设计实验验证分析的合理性。
序号
操作
现象
实验4
重复实验2操作后,继续向溶液中加入 。
溶液立即变蓝
-
(4) 该组同学想进一步探究pH对I2发生歧化反应的影响,进行了如下实验。
实验5:用20mL 4种不同浓度的KOH溶液与2mL淀粉溶液进行混合,测量混合液的pH后,向其中加入2滴饱和碘水,观察现象。记录如下:
实验组
A
B
C
D
pH
11.4
10.6
9.5
8.4
现象
无颜色变化
产生蓝色后瞬间消失
产生蓝色,30s后蓝色消失
从实验5可以看出pH越大,歧化反应速率越(填“快”或“慢”)。
解释pH=8.4时,“产生蓝色,30s后蓝色消失”的原因:。
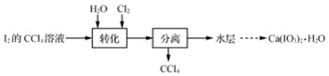
已知:碘酸是易溶于水的强酸,不溶于有机溶剂。
-
(1) 转化步骤是为了制得碘酸,该过程在图1所示的装置中进行。
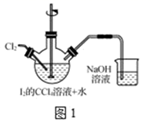
①当观察到现象时,停止通入氯气
②转化时发生反应的离子方程式为
-
(2) 除去HIO3水溶液中少量I2单质的实验操作为直至用淀粉溶液检验不出碘单质的存在。
已知:①Ca(IO3)2·6H2O是一种难溶于水的白色固体,在碱性条件下不稳定。
②Ca(IO3)2·6H2O加热升温过程中固体的质量变化如图2所示
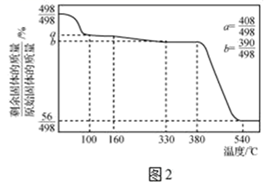
-
(3) Ca(IO)3·6H20在100~160℃条件下加热得到的物质成分是
-
(4) 下列说法正确的是_____________A . 转化过程中CCl4的作用只是增大I2的溶解量,提高I2的利用率 B . 为增大转化过程的反应速率,可适当加快通Cl2的速度 C . 以除碘后的水层为原料,加入过量的Ca(OH)2溶液,过滤,洗涤可得到Ca(IO3)2·6H2O D . 对已除碘后的水层为原料得到的沉淀Ca(IO3)2·6H2O进行洗涤,洗涤沉淀至洗涤后滤液滴加AgNO3溶液不再有沉淀产生
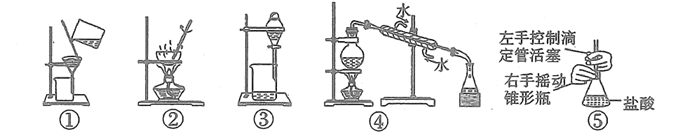
 提取碘水中的碘,可选择图③所示装置
C . 实验室制取蒸馏水常用图④所示装置
D . 用标准
提取碘水中的碘,可选择图③所示装置
C . 实验室制取蒸馏水常用图④所示装置
D . 用标准  溶液滴定未知浓度的盐酸,可选用图⑤所示装置
溶液滴定未知浓度的盐酸,可选用图⑤所示装置
- 氨气(NH3)是一种重要的化工原料。 ① NH3由(4)种元素组成,1 mol NH3中约含有(5)个氢原子,其中氮元素
- 现有100mL混和溶液,其中H2SO4、HNO3和KNO3的物质的量浓度分别是6mol/L、2mol/L和1mol/L,
- (08年嘉兴一中三模理) 已知均为非零向量,命题,命题的夹角为锐角,则是成立的( ) A.必要不充分条件 B.充
- 西方人文精神开始于对神主宰世界的否定,早期的人文精神萌芽于 A.古希腊文明 B.古罗马文明
- 下图所示为24小时的全日制时钟,指针为时针,读图并结合北半球夏至日各纬度昼长,回答以下三个小题。 纬度 昼长
- 受多种因素的制约,珠江三角洲地区的工业化和城市化的后劲日显不足,而且出现了一系列问题。据此完成 题 4.珠江三角洲地区工
- 作者把“家”比作了 、 和 。
- 小李同学利用假期到某工厂打工,获得了1500元工资。从经济活动的角度看,小李的行为属于 A.交换活动与分配活动 B
- 厨房里发生的下列变化中,属于物理变化的是 A.苹果腐烂
- 如图所示的电路,不可能出现的情况是()A.灯亮,铃响 B.灯亮、铃不响C.灯不亮、铃响 D.灯不亮、铃不响
- (6分)今年3月27日,你参加了以倡导低碳生活为主题的“地球一小时”活动吗?低碳,意指较低(更低)的温室气体(二氧化碳为
- (2011年湖北武汉,3题)氨水是一种化学肥料。打开贮存氨水的容器,就可以闻到一股强烈的氨味。从微观角度分析,其原因是(
- 将紫色洋葱在完全营养液中浸泡一段时间,撕取外表皮,先用浓度为0.3g.mL的蔗糖溶液处理,细胞发生质壁分离后,立即将外表
- 一定条件下,在密闭容器中,能表示反应X(气)+ 2Y(气) 2Z(气)一定达到化学平衡状态的是
- _______ are English people’s favorite , and they are often c
- 根据下面给出的数轴,解答下面的问题: (1)请你根据图中A、B两点的位置,分别写出它们所表示的有理数 A: ___
- 目前,化学家们已合成了一系列有机物:根据这一系列有机物的规律,试回答:(1)写出联m苯的化学式(用m表示)_______
- 对下列实验过程的评价,正确的是( )A.某溶液滴加BaCl2溶液,生成不溶于稀硝酸的白色沉淀,该溶液中不一定含有SO42
- 用如图所示的装置研究在作用力F一定时,小车的加速度a与小车质量M的关系,某位同学设计的实验步骤如下:A.用天平称出小车和
- The dull wetland _____ the moment the first ray of sunlight



