第一单元 研究物质的实验方法 知识点题库
已知A、B、C、D、E、F、G为中学化学中常见的化合物,其中A是淡黄色固体,B是无色液体,G为红褐色沉淀.常温下甲、乙、丙为气态非金属单质,丙呈黄绿色;丁、戊为常见金属单质,其中戊是当前用量最大的金属.它们之间的转化关系如下图所示(有的反应部分产物已经略去).请根据以上信息回答下列问题:
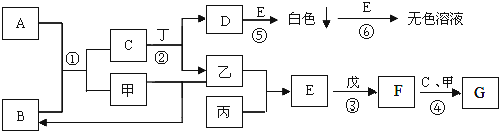
(1)写出下列物质的化学式:A ,E ,戊 .
(2)F转化为G的过程中出现的现象是: .
(3)写出②中反应的离子方程式: .
(4)①~⑥转化中不含有氧化还原反应的是: (填序号).
以硅藻土为载体的五氧化二钒(V2O5)是接触法生产硫酸的催化剂.从废钒催化剂中回收V2O5既避免污染环境
又有利于资源综合利用.废钒催化剂的主要成分为:
物质 | V2O5 | V2O4 | K2SO4 | SiO2 | Fe2O3 | Al2O3 |
质量分数/% | 2.2~2.9 | 2.8~3.1 | 22~28 | 60~65 | 1~2 | <1 |
以下是一种废钒催化剂回收工艺路线:
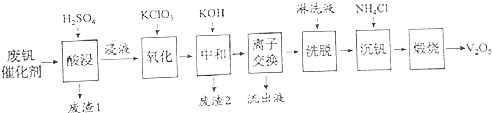
回答下列问题:
-
(1) “酸浸”时V2O5转化为VO2+ , 反应的离子方程式为,同时V2O4转成VO2+ . “废渣1”的主要成分是.
-
(2) “氧化”中欲使3 mol的VO2+变为VO2+ , 则需要氧化剂KClO3至少为mol.
-
(3) “中和”作用之一是使钒以V4O124﹣形式存在于溶液中.“废渣2”中含有.
-
(4)
“离子交换”和“洗脱”可简单表示为:4ROH+V4O124﹣
 R4V4O12+4OH﹣(以ROH为强碱性阴离子交换树脂).为了提高洗脱效率,淋洗液应该呈性(填“酸”“碱”“中”).
R4V4O12+4OH﹣(以ROH为强碱性阴离子交换树脂).为了提高洗脱效率,淋洗液应该呈性(填“酸”“碱”“中”). -
(5) “流出液”中阳离子最多的是.
-
(6) “沉钒”得到偏钒酸铵(NH4VO3)沉淀,写出“煅烧”中发生反应的化学方程式.
①钠与水反应生成NaOH和H2;所有金属与水反应都生成碱和H2
②铁露置在空气中一段时间后就会生锈;性质更活泼的铝不能稳定存在于空气中
③化合物NaCl的焰色为黄色;Na2CO3的焰色也为黄色
④密度为1.1g•cm﹣3与密度为1.2g•cm﹣3的NaCl溶液等体积混合,所得NaCl溶液的密度介于1.1g•cm﹣3与1.2g•cm﹣3之间;NaK合金的熔点应介于Na和K熔点之间.
-
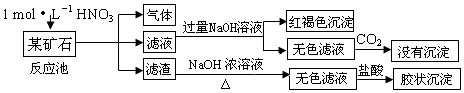
(1) 用滤渣制备粗硅的化学反应方程式为
-
(2) 下列说法正确的是
a.酸性:H2CO3>H2SiO3b.结合质子的能力:CO32﹣>AlO2﹣>HCO3﹣
c.稳定性:H2O>CH4>SiH4d.离子半径:O2﹣<Al3+
-
(3) 滤渣和NaOH溶液反应的离子方程式是,通过 现象说明此矿山中不含Al2O3
-
(4) 该矿石和稀HNO3发生氧化还原反应的离子方程式为.
物质 | 熔点/℃ | 沸点/℃ | 密度/g•cm﹣3 | 溶解性 |
乙二醇 | ﹣11.5 | 198 | 1.11 | 易溶于水和乙醇 |
丙三醇 | 17.9 | 290 | 1.26 | 能跟水、酒精以任意比互溶 |
请用下图所示的仪器分离以上各混合液,仪器和方法不能对应的是( )
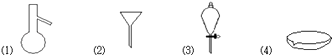
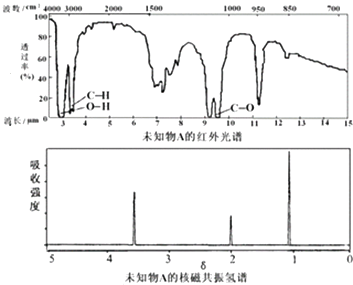
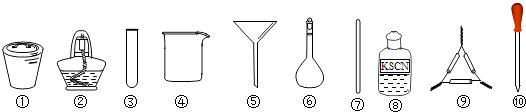
①加热试管时,先均匀加热,后局部加热 ②做H2还原CuO实验时,先通H2 , 后加热CuO,反应完毕后,先撤酒精灯待试管冷却,后停止通H2 ③制取气体时,先检查装置气密性,后装药品 ④点燃可燃性气体如H2、CO等时,先检验气体纯度,后点燃 ⑤制取蒸馏水时,先通冷却水,后加热蒸馏烧瓶 ⑥进行分液操作时,先从上口倒出上层液体,后从通过下端活塞放出下层液体
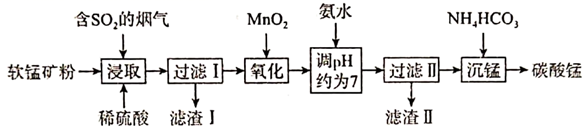
已知:①酸性条件下MnO2与CuS反应生成淡黄色沉淀;
②部分阳离子沉淀时溶液的pH。
|
离子 |
Al3+ |
Fe3+ |
Fe2+ |
Mn2+ |
Cu2+ |
|
开始沉淀的pH |
4.1 |
2.2 |
5.8 |
8.8 |
4.2 |
|
沉淀完全的pH |
4.7 |
3.2 |
8.8 |
10.1 |
6.7 |
请回答下列问题:
-
(1) 滤渣Ⅰ的主要成分是(填物质名称)。
-
(2) “氧化”步骤中,加入MnO2氧化的离子是,检验该离子被完全氧化的方法是。
-
(3) 加入氨水调节溶液的pH约为7,其目的是。
-
(4) “沉锰”步骤中,加入NH4HCO3时反应的离子方程式为。
-
(5) 碳酸锰纯度的测定:称量18.00 g碳酸锰样品(杂质不参加反应),溶于过量的稀硫酸中,向所得溶液中加入稍过量的磷酸和硝酸,加热发生反应:2Mn2++NO3-+4PO43-+2H+
 2[Mn(PO4)2]3-+NO2-+H2O。除去溶液中的NO3-和NO2- , 加入100.00 mL 2.00 mol/L的(NH4)2Fe(SO4)2溶液,发生反应[Mn(PO4)2]3-+Fe2+=Mn2++Fe3++2 PO43-;再用1.00 mol/L酸性K2Cr2O7溶液氧化过量的Fe2+ , Fe2+反应完全时消耗10.00 mL酸性K2Cr2O7溶液。则碳酸锰样品纯度为%。(保留三位有效数字)。
2[Mn(PO4)2]3-+NO2-+H2O。除去溶液中的NO3-和NO2- , 加入100.00 mL 2.00 mol/L的(NH4)2Fe(SO4)2溶液,发生反应[Mn(PO4)2]3-+Fe2+=Mn2++Fe3++2 PO43-;再用1.00 mol/L酸性K2Cr2O7溶液氧化过量的Fe2+ , Fe2+反应完全时消耗10.00 mL酸性K2Cr2O7溶液。则碳酸锰样品纯度为%。(保留三位有效数字)。
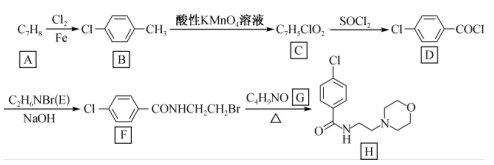
回答下列问题:
-
(1) A 的名称,E中的官能团名称为。
-
(2) C的结构简式为 ,D→ F的反应反应类型为 。
-
(3) F+G →H 的化学方程式为。
-
(4) C的同分异构体中满足下列条件的有种(不考虑立体异构)。
①属于芳香族化合物②能发生银镜反应其中核磁共振氢谱有3组峰且峰面积比为2:2:1的结构简式为。
-
(5) 参照上述合成路线,写出以
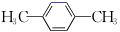 和CH3NH2为原料合成
和CH3NH2为原料合成 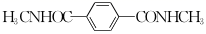 路线:(无机试剂任选)。
路线:(无机试剂任选)。
-
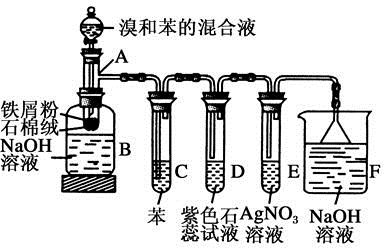
(1) 向反应容器A中逐滴加入溴和苯的混合液,几秒内就发生反应。写出A中所发生反应的化学方程式(有机物写结构简式):。
-
(2) B中NaOH溶液的作用是。
-
(3) 试管C中苯的作用是。反应开始后,观察D和E两试管,看到的现象为,此现象可以验证苯和液溴的反应为(填反应类型)。
-
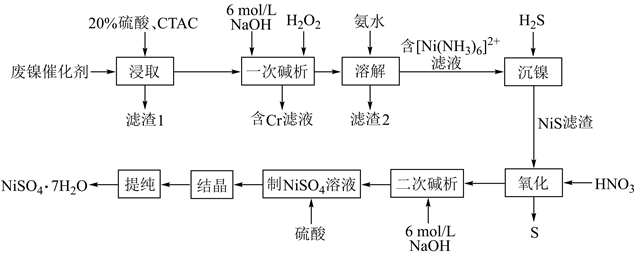
(1) “浸取”时,在硫酸浓度和用量、溶解时温度、搅拌速率均一定时,提高镍的回收率还可采取的措施是(写出一条)。
-
(2) “滤渣1”的主要成分是。
-
(3) “一次碱析”时,Cr(OH)3转化为的CrO
 的离子方程式为。
的离子方程式为。
-
(4) 加氨水“溶解”的目的是,‘滤渣 2”的主要成分是。
-
(5) “氧化”时,HNO3被还原为NO,该反应的化学方程式为。
-
(6) 已知0.01mol•L-1Ni(NO3)2开始沉淀时的pH为7.2,计算Ni(OH)2的Ksp=(列出计算式),则“二次碱析”使Ni2+沉淀完全时(c=1.0×10—5 mol•L-1)的pH为。
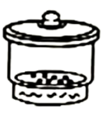 B .
B . 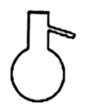 C .
C . 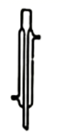 D .
D . 
 是无公害型冷却水系统的金属腐蚀抑制剂,工业上利用钼精矿(主要成分是不溶于水的
是无公害型冷却水系统的金属腐蚀抑制剂,工业上利用钼精矿(主要成分是不溶于水的 , 含少量
, 含少量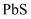 等)制备钼酸钠的工艺如图所示。
等)制备钼酸钠的工艺如图所示。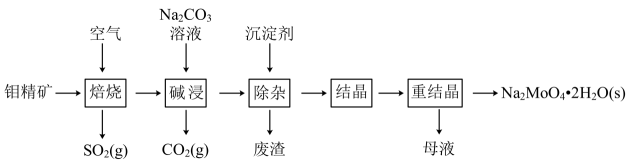
回答下列问题:
-
(1)
 中钼元素的化合价是。
中钼元素的化合价是。
-
(2) “焙烧”时空气从炉底进入,矿石经粉碎后从炉顶进入,这样处理的目的是,“焙烧”时
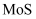 , 转化为
, 转化为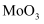 , 反应的化学方程式为。
, 反应的化学方程式为。
-
(3) 碱浸”所得
 溶液中含
溶液中含 杂质,其中
杂质,其中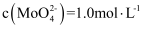 ,
, 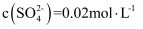 , 在结晶前需加入
, 在结晶前需加入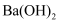 固体以除去溶液中的
固体以除去溶液中的 。当
。当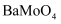 开始沉淀时,
开始沉淀时, 的去除率是。[
的去除率是。[ , 溶液体积变化忽略]。
, 溶液体积变化忽略]。
-
(4) “重结晶”的具体操作为。
-
(5) 另一种利用钼精矿制备钼酸钠的工艺流程中,直接向粉碎后的钼精矿中加入
 溶液和
溶液和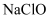 溶液来得到钼酸钠,反应的离子方程式为,该工艺的优点是。(任写一条)
溶液来得到钼酸钠,反应的离子方程式为,该工艺的优点是。(任写一条)
-
(6)
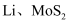 可充电电池的工作原理为:
可充电电池的工作原理为: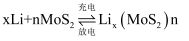 , 则电池充电时阳极的电极反应式为。
, 则电池充电时阳极的电极反应式为。
- 下列“上海合作组织”成员国中,不与我国接壤的是: A.哈萨克斯坦 B.乌兹别克斯坦
- 某热电厂用脱硫方法得到CaSO4生产K2SO4的工艺流程如下。 【资料】碳酸铵在水溶液中温度高于70℃时开始
- 亚洲有世界上最高大雄伟的喜马拉雅山脉,它的形成是由于( ) A.亚欧板块和非洲板块碰撞 B.亚欧板块和美洲
- 圆上的点到直线的距离最大值是_______________
- 本初子午线是指 A、180°经线 B、0°经线 C、东西半球分界线
- 复数 A. B. C. D.
- 在横线上分别填上由下列命题构成的“p∨q”“p∧q”“p”形式的复合命题的真假:p:3×3=6,q:3+3=6,则p∨q
- 用毛皮摩擦过的气球能吸附在墙面上不掉下来,下列现象与其实质相同的是()A.寒冷的冬天用湿手摸户外的金属单杠,手会被粘上B
- 一个历史事实可以有若干事件构成,事件又可以由若干小事件构成,由此可以排出事件的等级或层次,下列选项符合上述说法的是 A.
- (08年江苏卷)二战后,德国和朝鲜形成分裂局面的相同原因是( ) A.国内民族矛盾的激化 B.美国和苏联的相互对抗
- 如图是单克隆抗体制备过程示意图,其中1过程注射的物质和A细胞的名称分别为() A.抗体、T淋巴细胞 B. 抗
- 原子序数由小到大排列的四种短周期元素X、Y、Z、W,四种元素的原子序数之和为32,在周期表中X是原子半径最小的元素,Y、
- 鉴别下列各组物质,所用两组试剂均正确的是( )待鉴别的物质 鉴别试剂1 鉴别试剂2 A 稀盐酸和稀硫酸 氯化
- 下列各项中对课文理解有误的一项是( )。(2分)A.《女娲造人》是根据中国古代神话改写的,全文处处洋溢着人类诞生的喜
- 造成青少年近视的原因是A.晶状体变形,发生实质性的病变 B.眼球的前后径过长,物象落在视网膜的前方 C.晶状体混浊,不
- 下列各项中,没有语病的一项是(3分)() A.在国务院常务办公会做出“扩大房地产税试点范围”的决定后,财政部、住房和城乡
- ﹣的相反数是() A.﹣8 B. C.0.8 D.8
- 12.阅读下面的文字,完成下列小题。 乡 关 向延波 曾经,谁家的屋檐下都趴着一只忠实的黄狗,谁家的竹林里都养着一群
- 从“三角贸易”中获利最大的国家是 A.法国B.德国C.西班牙D.英国
- “善为国者,必先富民,然后治之。”进入“十二五”历史新起点,党和国家将“民富”目标摆到更加突出的地位。要实现这一目标,



