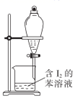
第一单元 研究物质的实验方法 知识点题库
已知下列氧化剂均能氧化+4价的硫元素,为了除去稀硫酸中混有的亚硫酸,应选用的最合理的氧化剂是( )
A . KMnO4
B . Ca(ClO)2
C . Cl2
D . H2O2
将下列各组中的每种有机物分别放入水中,振荡后再静置,液体分层且该组的全部物质都能浮在水的上层的是( )
A . 1﹣己炔、甲苯、十一烷
B . 乙醇、苯、溴苯
C . 乙二醇、乙醛、硝基苯
D . 溴苯、四氯化碳、乙酸钠
工业上用菱锰矿(MnCO3)[含FeCO3、SiO2、Cu2(OH)2CO3等杂质]为原料制取二氧化锰,其流程示意图如下:
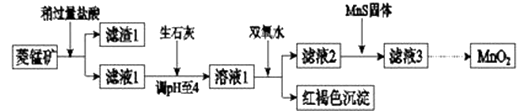
已知:生成氢氧化物沉淀的pH
|
|
Mn(OH)2 |
Fe(OH)2 |
Fe(OH)3 |
Cu(OH)2 |
|
开始沉淀时 |
8.3 |
6.3 |
2.7 |
4.7 |
|
完全沉淀时 |
9.8 |
8.3 |
3.7 |
6.7 |
注:金属离子的起始浓度为0.1mol/L,回答下列问题:
-
(1) 含杂质的菱锰矿使用前需将其粉碎,主要目的是.盐酸溶解MnCO3的化学方程式是.
-
(2) 向溶液1中加入双氧水时,反应的离子方程式是.
-
(3) 滤液2中加入稍过量的难溶电解质MnS,以除去Cu2+ , 反应的离子方程式是.
-
(4) 将MnCl2转化为MnO2的一种方法是氧化法.其具体做法是用酸化的NaClO3溶液将MnCl2氧化,该反应的离子方程式为:Mn2++ClO3﹣+ = + +.
-
(5) 将MnCl2转化为MnO2的另一种方法是电解法.
①阳极生成MnO2的电极反应式是.
②若直接电解MnCl2溶液,生成MnO2的同时会产生少量Cl2 . 检验Cl2的操作是.
③若在上述MnCl2溶液中加入一定量的Mn(NO3)2粉末,则无Cl2产生.其原因是.
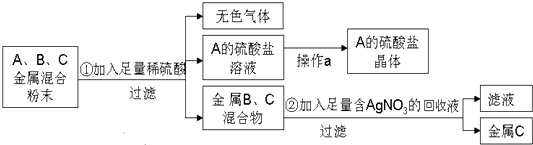
化学实验室要从含少量铜粉的银、锰(Mn)混合金属粉末中分离出贵金属,并获得一种盐晶体,将有关三种金属随意编号为:A、B、C,并设计了如下流程:
-
(1) A、B、C三种金属的活动性顺序为>>.
-
(2) 金属C是,操作a的名称是.
-
(3) 已知A的硫酸盐中A元素显+2价,请写出步骤①的反应的化学方程式:.
在从碘水中萃取碘的实验中,下列说法正确的是( )
A . 萃取剂要求不溶于水,且比水更容易使碘溶解
B . 注入碘水和萃取剂,倒转分液漏斗反复用力振荡后立即分液
C . 萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大
D . 实验室如果没有四氯化碳,可以用酒精代替
下列化学实验基本操作中,正确的是( )
A . 稀释浓硫酸时,把浓硫酸慢慢倒入盛有水的量筒中并搅拌
B . 用胶头滴管向试管中加入液体时,胶头滴管紧贴试管内壁
C . 分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出
D . 用托盘天平称量物质时,称量物质放在右盘,砝码放在左盘
下列说法中错误的是( )
A . K2FeO4可代替Cl2处理饮用水,有杀菌消毒作用
B . CaO2属于碱性氧化物,也属于离子化合物,其阴阳离子个数比为1:2
C . 《本草纲目》中“以火烧之,紫青烟起,乃真硝石”利用焰色反应区分硝石(KNO3)和朴硝(Na2SO4)
D . 高温下可用金属钠还原四氯化钛来制取金属钛
《开宝本草》中记载了如何提取硝酸钾:“此即地霜也,所在山泽,冬月地上有霜,扫取以水临汁后,乃煎炼而成”。文中对硝酸钾的提取没有涉及的操作及方法是( )
A . 溶解
B . 蒸发
C . 结晶
D . 萃取
利用废旧镀锌铁皮制备磁性Fe3O4胶体粒子及副产物ZnO,制备流程图如下:
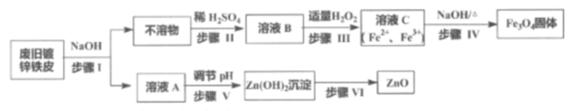
已知反应:①Zn+2NaOH=Na2ZnO2+H2↑②Zn(OH)2+2NaOH=Na2ZnO2+2H2O
回答下列问题:
-
(1) 步骤I中的分离操作名称是,溶液A中的溶质有(填化学式)。
-
(2) 步骤Ⅲ中反应的离子方程式是。
-
(3) 证明溶液B中含有Fe2+的方法是。
-
(4) 步骤Ⅴ可选用的试剂是(填序号)。
a. NaOH溶液
b. 氨水
c. 盐酸
-
(5) 在工业上常用水热法制造Fe3O4胶体粒子,有利于提高其纯度和磁性能,主要反应过程为:Fe2++S2O32-+O2+OH- →Fe3O4(胶体)+S4O62-+H2O,若反应过程中产生的Fe3O4(胶体)与S4O62-均为1mol,则参加反应的氧气在标准状况下的体积为L。
实验室中,下列行为不符合安全要求的是( )
A . 熄灭酒精灯时,用灯帽盖灭
B . 金属钠着火时,立即用沙土覆盖
C . 实验结束后将废液倒入指定容器中
D . 稀释浓硫酸时,将水注入浓硫酸中并不断搅拌
下列有关有机化合物的说法错误的是( )
A . 可用甲苯萃取溴水中的溴
B . 可用NaHCO3溶液鉴别乙酸和乙醇
C . C4H8O2的同分异构体中属于酯类的有5种
D . 2-甲基丁烷又名异戊烷
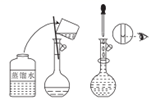
下列图示的三种实验操作名称从左到右依次是( )
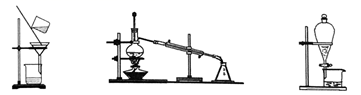
A . 过滤、蒸发、分液
B . 蒸馏、过滤、分液
C . 过滤、蒸馏、分液
D . 分液、蒸馏、过滤
高分子化合物 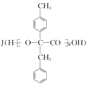 的合成路线如图:
的合成路线如图:
 的合成路线如图:
的合成路线如图: 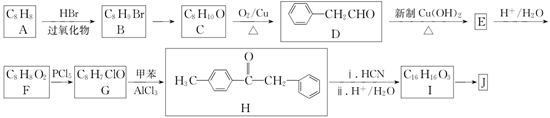
已知:Ⅰ. 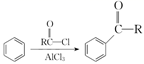
Ⅱ. 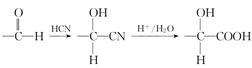
回答下列问题:
-
(1) A的化学名称为。
-
(2) 由F生成G的反应类型是。
-
(3) B→C反应所需试剂,条件分别为、。
-
(4) H的分子式为。
-
(5) Ⅰ中官能团的名称是。
-
(6) 写出一种与F互为同分异构体的酯类芳香族化合物的结构简式(核磁共振氢谱为四组峰,峰面积比为1:2:2:3):。
-
(7) 分别写出A→B,C→D反应的化学方程式:、。
下列实验操作描述正确且能达到实验目的的是( )
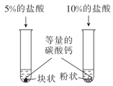
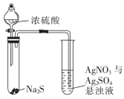
| A | B | C | D |
| | | | |
| 苯萃取碘水后的分离操作 | 配制 1 mol/L的NaCl溶液时的定容操作 | 探究接触面积对反应速率的影响 | 验证Ksp(AgSO4)>Ksp(Ag2S) |
A . A
B . B
C . C
D . D
下列说法正确的是( )
A . 四氯化碳、酒精均可用于萃取碘水中的碘单质
B . 氯化铝溶液中加入过量NaF溶液,无明显现象,再加入过量氨水,产生白色沉淀
C . 纸层析法分离Fe3+和Cu2+时,用胶头滴管取待测样品在距滤纸条末端2cm处重复点样,使斑点直径小于0.5cm
D . 氯酸钾、高锰酸钾、硝酸钾等强氧化剂不能研磨,否则将引起爆炸
下列实验操作错误的是( )
A . 实验室制备氯气时在通风橱中进行
B . 实验剩余的钠放回试剂瓶中
C . 不慎打翻燃着的酒精灯,立即用湿抹布盖灭
D . 试管中残留的 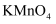 溶液,直接倒入水槽中
溶液,直接倒入水槽中
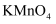 溶液,直接倒入水槽中
溶液,直接倒入水槽中
从高铝粉煤灰(主要成分为 、
、 、
、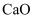 、
、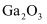 、
、 等)中回收金属
等)中回收金属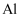 、
、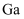 并制备电池正极材料
并制备电池正极材料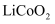 的工艺流程如下图所示:
的工艺流程如下图所示:
 、
、 、
、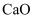 、
、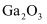 、
、 等)中回收金属
等)中回收金属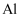 、
、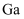 并制备电池正极材料
并制备电池正极材料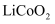 的工艺流程如下图所示:
的工艺流程如下图所示: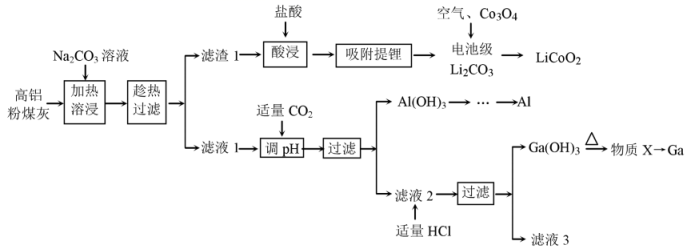
已知:①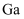 与
与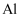 同主族,其化学性质相似。
同主族,其化学性质相似。
②随着温度升高,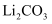 在水溶液中的溶解度减小:
在水溶液中的溶解度减小:
温度/ | 0 | 20 | 40 | 60 | 80 | 100 |
溶解度/ | 1.54 | 1.33 | 1.17 | 1.01 | 0.85 | 0.72 |
③本工艺流程中,不同金属离子形成氢氧化物沉淀的 范围如表格所示:
范围如表格所示:
金属离子 | 形成氢氧化物沉淀的 |
| 3.3~10.6 |
| 2.9~9.4 |
回答下列问题:
-
(1) “滤渣1”的成分除了
 之外还含有。
之外还含有。
-
(2) 已知“酸浸”后铁元素以铁配离子(
 )的形式存在,写出
)的形式存在,写出 在该过程中的离子方程式。
在该过程中的离子方程式。
-
(3) “调
 ”步骤中的范围应为,“滤液2”中镓元素的存在形式为。
”步骤中的范围应为,“滤液2”中镓元素的存在形式为。
-
(4) 工业上通过电解法利用“物质
 ”制备
”制备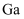 , 反应的化学方程式为。
, 反应的化学方程式为。
-
(5) “
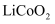 ”中的
”中的 元素化合价为,在“电池级
元素化合价为,在“电池级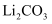 ”转化为“
”转化为“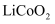 ”的反应中,氧化剂与还原剂物质的量之比为。
”的反应中,氧化剂与还原剂物质的量之比为。
化学与生产、生活息息相关。下列叙述不正确的是( )
A . 橱窗所用有机玻璃为高分子化合物
B . 家庭装修用水性涂料代替油性涂料有利于健康
C . 应用光伏发电可缓解温室效应及减少酸雨发生
D . 用己烷萃取玉米胚芽中的油脂时发生了化学反应
高血脂是一种常见病症,在中老年人当中发病率高,它引起动脉粥硬化,乃至冠心病、脑血栓、脑出血等,危及生命。如图是一种治疗高血脂的新药I的合成路线:
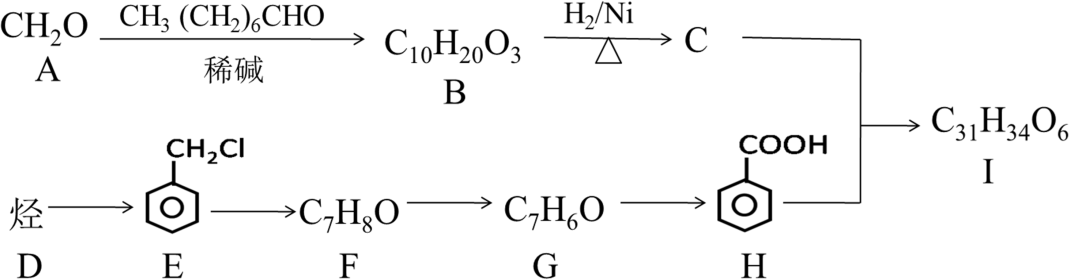
已知:R1CHO+R2CH2CHO
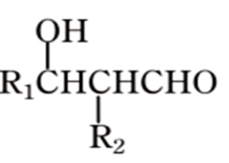 (R可以是氢或烃基)
(R可以是氢或烃基)
回答下列问题:
-
(1) A的化学名称为,A→B的反应类型为。
-
(2) 写出D→E的化学反应方程式。
-
(3) E→F反应的试剂及条件为。
-
(4) 写出C+H→I的化学反应方程式。
-
(5) 1mol化合物I最多能与molNaOH发生反应。
-
(6) J为H的同系物,相对分子质量相差14,符合下列条件的J的同分异构体有种(不含立体异构)。①属于芳香族化合物;②能发生银镜反应;③能与氯化铁发生显色反应。其中核磁共振氢谱有5组吸收峰,且峰面积比为2:2:2:1:1的结构简式为。
-
(7) 丙二酸(HOOCCH2COOH)是有机合成中的重要原料,主要用于医药中间体,也用于香料、粘合剂、树脂添加剂、电镀抛光剂等。请以甲醛和乙醛为原料(其它无机试剂任选),写出丙二酸的合成路线。
下列实验操作正确的是( )
A . 使用pH试纸时可直接用手捏住
B . 焰色试验后,要用稀硫酸洗涤铂丝并在火焰上灼烧至无色
C . 定容时,将蒸馏水沿玻璃棒注入容量瓶,至溶液的凹液面与刻度线相切
D . 强氧化物如KMnO4、KClO3、Na2O2等固体不能随便丢弃,可通过化学反应转化为一般化学品后处理
最近更新
- Caroline doesn't have a gift for music, but she ________ it
- 1 kg铀全部裂变释放出的能量约为8.5×1014 J,相当于完全燃烧多少无烟煤释放的能量?(无烟煤的热值为3.4×10
- Helen always helps her mother even though going to school __
- Two thieves came to a house to steal something, they dug
- 将物体受到两个共点力和合成为一个力,下列说法正确的是( )A.是物体实际受到的一个力B.单独作用时与和共同作用的效
- 根据表中的信息判断下列说法正确的是( )。 物质 金刚石 石墨 外观 无色,透明固体 灰黑,不透明固体 熔点 ? ?
- 下图是两个生态系统中腐殖质总量随时间而发生变化的情况,甲、乙曲线分别代表哪两个生态系统?A. 热带雨林、温带森林
- 人类与大自然关系的最高境界就是 【】 A.人类是大自然的主宰
- 网络反腐的成效被形象地称为“小鼠标绊倒大贪官”。近日,为鼓励广大网民依法如实举报违纪违法行为,回
- 下列命题: ①若A、B、C、D是空间任意四点,则有+++=; ②若共线,则与所在直线平行 ③对空间任意一点O与不共线的三
- 设全集U=R,集合M={x|x>0},N={x|x2≥x},则下列关系中正确的是A.M∩N∈M
- NA为阿伏伽德罗常数,下列说法正确的是 A.18gD2O和18gH2O中含有的质子数均为10NA B.高温下,0.2
- 手机中使用的锂(Li)电池是新型的高能电池,某种锂电池的总反应可表示为Li+MnO2=LiMnO2。此反应中锂元素的化合
- When the disabled sportsman won a gold medal,a lot of people
- 一个英国人在乾隆二十五年(1760年)来到中国,这一年他可能经历的事情是 A.看到机户和机工因工资纠纷到衙门打官司 B.
- 2014年双十一、双十二期间,各大商场纷纷推出优惠折扣战。商家这样做是因为 ①一般来说,某种商品价格下降时,会导致其需求
- ......
- 如果把分子看成是球形的话,那么一般分子直径大约是
- 写出定理“等腰三角形的两个底角相等”的逆命题: , 是
- In many countries in the world, breakfast is a snack