第二节 氯及其化合物 知识点题库
如图是实验室中制备气体或验证气体性质的装置图.回答下列问题:
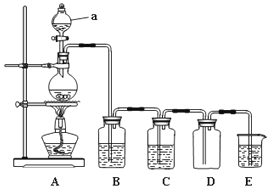
-
(1) 利用图装置制备纯净、干燥的氯气.
①圆底烧瓶内发生反应的化学方程式为 ;若有6mol的HCl参加反应则被氧化的HCl为 mol.
-
(2) 利用图装置证明SO2具有漂白性、还原性及生成气体中含有CO2 . 圆底烧瓶内加入碳,a中加入浓硫酸,B、D中均为少量品红溶液,C中为足量酸性高锰酸钾溶液,E中为澄清石灰水.
①证明SO2具有漂白性的装置是 ;
②证明SO2具有还原性的现象是
③证明生成气体中含有CO2的现象是 ;
④D装置的作用是
按下列实验方法操作,能达到要求的是( )
A . 用托盘天平称量25.20g氯化钠固体
B . 用湿润的氯气和干燥的红色布条,检验氯气的漂白性
C . 用NaOH溶液和FeCl3溶液制备Fe(OH)3胶体
D . 将氢氧化钠固体在容量瓶中溶解,配制一定物质的量浓度的NaOH溶液
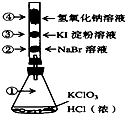
已知常温下氯酸钾与浓盐酸反应放出氯气,现按下图进行氯气的性质实验.玻璃管内装有分别滴有不同溶液的白色棉球,反应一段时间后,对图中指定部位颜色描述正确的是( )
① | ② | ③ | ④ | |
A | 黄绿色 | 橙色 | 蓝色 | 白色 |
B | 无色 | 橙色 | 紫色 | 白色 |
C | 黄绿色 | 橙色 | 蓝色 | 无色 |
D | 黄绿色 | 无色 | 紫色 | 白色 |
A . A
B . B
C . C
D . D
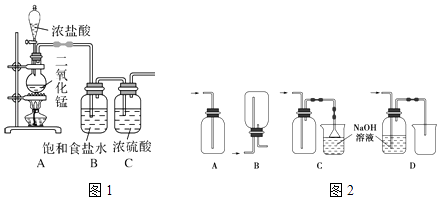
化学实验有助于理解化学知识,形成化学观念,提高探究与创新能力,提升科学素养.在实验室中用浓盐酸与MnO2共热制取Cl2并进行相关实验.
-
(1) 盛浓盐酸的装置名称为.
-
(2) 如图1,装置B的作用是,装置C的作用是
-
(3) 如图2,下列收集Cl2的正确装置是.
-
(4) 写出实验室制取Cl2的化学方程式.
-
(5) 若实验时加入1.74g的二氧化锰则至多生成多少mL Cl2 (标准状况)?
向某溶液中加入BaCl2溶液,再加入稀HNO3至溶液呈酸性,有白色沉淀产生。该溶液一定含有( )
A . CO32―
B . OH―
C . SO42―
D . HCO3―
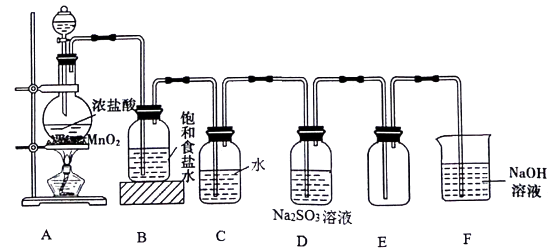
化学探究学习小组的同学用下图所示装置制取氯气并探究氯气的某些性质。
-
(1) 装置A中制取Cl2的化学方程式为。
-
(2) 装置C中发生反应的离子方程式为,反应后溶液中含Cl元素的分子有。
-
(3) 实验结束后,测得装置D溶液中存在大量SO42-。Cl2通过装置D溶液时发生反应的离子方程式为 。
-
(4) 装置F的作用是,该装置中发生反应的离子方程式。
一定量的氢气在氯气中燃烧,所得混合物用100mL3mol/L的NaOH溶液(密度为1.12 g/mL)恰好完全吸收,测得溶液中含有NaClO的物质的量为0.05 mol。
-
(1) 求原NaOH溶液的质量分数。
-
(2) 求所得溶液中Cl-的物质的量。
-
(3) 所用氯气和参加反应的氢气的物质的量之比n(Cl2):n(H2)。
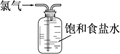
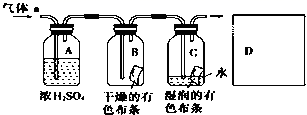
某同学设计如图所示装置探究氯气能否与水发生反应。已知气体a的主要成分是含有少量水蒸气的氯气。请回答下列问题:
-
(1) 浓硫酸的作用是。
-
(2) 写出实验室制取Cl2的化学方程式。
-
(3) 证明氯气和水发生反应的实验现象为。
-
(4) 该实验设计存在的缺陷是,为了克服该缺陷,需要补充装置D,其中发生反应的离子方程式为。
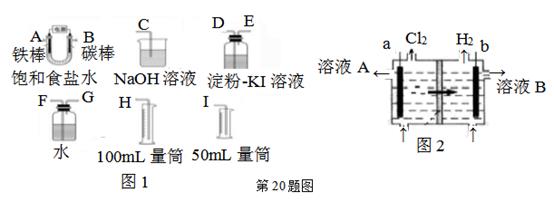
现需设计一套实验装置来电解饱和食盐水,并测量电解产生的氢气的体积(约6
mL)和检验氯气的氧化性(不应将多余的氯气排入空气中)。
-
(1) 试从上图图1中选用几种必要的仪器,连成一整套装置,各种仪器接口的连接顺序(填编号)是:A接,B接。
-
(2) 铁棒接直流电源的极;碳棒上发生的电极反应为。
-
(3) 能说明氯气具有氧化性的实验现象是。
-
(4) 假定装入的饱和食盐水为50 mL(电解前后溶液体积变化可忽略),当测得的氢气为5.6 mL(已折算成标准状况)时,溶液的pH为。
-
(5) 工业上采用离子交换膜法电解饱和食盐水,如上图图2,该离子交换膜是(填“阳离子”或“阴离子”)交换膜,溶液A是(填溶质的化学式)
既能使石蕊试液变红,又能使品红试液变为无色,还能使溴水褪色的是( )
A . Cl2
B . H2S
C . SO2
D . CO
设NA为阿伏加德罗常数的值。下列说法正确的是( )
A . 标准状况下,2.24L SO3中所含原子数为0.4NA
B . 10mL 12mol/L盐酸与足量MnO2加热反应,制得Cl2的分子数为0. 03NA
C . 0.1mol CH4与0.4mol Cl2在光照下充分反应,生成CCl4的分子数为0.1NA
D . 常温常压下,6g乙酸中含有C-H键的数目为0.3NA
下列各种物理性质中,对氯气来说错误的是( )
A . 黄绿色的气体
B . 密度比空气小
C . 能溶于水
D . 有刺激性气味
-
(1) Ⅰ.某课外活动小组将下图所示装置按一定顺序连接,在实验室里制取一定量的FeCl3(所通气体过量并充分反应)。请回答下列问题:
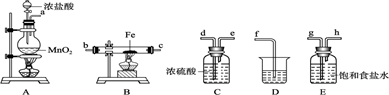
A 中发生反应的化学方程式为。在该反应中当 0.4molHCl发生反应时,生成标准状况下的Cl2 的体积为。浓盐酸在反应中显示出来的性质是(填序号);
A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
-
(2) 各装置的正确连接顺序为(填写装置代号)A→→→→D。
-
(3) 装置 E 的作用是。写出装置 D(D中所盛溶液为 NaOH)中反应的化学方程式
-
(4) 工业上用电解法制备氯气的化学方程式为:。
-
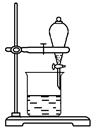
(5) Ⅱ.某小组用CCl4萃取碘水中的碘,在下图的分液漏斗中,下层液体呈色;他们打开分液漏斗活塞,却未见液体流下,原因可能是
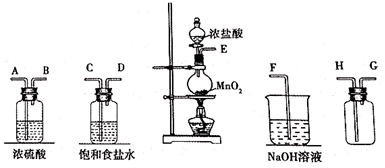
氯气广泛应用于杀菌、消毒及化工领域,某化学小组设计如图装置制备少量干燥纯净的氯气,试回答下列问题:
-
(1) 盛有浓盐酸仪器名称 ,装置的正确连接顺序为;
-
(2) 气体发生装置中发生反应的化学方程式为;
-
(3) 题给装置中饱和食盐水的作用是 ,检验氯气是否收集满的方法是 ;
-
(4) 写出尾气吸收装置中反应的离子方程式 ;
-
(5) 工业上常用氯气制备“84消毒液”,它能有效杀灭新冠病毒,某品牌84消毒液:含25%NaClO、1000 mL、密度1.192 g·cm -3。该品牌消毒液需要稀释后才能使用,某化学实验小组用该品牌消毒液配制1000mL0.2mol·L-1的稀溶液。
①量取84消毒液 mL;
②定容时仰视刻度线,所配溶液浓度会 (填“偏高”、“偏低”或“无影响”),此时应采取的处理方法。
在含有NaBr和NaI的溶液中通入足量的  ,然后把溶液蒸干并将剩余残渣灼烧,最后留下的物质是( )
,然后把溶液蒸干并将剩余残渣灼烧,最后留下的物质是( )
 ,然后把溶液蒸干并将剩余残渣灼烧,最后留下的物质是( )
,然后把溶液蒸干并将剩余残渣灼烧,最后留下的物质是( )
A . NaCl和NaBr的混合物
B . NaCl和  C . NaCl
D . NaCl、
C . NaCl
D . NaCl、  和
和 
 C . NaCl
D . NaCl、
C . NaCl
D . NaCl、 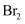 和
和 
 与
与  的氧化性相近,在自来水消毒和果蔬保鲜等方面应用广泛。
的氧化性相近,在自来水消毒和果蔬保鲜等方面应用广泛。 某兴趣小组通过如下装置(夹持装置略)对  制备、吸收、释放和应用进行了研究。
制备、吸收、释放和应用进行了研究。
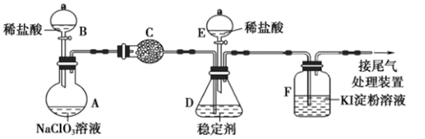
已知:装置  中的药品可以吸收氯气。回答下列问题:
中的药品可以吸收氯气。回答下列问题:
-
(1) 打开
 的活塞,
的活塞,  中发生反应生成
中发生反应生成  ,请将化学方程式配平
,请将化学方程式配平 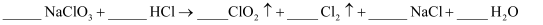 。
。 -
(2) 吸收
 气体的稳定剂Ⅰ和稳定剂Ⅱ,加酸后释放
气体的稳定剂Ⅰ和稳定剂Ⅱ,加酸后释放  的浓度随时间的变化如下图所示。
的浓度随时间的变化如下图所示。 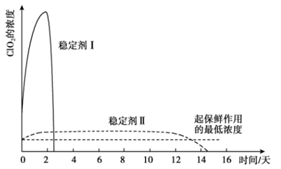
若将其用于水果保鲜,你认为效果较好的稳定剂是,原因是。
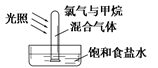
下列关于氯气的实验装置能达到实验目的的是( )
| A | B | C | D |
| | | | |
| 干燥氯气 | 收集氯气 | 探究氯气与甲烷的反应 | 证明氯气具有漂白性 |
A . A
B . B
C . C
D . D
下列氯化物中,只能由金属和氯气直接反应制得,不能由金属和盐酸反应制得的是( )
A . MgCl2
B . FeCl2
C . FeCl3
D . AlCl3
化学是一门充满神奇色彩而又非常实用的科学,下列叙述错误的是( )
A . 探索原子、分子的特征和行为,从而控制原子、分子之间的反应
B . 分析自然界物质构成,以便在工厂中实现规模生产
C . 漂白粉在空气中久置变质,是因为其中的CaCl2与空气中的CO2反应生成CaCO3
D . CCl4和钠在700℃时反应生成纳米级金刚石和另一种化合物,其可能是NaCl
氯化法制取FeCl3流程:以废铁屑和氯气为原料,在立式反应炉里反应,生成的氯化铁蒸气和尾气由炉的顶部排出,进入捕集器冷凝为固体结晶,实验室模拟该方法的装置如下图所示,下列说法错误的是( )
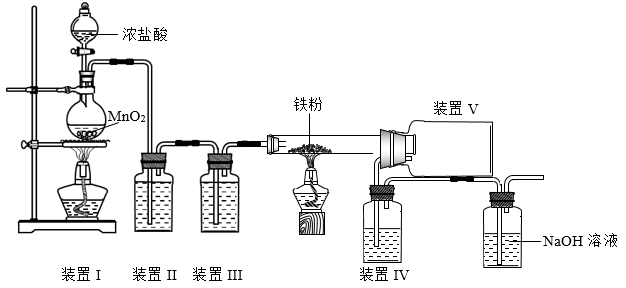
A . 装置I反应的离子方程式为 B . 装置II洗气瓶中加入饱和氯化钠溶液除去Cl2中的少量HCl
C . 装置IV洗气瓶中盛放的液体为浓盐酸
D . 装置V的作用是收集FeCl3
B . 装置II洗气瓶中加入饱和氯化钠溶液除去Cl2中的少量HCl
C . 装置IV洗气瓶中盛放的液体为浓盐酸
D . 装置V的作用是收集FeCl3
 B . 装置II洗气瓶中加入饱和氯化钠溶液除去Cl2中的少量HCl
C . 装置IV洗气瓶中盛放的液体为浓盐酸
D . 装置V的作用是收集FeCl3
B . 装置II洗气瓶中加入饱和氯化钠溶液除去Cl2中的少量HCl
C . 装置IV洗气瓶中盛放的液体为浓盐酸
D . 装置V的作用是收集FeCl3
最近更新
- 一容器中X元素构成的气态单质X2分子有3种,相对分子质量分别为32、34、36。又知容器中3种分子数之比为15∶4∶1。
- 为探究一溴环己烷()与NaOH的醇溶液共热发生的是水解反应还是消去反应,甲、乙、丙三位同学分别设计如下三个实验方案: 甲
- 某校地理研究性学习小组考察了我国某区域一段河流(如图,虚线部分表示是主航道中心线)。读图后回答:(1)该研究小组考察的区
- 若方程的两根恰好互为相反数,则的值为( ) A.4 B. –4
- 下图表示“北半球某区域等压线分布图”,回答10—11题。10、图7中A、B、C、D四个箭头中正确表示风向的是( )
- 用天平和量筒测定盐水的密度,有如下操作:A.用天平称出烧杯和盐水的总质量M;B.用天平称出烧杯和剩下盐水的总质量m;C.
- 有NaCl和NaI的混合物共26.7 g,溶于水,通入足量氯气后,蒸干、灼烧,固体质量变为17.55 g。求原混合物中氯
- 如图,点A在x轴上,OA=4,将线段OA绕点O顺时针旋转120°至OB的位置. (1)求点B的坐标; (2)求经过点A、
- The writer emphasizes the importance of being completely hon
- 现代信息技术的三大基础是信息的__________、__________和__________.
- 明清时期,统治者实行“海禁”和“闭关锁国”政策的根本目的是( ) A.保护农耕经济 B.限制工商业发
- 今天,影视、报刊、图书出版、音像、教育、体育等文化产品、文化活动,充斥了人们的整个生活。新的经济形式如网络经济、假日经济
- ------It was really very kind of you to give me a life home.
- 已知:如图,AB=AC,AD⊥BC于D,点E在AD上,图中共有对全等三角形.
- 在草原上人工种草,为防止鸟把草籽吃掉,用网把实验区罩上。后来发现,草的叶子几乎被虫子吃光。造成这种现象的原因是( )
- 五、现代文(文学类)阅读(21分) 阅读下面的文章,回答15-18小题。 我改变的事物 刘亮程 ①我年轻力盛的那些年,常
- 如图所示,放在水平地面上的物体所受重力为G,系着它的一根竖直轻绳绕过光滑滑轮,它的另一端受的拉力为,地面对物体的支持力为
- 正常情况下,有可能存在等位基因的是 A.一个四分体上
- 在水中充分搅拌,能形成溶液的是 A.面粉 B.花生油 C.食盐 D.冰块
- 下面是三种组成蛋白质的氨基酸的结构式,据图下列叙述不正确的是() A. 以上这三种氨基酸的R基依次分别是﹣H