4.1 物质在溶解过程中有能量变化吗? 知识点题库
在粗盐提纯的实验中,蒸发时正确的操作是( )
A . 把浑浊的液体倒入蒸发皿内加热
B . 开始析出晶体后用玻璃棒搅拌
C . 待水分完全蒸干后停止加热
D . 蒸发皿中出现大量固体时即停止加热
下列变化过程与能量的说法中正确的是( )
A . 中和反应是吸热反应
B . 燃烧属于放热反应
C . 化学键断裂放出能量
D . 吸热反应中,反应物总能量大于生成物总能量
下列化工生产原理错误的是( )
①可以电解熔融的氯化钠来制取金属钠;
②可以将钠加入氯化镁饱和溶液中制取镁;
③用电解法冶炼铝时,原料是氯化铝;
④高炉炼铁的反应是放热的,故无需加热.
A . ②③
B . ①③
C . ①②③
D . ②③④
下列分别是利用不同能源发电的实例图形,其中不属于新能源开发利用的是( )
A .  风力发电
B .
风力发电
B .  太阳能发电
C .
太阳能发电
C .  火力发电
D .
火力发电
D .  潮汐能发电
潮汐能发电
 风力发电
B .
风力发电
B .  太阳能发电
C .
太阳能发电
C .  火力发电
D .
火力发电
D .  潮汐能发电
潮汐能发电
美国研究人员将CO和O附着在一种钌催化剂表面,用激光脉冲将其加热到2000K,成功观察到CO与O形成化学键生成CO2的全过程.下列说法不正确的是( )

A . CO2属于酸性氧化物
B . CO与O形成化学键的过程中放出能量
C . 钌催化剂可以改变该反应的焓变
D . CO与O形成化学键的过程中有电子转移
下列说法错误的是( )
A . 化学反应必然伴随发生能量变化
B . 石灰石烧制石灰是吸热反应
C . 反应的活化能越大,该化学反应前后的能量变化就越大
D . 将AgNO3溶液滴加到KCl溶液中,反应的活化能几乎为零
下列说法中正确的是( )
A . 在化学反应过程中,发生物质变化的同时不一定发生能量变化
B . 生成物全部化学键形成时所释放的能量大于破坏反应物全部化学键所吸收的能量时,反应为吸热反应
C . 有气体参加的化学反应,若增大压强(即缩小反应容器的体积),可增加活化分子的百分数,从而使反应速率增大
D . 升高温度能使化学反应速率增大,主要原因是增加了反应物分子中活化分子的百分数
下列关于能量变化的说法正确的是( )
A . 冰融化成水放出热量
B . 化学键断裂过程一定放出能量
C . 生成物的总能量一定低于反应物的总能量
D . 化学键的断裂和形成是化学反应中能量变化的主要原因
下列有关能量的说法正确的是( )
A . 化学能可转变为电能
B . 化学变化时断裂化学键需放出能量
C . 化学反应能量转换遵守能量守恒定律
D . 化学反应伴随能量变化是化学反应基本特征之一
下列反应中属于吸热反应同时又是氧化还原反应的是( )
A . 灼热的炭与CO2反应
B . 铝与稀盐酸
C . Ba(OH)2·8H2O与NH4Cl反应
D . Na2O2与H2O的反应
下列反应过程中的能量变化与图一致的是( )
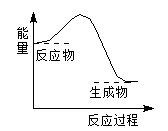
A . 2Al+Fe2O3  2Fe+Al2O3
B . C+CO2
2Fe+Al2O3
B . C+CO2  2CO
C . CaCO3
2CO
C . CaCO3  CaO+CO2↑
D . C+H2O
CaO+CO2↑
D . C+H2O  CO+H2
CO+H2
 2Fe+Al2O3
B . C+CO2
2Fe+Al2O3
B . C+CO2  2CO
C . CaCO3
2CO
C . CaCO3  CaO+CO2↑
D . C+H2O
CaO+CO2↑
D . C+H2O  CO+H2
CO+H2
下列说法不正确的是( )
A . 某试样焰色反应呈黄色,则试样中一定不含有K+
B . 鉴别NaCl和KI溶液可用硝酸酸化的硝酸银溶液
C . 容量瓶不能用作溶解物质的容器
D . 粗盐的提纯实验中,滤液在蒸发皿中加热蒸发结晶
已知:H2(g)+F2(g)=2HF(g) ΔH=-270 kJ·mol-1 , 下列说法正确的是:( )
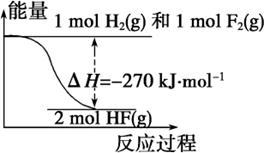
A . 氟化氢气体分解生成氢气和氟气的反应是放热反应
B . 1 mol H2与1 mol F2反应生成2 mol液态HF放出的热量小于270 kJ
C . 在相同条件下,1 mol H2与1 mol F2的能量总和小于2 mol HF气体的能量
D . 该反应中的能量变化可用如图来表示
根据右图所示能量循环图,下列说法正确的是( )
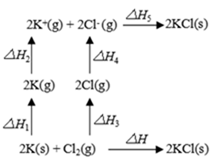
A . △H1>0;△H2<0
B . △H3>0;△H4<0
C . △H5>0;△H<0
D . △H=△H1+△H2+△H3+△H4-△H5
在密闭容器中加入镍粉后再充入一定量的CO气体,一定条件下,发生反应:Ni(s)+4CO(g)  Ni(CO)4(g),已知该反应的平衡常数与温度的关系如下表,下列说法正确的是( )
Ni(CO)4(g),已知该反应的平衡常数与温度的关系如下表,下列说法正确的是( )
 Ni(CO)4(g),已知该反应的平衡常数与温度的关系如下表,下列说法正确的是( )
Ni(CO)4(g),已知该反应的平衡常数与温度的关系如下表,下列说法正确的是( ) | 温度/℃ | 20 | 100 | 230 |
| K | 1×105 | 1 | 2×10-5 |
A . 该反应正反应为放热反应
B . 在100℃时,测得某时刻Ni(CO)4、CO的浓度均为1mol·L-1 , 则此时v正>v逆
C . 20℃时反应Ni(CO)4(g)  Ni(s)+4CO(g)的平衡常数约为10-5
D . 恒温恒压下,向容器中再充入少量CO,达到平衡时,CO的转化率将增大
Ni(s)+4CO(g)的平衡常数约为10-5
D . 恒温恒压下,向容器中再充入少量CO,达到平衡时,CO的转化率将增大
 Ni(s)+4CO(g)的平衡常数约为10-5
D . 恒温恒压下,向容器中再充入少量CO,达到平衡时,CO的转化率将增大
Ni(s)+4CO(g)的平衡常数约为10-5
D . 恒温恒压下,向容器中再充入少量CO,达到平衡时,CO的转化率将增大
已知: 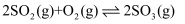 ∆H= mkJ·mol·L-1 , 不同条件下反应过程能量变化如图所示。下列说法正确的是( )
∆H= mkJ·mol·L-1 , 不同条件下反应过程能量变化如图所示。下列说法正确的是( )
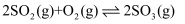 ∆H= mkJ·mol·L-1 , 不同条件下反应过程能量变化如图所示。下列说法正确的是( )
∆H= mkJ·mol·L-1 , 不同条件下反应过程能量变化如图所示。下列说法正确的是( ) 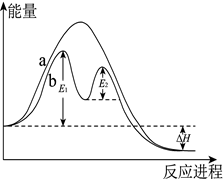
A . m>0
B . 过程a使用了催化剂
C . 过程b发生的两步反应均为吸热反应
D . 使用催化剂后,SO2的平衡转化率保持不变
已知:① 
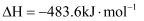

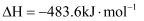
② 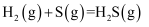
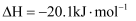 .下列判断一定正确的是( )
.下列判断一定正确的是( )
A . 1mol氢气完全燃烧生成  吸收241.8kJ热量
B . 水蒸气和硫化氢的能量相差221.7kJ
C . 由①②知,水的热稳定性大于硫化氢
D . 反应②中改用固态硫,1 mol
吸收241.8kJ热量
B . 水蒸气和硫化氢的能量相差221.7kJ
C . 由①②知,水的热稳定性大于硫化氢
D . 反应②中改用固态硫,1 mol  完全反应放热将大于20.1 kJ
完全反应放热将大于20.1 kJ
 吸收241.8kJ热量
B . 水蒸气和硫化氢的能量相差221.7kJ
C . 由①②知,水的热稳定性大于硫化氢
D . 反应②中改用固态硫,1 mol
吸收241.8kJ热量
B . 水蒸气和硫化氢的能量相差221.7kJ
C . 由①②知,水的热稳定性大于硫化氢
D . 反应②中改用固态硫,1 mol  完全反应放热将大于20.1 kJ
完全反应放热将大于20.1 kJ
下列反应的能量变化与图示一致的是( )
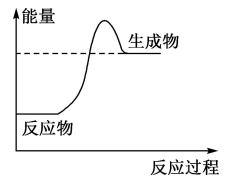
A . 铝热反应
B . 蜡烛燃烧
C . 中和反应
D . 高温煅烧石灰石
下列关于化学反应中能量变化的说法正确的是( )
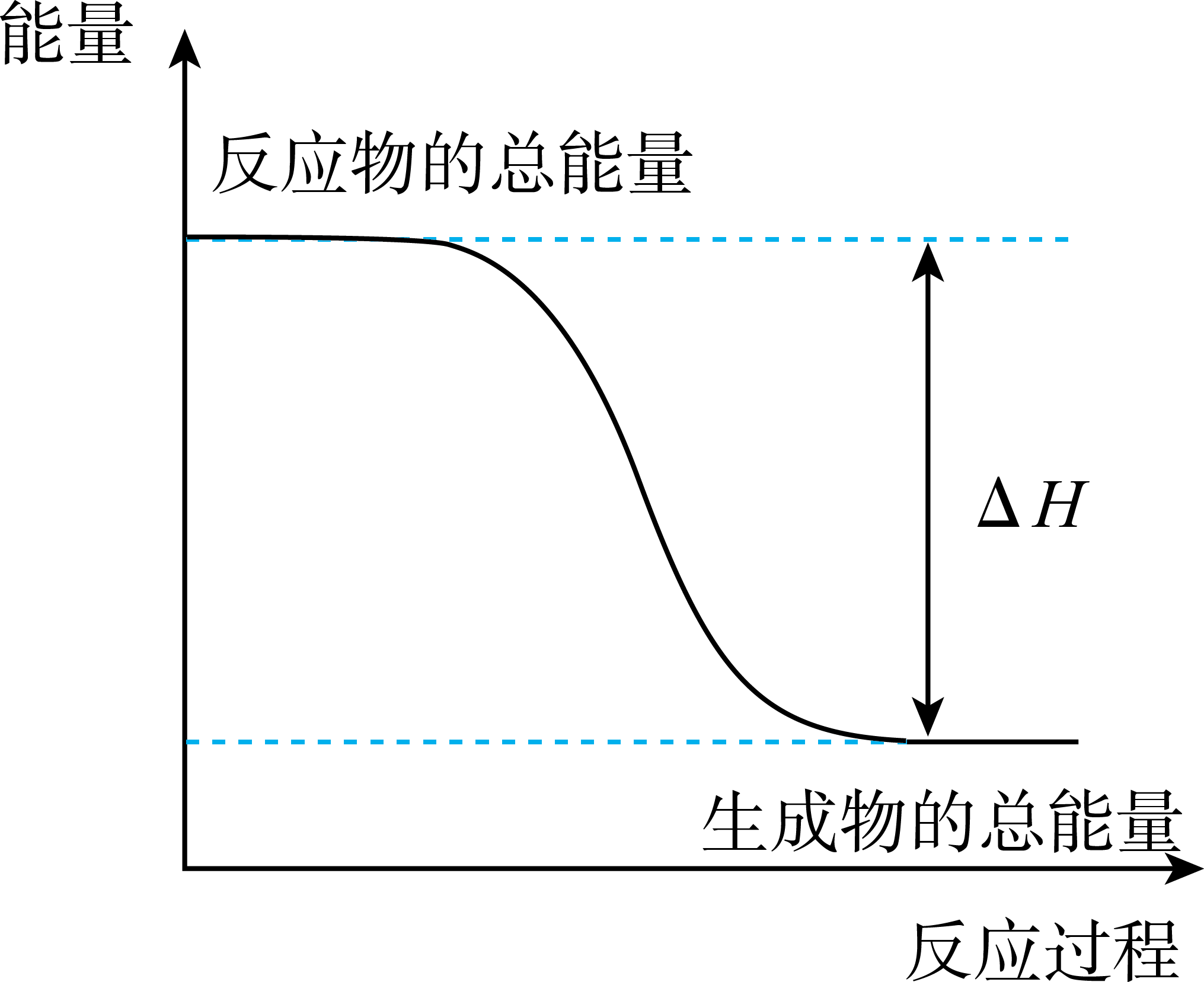
A . 断开化学键会释放能量
B . 化学反应过程中一定伴有能量变化
C . 常温下进行的一定是放热反应
D . 如图表示该反应为吸热反应
人们通过化学方法可以开辟新能源和提高能源的利用率,根据情景回答下列问题:
-
(1) 工业合成氨反应
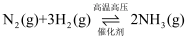 是放热的可逆反应。已知1mol高温高压N2(g)完全反应生成
是放热的可逆反应。已知1mol高温高压N2(g)完全反应生成 (g)可放出92kJ热量。如果将0.5mol
(g)可放出92kJ热量。如果将0.5mol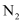 (g)和足量
(g)和足量 (g)混合,使其充分反应,放出的热量(填“大于”“小于”或“等于”)46kJ。
(g)混合,使其充分反应,放出的热量(填“大于”“小于”或“等于”)46kJ。
-
(2) 在容积为5L的密闭容器内模拟工业合成氨,反应经过5min后,生成10mol

①用
 表示的化学反应速率为
表示的化学反应速率为
②一定条件下,能说明该反应进行到最大限度的是。
a.
 的转化率达到最大值
的转化率达到最大值b.
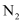 、
、 和
和 的分子数之比为
的分子数之比为
c.体系内气体的密度保持不变
d.体系内物质的平均相对分子质量保持不变
-
(3) 某实验小组进行如图甲所示实验。请判断b中的温度(填“升高”或“降低”)。反应过程(填“a”或“b”)的能量变化可用图乙表示。
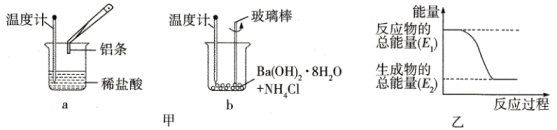
-
(4) 用
 和
和 组合形成的质子交换膜燃料电池的结构如图:
组合形成的质子交换膜燃料电池的结构如图: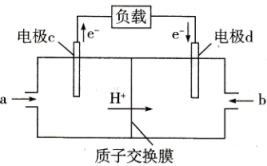
①电极c是(填“正极”或“负极”),电极d的电极反应式为。
②若线路中转移1mol电子,则该燃料电池理论上消耗的
 在标准状况下的体积为L。
在标准状况下的体积为L。
最近更新
- 设是由满足下列性质的函数构成的集合:在定义域内存在, 使得成立.已知下列函数:①;②;③;④,其中属于集合的函数是
- 25.当代环境问题主要是由人类污染造成的如巨大的人口压力、自然资源的不合理利用、片面追求经济增长速度等都是产生环境问题的
- (世界经理人数据讯)根据英国风险评估公司Maplecroft公布的自然灾害风险指数排名。该排名基于1980年至2010年
- 阅读下面的文字,完成下列各题。 聚落考古在文明起源研究中具有标志性、概括性意义,在文明起源研究中有着无法替代的重要意义。
- 如图,一理想变压器原线圈接入一交流电源,副线圈电路中R1、R2、R3和R4均为固定电阻,开关S是闭合的。 和 为
- 小明和小刚做游戏一个不透明的布袋里装有4个大小、质地均相同的乒乓球,球上分别标有数字1,2,3,4,随机从布袋中摸出一个
- 下列实验现象的描述中,不正确的是 () A.细铁丝在氧气中燃烧,火星四射,生成黑色固体B.将氢氧
- 你观察过养在鱼缸中的鱼吗?它的口和鳃盖后缘,不断地相互交替张开和关闭。这是鱼在进行哪种生理活动 ( )
- 分式中的值都扩大5倍,则分式的值 ( ) A.扩大5倍
- 有人认为,中国古代君主专制理论由先秦法家奠定,经汉朝儒生发展而成。这两个阶段的代表人物分别是 ( )
- 化学实验中常用到木条,下列实验中木条的使用不能达到目的是() A.用带火星的木条检验氧气 B.用燃着的木条点燃酒精灯 C
- (本题满分13分) 在△中,已知·=9,sin=cossin,面积S=6. (Ⅰ)求△的三边的长; (Ⅱ)设是△(含边界
- 如图所示,某人在D处测得山顶C的仰角为30°,向前走200米来到山脚A处,测得山坡AC的坡度i=1∶0.5,则山的高度为
- (二)实用类文本阅读(12分) 阅读下面的文字,完成4~6题。 严耕望:中国史学界的朴实楷模 余英时 1973—1
- “谁人不知张少帅,千古功臣一代骄”,与张少帅有关的历史事件是 A、南昌起义 B、台儿庄战役
- (2008·全国Ⅱ,29)“借用别人的智慧来做事,因为你的智慧是有限的。”这句话所强调的是 ①做事要充分发挥主观能动性,
- 有时候两只狗会为了一块骨头而相互打斗,这时候它们之间的关系是:( )A. 合作 B. 捕食 C.
- Failure is never a pleasure, but it can have a ef
- 噬菌体侵染细菌后可以使细菌死亡,HIV感染T细胞后可以造成T细胞大量死亡,那么噬菌体和HIV利用细菌和T细胞中的物质主要
- 汽油机工作时,在 冲程,将内能转化为机械能。



