4.1 物质在溶解过程中有能量变化吗? 知识点题库
-
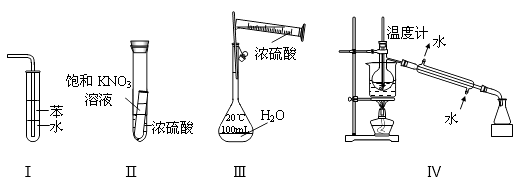
(1) 学校燃烧煤煮饭,
-
(2) 给手机的电池充电,
-
(3) 用畜电池点亮灯泡,
-
(4) 电解水得到O2和H2.
 2H2↑+O2↑
B . 高温使水分解制气:2H2O
2H2↑+O2↑
B . 高温使水分解制气:2H2O  2H2↑+O2↑
C . 太阳能催化分解水制气:2H2O
2H2↑+O2↑
C . 太阳能催化分解水制气:2H2O  2H2↑+O2↑
D . 天然气制气:CH4+H2O
2H2↑+O2↑
D . 天然气制气:CH4+H2O  CO+3H2
CO+3H2
①H2(g)+  O2(g)=H2O(l) ΔH=-285.8 kJ/mol
O2(g)=H2O(l) ΔH=-285.8 kJ/mol
②H2(g)+  O2(g)=H2O(g) ΔH=-241.8 kJ/mol
O2(g)=H2O(g) ΔH=-241.8 kJ/mol
③C(s)+  O2(g)=CO(g) ΔH=-110.5 kJ/mol
O2(g)=CO(g) ΔH=-110.5 kJ/mol
④C(s)+O2(g)=CO2(g) ΔH=-393.5 kJ/mol
回答下列问题:
-
(1) 上述反应中属于放热反应的是。
-
(2) H2的燃烧热为,C的燃烧热为。
-
(3) 燃烧10 g H2生成液态水,放出的热量为。
-
(4) CO的燃烧热为,其热化学方程式为。
-
(1) 除去NaCl溶液中的Br2(性质与碘相似),方法是。
-
(2) 除去澄清石灰水中悬浮的CaCO3 , 用。
-
(3) 除去自来水中难挥发的成分得到纯净水,方法是。
-
(4) 汽油和氯化钠溶液,采用。
-
(5) 从海水中获取食盐,采用。
 +2H+=CO2↑+H2O
+2H+=CO2↑+H2O
-
(1) 在微生物作用的条件下,
 经过两步反应被氧化成
经过两步反应被氧化成  。两步反应的能量变化示意图如下:
。两步反应的能量变化示意图如下: 
①第一步反应是(填“放热”或“吸热”)反应,判断依据是。
②1mol
 (aq)全部氧化成
(aq)全部氧化成  (aq)的热化学方程式是。
(aq)的热化学方程式是。 -
(2) 白磷、红磷是磷的两种同素异形体,在空气中燃烧得到磷的氧化物,空气不足时生成P4O6 , 空气充足时生成P4O10。
①已知298K时白磷、红磷完全燃烧的热化学方程式分别为:
P4(s,白磷)+5O2(g)=P4O10(s) ΔH1=-2983.2kJ·mol-1
P(s,红磷)+
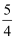 O2(g)=
O2(g)= 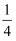 P4O10(s) ΔH2=-738.5kJ·mol-1
P4O10(s) ΔH2=-738.5kJ·mol-1则该温度下白磷转化为红磷的热化学方程式为。相同状况下,能量较低的是(填“红磷”或“白磷”),白磷的稳定性比红磷(填“高”或“低”)。
②已知298K时白磷不完全燃烧的热化学方程式为P4(s,白磷)+3O2(g)=P4O6(s) ΔH=-1638kJ·mol-1.在某密闭容器中加入12.4g白磷和8.96L氧气(标准状况下),控制条件使之恰好完全反应。则所得到的P4O10和P4O6的物质的量之比为,反应过程中放出的热量为。
-
(3) 已知H2(g)+Br2(l)=2HBr(g) ΔH=-72kJ·mol-1 , 蒸发1molBr2(l)需要吸收的能量为30kJ,其他相关数据如下表:
物质
H2(g)
Br2(g)
HBr(g)
1mol分子中的化学键断裂时需要吸收的能量/kJ
436
200
a
则表中a=。
-
(1) 已知:I.H2O(g) = H2(g) +
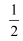 O2(g) ΔH = +241.8kJ/mol
O2(g) ΔH = +241.8kJ/molII.C(s) +
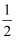 O2(g) = CO(g) ΔH = -110.5kJ/mol
O2(g) = CO(g) ΔH = -110.5kJ/molIII.C(s) + O2(g) = CO2(g) ΔH = -393.5kJ/mol
①上述反应中,属于吸热反应的是(填序号)。
②表示C的燃烧热的热化学方程式为(填序号)。
③写出CO燃烧的热化学方程式。
-
(2) 在密闭容器中,通入a mol N2和b mol H2 , 在一定条件下反应达到平衡时,容器中剩余c mol N2。
①达到平衡时,生成NH3的物质的量为,H2的转化率为。
②若把容器的容积缩小一半,则正反应速率(填“增大”“减小”或“不变”,下同),逆反应速率,N2的转化率。
ⅰ)太阳光催化分解水: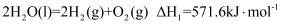
ⅱ)焦炭与水反应: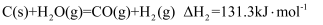
ⅲ)甲烷与水反应:
-
(1) 反应ⅰ中主要的能量转化为;你认为通过此途径进行H2工业化生产的最突出优点是。
-
(2) 相同温度压强下,若分别以ⅰ、ⅱ反应生成1mol H2 , 反应ⅱ比ⅰ要少吸收热量;你认为ⅱ反应需要吸热较小的原因可能是。
-
(3) ①写出反应ⅲ的化学平衡常数的表达式:
 ;
;②一定温度下,ⅲ反应中使用催化剂后,下列物理量能保持不变的有。
a.焓变
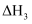 b.反应活化能Ea c.活化分子百分比 d.平衡常数K3
b.反应活化能Ea c.活化分子百分比 d.平衡常数K3 -
(4) ①利用上述热化学方程式,推测反应
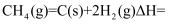 ;
;②以
 为燃料、KOH溶液为电解液的燃料电池,负极的电极反应式为。
为燃料、KOH溶液为电解液的燃料电池,负极的电极反应式为。
- 洋务思潮、维新思潮和共和思潮的兴衰反映了近代前期历史发展的主流。下列关于中国近代前期历史主流的表述,最为确切的是 A.推
- 在Cu2S+2Cu2O=6Cu+SO2↑反应中,说法正确的是 A.Cu2S在反应中既是氧化剂,又是还原剂 B.C
- 下列各种行为属于我国公民行使监督权的是①对政府工作提出批评与建议 ②依法在公共道路上游行、示威③依法对村长提出
- 已知向量则的最大值为 .
- 下列对实验的相关叙述,不正确的是( ) A.内质网是细胞中膜面积最大的细胞器,但在普通光学显微镜下不能看到内质网、
- Research has shown that music has an important effect on one
- 三、文学类文本阅读(25分) 11.阅读下面的文字,完成(1)~(4)题 两个朋友
- 在一个双链DNA分子中,脱氧核苷酸数为a,腺嘌呤碱基数为b,则下列有关数量关系式错误的是 A.鸟嘌呤的数量为a-b
- 某及其瓶里盛有N2和O2的混合气体(体积比4:1).小贝同学要用燃烧法除去O2而得到较纯净的N2,你认为她采用的试剂最好
- 固醇类物质中不包括 (
- 2003年美国高盛公司将巴西、俄罗斯、印度和中国4国的英文首字母连缀起来,创造了一个响亮的名称BRIC(与砖的英文“Br
- 椭圆过(3,0)点,离心率e=,求椭圆的标准方程.
- 为防治农田鼠害,研究人员选择若干大小相似、开放的大豆田,在边界上每隔一定距离设置适宜高度的模拟树桩,为肉食性猛禽提供栖息
- 下列化合物的分子中所有原子一定共面的是:( ) A.CH2Cl2 B.CH2=CHCl
- 作文(50分)阅读下面的材料,按要求作文。社会是一所学校,生活是我们的良师。在受挫折时我们学会了坚强;在不利的环境中,我
- 全国性的抗日战争爆发于 A.九一八事变
- 根据元素周期表,填写下列空白: (1)最活泼的非金属元素位于周期表中第 周期第 族、第 纵行
- 某化学兴趣小组的学生,发现金属R不在初中学到的金属活动性顺序表中,该小组为了了解R与常见金属铝、铜的金属活动性顺序,进行
- 若某动物细胞内有两对同源染色体,分别用A和a,B和b表示。下列各组精子中由同一个精原细胞经减数分裂形成的是 A.AB、a
- 秦统一六国的最主要的主观因素是 A.秦国的商鞅变法比较彻底,在七国中实力最强B.社会经济的迅速发展,为秦统一提供了物质基



