4.1 物质在溶解过程中有能量变化吗? 知识点题库
-
(1) 学校燃烧煤煮饭 ,
-
(2) 用畜电池点亮灯泡 。
-
(1) 将水蒸气通过红热的炭即可产生水煤气。反应为C(s)+H2O(g)
 CO(g)+H2(g) ΔH =+131.3 kJ·mol-1。
CO(g)+H2(g) ΔH =+131.3 kJ·mol-1。 ①该反应在常温下(填“能”或“不能”)自发进行。
②一定温度下,在一个容积可变的密闭容器中,发生上述反应,下列能判断该反应达到化学平衡状态的是(填字母,下同)。
a.容器中的压强不变
b.1 mol H—H键断裂的同时,断裂2 mol H—O键
c.c(CO)=c(H2)
d.密闭容器的容积不再改变
-
(2) 将不同量的CO(g)和H2O(g)分别通入体积为2 L的恒容密闭容器中,进行反应CO(g)+H2O(g)
 CO2(g)+H2(g),得到如下三组数据:
CO2(g)+H2(g),得到如下三组数据: 实验组
温度/℃
起始量/mol
平衡量/mol
达到平衡所需时间/min
H2O
CO
H2
CO
1
650
2
4
1.6
2.4
6
2
900
1
2
0.4
1.6
3
3
900
a
b
c
d
t
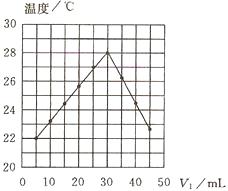
①实验1中从反应开始至平衡以CO2表示的平均反应速率为v(CO2)=(取小数点后两位,下同)。
②该反应的正反应为(填“吸”或“放”)热反应,实验2条件下平衡常数K=。
-
(3) 目前工业上有一种方法是用CO2来生产甲醇。一定条件下发生反应:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g),如图表示该反应进行过程中能量(单位为kJ·mol-1)的变化。在体积为1 L的恒容密闭容器中,充入1 mol CO2和3 mol H2 , 达到平衡后下列措施中能使c(CH3OH)增大的是。
CH3OH(g)+H2O(g),如图表示该反应进行过程中能量(单位为kJ·mol-1)的变化。在体积为1 L的恒容密闭容器中,充入1 mol CO2和3 mol H2 , 达到平衡后下列措施中能使c(CH3OH)增大的是。 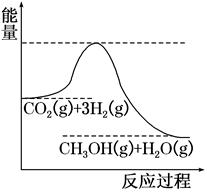
a.升高温度
b.充入He(g),使体系压强增大
c.将H2O(g)从体系中分离出来
d.再充入1 mol CO2和3 mol H2
① 2NO(g)  N2O2(g) (快) △H1< 0 平衡常数 K1
N2O2(g) (快) △H1< 0 平衡常数 K1
② N2O2(g)+O2  2NO2(g) (慢) △H2< 0 平衡常数 K2
2NO2(g) (慢) △H2< 0 平衡常数 K2
下列说法正确的是( )
 2NO2(g) △H= △H1-△H2
B . 2NO(g)+O2
2NO2(g) △H= △H1-△H2
B . 2NO(g)+O2  2NO2(g) 的平衡常数K=K1×K2
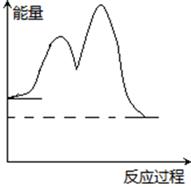
C . 该转化反应过程中能量变化可如图表示
D . 总速率的大小由反应①决定
2NO2(g) 的平衡常数K=K1×K2
C . 该转化反应过程中能量变化可如图表示
D . 总速率的大小由反应①决定
-
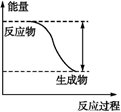
(1) 该反应为(填“吸热”或“放热”)反应。
-
(2) 若要使该反应的反应速率增大,下列措施可行的是_________(填字母)。A . 改铁片为铁粉 B . 改稀硫酸为98%的浓硫酸 C . 升高温度 D . 使用催化剂
-
(3) 若将上述反应设计成原电池,铜为原电池某一极材料,则铜为:(填“正”或“负”)极,该极上发生的电极反应为:,外电路中电子移动方向为:。
-
(1) 已知CH3OH(g)+
 O2(g)
O2(g)  CO2(g)+2H2(g)的能量变化如图所示:
CO2(g)+2H2(g)的能量变化如图所示: 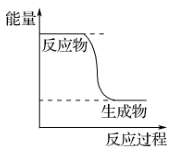
下列说法正确的是(填字母标号)。
a.CH3OH转变成H2的过程是一个吸收能量的过程
b.H2的生成速率与CH3OH的消耗速率之比为1:2
c.化学变化不仅有新物质生成,同时也一定有能量变化
d.1molH-O键断裂的同时2molC=O键断裂,则反应达最大限度
-
(2) 某温度下,将5molCH3OH和2molO2充入容积为2L的密闭容器中,经过4min反应达到平衡,测得c(O2)=0.2mol/L,4min内平均反应速率v(H2)=,则CH3OH的转化率为。
-
(3) CH3OH燃料电池是目前开发最成功的燃料电池之一,这种燃料电池由甲醇、空气(氧气)、KOH(电解质溶液)构成。已知其负极反应式为CH3OH+8OH--6e-=
 +6H2O。
+6H2O。 则下列说法正确的是(填序号)。
①电池放电时通入空气的电极为负极
②电池放电时,电解质溶液的碱性逐渐减弱
③电池放电时每消耗6.4gCH3OH转移1.2mol电子
①H2(g)+  O2(g)═H2O(l) △H=﹣285.8kJ•mol﹣1
O2(g)═H2O(l) △H=﹣285.8kJ•mol﹣1
②H2(g)+  O2(g)═H2O(g) △H=﹣241.8kJ•mol﹣1
O2(g)═H2O(g) △H=﹣241.8kJ•mol﹣1
③C(s)+  O2(g)═CO(g) △H=﹣110.5kJ•mol﹣1
O2(g)═CO(g) △H=﹣110.5kJ•mol﹣1
④CO2(g)═C(s)+O2(g) △H=+393.5kJ•mol﹣1
回答下列各问题:
-
(1) 上述反应中属于放热反应的是。
-
(2) H2的燃烧热为;C的燃烧热为。
-
(3) 燃烧10gH2生成液态水,放出的热量为。
-
(4) CO燃烧热的热化学方程式为。
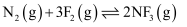
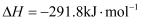 ,则
,则  的
的 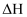 为( )
为( )
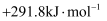 B .
B . 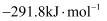 C .
C . 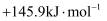 D .
D . 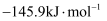
①CO2(g)+3H2(g)=CH3OH(g)+H2O(g) △H1=-49.0 kJ/mol
②CO2(g)+H2(g)=CO(g)+H2O(g) △H2=+41.2 kJ/mol
下列说法正确的是( )
- 补写诗歌,使语意完整。你走了,没有留下地址,只留下一串笑容在夕阳里; 你走了,没有和谁说起,
- 指出句子中的错误并改正。 这个精致的灯笼将作为今天得分最高的嘉宾的礼品送给他。
- 朱元璋为加强对军队的控制,设五军都督府和兵部相互制约。对五军都督府职权表述正确的是() A.五军都督府掌京师军权,兵
- 若在能溶解氧化铝的溶液中,分别加入下列各组离子,可能大 量共存的是( ) A. NH4+、NO3-、 CO32- 、
- 实验结束后,如图所示仪器的放置方法正确的是( )
- 如图所示电路中,电源电动势为E,内电阻不能忽略。闭合S后,调整R的阻值,使电压表的示数增大。在这一过程中( )A
- 下列不属于陆生动物的特征的是()A.一般有防止水分散失的结构 B.用体壁呼吸C.绝大多数用气管或肺呼吸
- 某人酗酒后,说话含糊不清,主要是因为酒精毒害了他的( ) A.脑干 B.大脑 C.
- You ________ smoke here. It’s bad for ourhealth. A. must B
- 下列现象中,体现政府组织社会主义文化建设职能的是( )A.欧盟轮值国主席法国总统萨科齐执意要见达赖,中国政府因此推迟中
- 下列说法正确的是( ) A.第二周期元素的第一电离能随原子序数递增依次增大 B.CO2、SO2都是直线形的非极性分子
- 如图中,①、②、③、④表示某区域地形类型中的山脊或山谷,点a、b、c对应的海拔分别为900米、600米、300米。读图,
- 某蛋白质由m条肽链、n个氨基酸组成。该蛋白质至少有氧原子的个数是 A.n+m B.n-2m
- 过抛物线y=ax2(a>0)的焦点F作一直线交抛物线于P、Q两点,若PF与QF的长分别是p、q,则+等于
- 用适当的化学符号填空 (1)绿色植物的光合作用吸收的气体是 ,释放的气体是 。 (2)
- 根据汉语意思完成句子,每空一词。 1.我觉得汤姆和保罗没有任何相同之处。 I don't think Tom and P
- 增城属于县级行政单位,结合增城社会经济具体情况,增城人大代表的选举,应该采用( ) A 直接选举 B
- 右图为R元素的原子结构示意图。下列说法错误的是 A.x为11 B.R属于金属元素 C.决定R元素种类的是核内
- 阅读下面的文言文,完成后面的题(其中选择题每小题2分,共15分) 吾尝终日而思矣,不如须臾之所学也。吾尝跂而望矣,不如登
- (08年黄冈中学一模文) (12分)在△ABC中,角A、B、C的对边分别是a、b、c,且A为锐角,. (Ⅰ)求f



