第2节 铝 金属材料 知识点题库
-
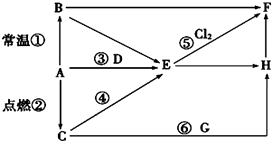
(1) 推断A为;B为;E为;H为(填化学式).
-
(2) 反应⑤的化学方程式,反应⑥的化学方程式.
请回答:
-
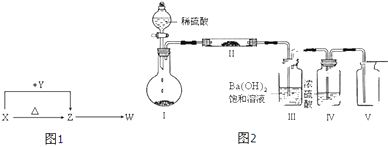
(1) W的电子式是.
-
(2) X与Y在溶液中反应的离子方程式是.
-
(3) X含有的四种元素之间(二种、三种或四种)可组成多种化合物,选用其中某些化合物,利用如图2装置(夹持固定装置已略去)进行实验,装置Ⅲ中产生白色沉淀,装置Ⅴ中可收集到一种无色气体.
①装置Ⅰ中反应的化学方程式是,
装置Ⅱ中物质的化学式是.
②用X含有的四种元素中的两种组成的某化合物,在催化剂存在下制备并收集纯净干燥的装置Ⅴ中气体,该化合物的化学式是,所需仪器装置是(从图中选择必要装置,填写编号).
-
(4) 向Z溶液中通入氯气,可制得某种生产和生活中常用的漂白、消毒的物质,同时有X生成,该反应的化学方程式是.
-
(1) 写出铁元素在周期表中的位置。
-
(2) 写出在空气中Fe(OH)2转化为Fe(OH)3的化学方程式。
-
(3) 绿矾(FeSO4·7H2O)是补血剂的原料,易变质。
①由FeSO4溶液制得FeSO4·7H2O过程中的操作有、过滤、洗涤、干燥。
②检验绿矾是否变质的试剂是。
-
(4) 利用绿矾制备还原铁粉的工业流程如下:
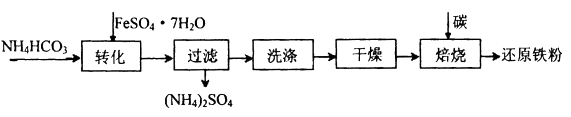
①干燥过程主要是为了脱去游离水和结晶水,过程中会有少量FeCO3·nH2O在空气中被氧化为FeOOH,该反应的化学方程式为。
②取干燥后的FeCO3样品12.49g,焙烧,最终得到还原铁粉6.16g,计算样品中杂质FeOOH的质量。
-
(5) 以羰基化合物为载体运用化学平衡移动原理分离、提纯某纳米级活性铁粉(含有一些不反应的杂质),反应装置如下图。
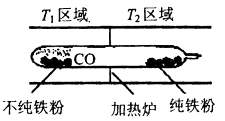
Fe(s)+5CO(g)
 Fe(CO)5(g) △H<0,T1 T2(填“>”、“<”或“=”)。
Fe(CO)5(g) △H<0,T1 T2(填“>”、“<”或“=”)。
回答下列问题:
-
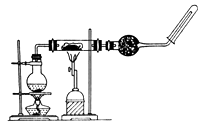
(1) 在圆底烧瓶内加入碎瓷片,其作用是_____(填字母代号)A . 加快化学反应速率 B . 防止溶液暴沸
-
(2) 写出铁与高温下水蒸气反应的化学方程式;
-
(3) 干燥管中盛装的物质是;
-
(4) 点燃试管收集的气体前,则必须对该气体进行;
-
(5) 实验时将铁粉与石棉绒混合以及在反应管的两端均放入少量石棉绒,其原因可能是(填序号)___________A . 石棉绒的作用是催化剂 B . 石棉绒受热均匀的作用是使铁粉 C . 石棉绒的作用是作铁粉的载体以及防止铁粉被吹入导管而引起堵塞
-
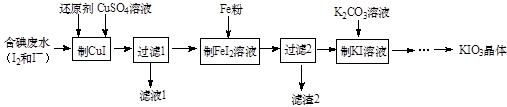
(1) 检验“含碘废水”中含有的单质I2 , 常用的试剂是。
-
(2) 进行“过滤1”时,需同时对CuI沉淀进行洗涤。在洗涤过滤滤液中可通过滴加盐溶液来检验其是否已洗涤干净。
-
(3) “滤渣2”的成分为(填化学式)。
-
(4) “制KI”时,发生反应的化学方程式为。
-
(5) 江苏食用加碘盐新标准是每千克食盐中碘元素含量为25毫克(波动范围为18~33mg/kg)。测定食盐试样中碘元素含量的步骤如下:称取4.000g市售食盐加入锥形瓶中,依次加入适量的水、稍过量KI及稀硫酸;充分反应后,再加入12.00mL6.000×10-4mol·L-1Na2S2O3溶液,与生成的碘恰好完全反应。有关反应原理为:
KIO3+5KI+3H2SO4=3K2SO4+3I2+3H2O; I2+2S2O
 =2I- +S4O
=2I- +S4O 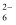 。
。①计算该食盐试样中碘元素的含量(单位mg/kg,写出计算过程)。
②该食盐试样是否符合江苏食用加碘盐新标准,并说明判断依据。
| 选项 | 实验 | 现象 | 结论 |
| A | 向添有KIO3的食盐中加入淀粉溶液、稀盐酸及KI | 溶液变蓝色 | 氧化性:IO3- >I2 |
| B | 将SO2气体通入到Ba(NO3)2溶液中 | 生成白色沉淀 | 此沉淀是BaSO3 |
| C | 将FeCl2样品溶于盐酸后,滴加KSCN溶液 | 溶液变成红色 | 原FeCl2样品已变质 |
| D | 燃烧的钠粒放入CO2中 | 燃烧且有白色和黑色颗粒产生 | 黑色颗粒是炭,白色颗粒可能是Na2CO3 |
-
(1) Ⅰ.引发铝热反应的实验操作是
-
(2) 做铝热反应时,内层纸漏斗底部剪一小孔用水润湿的目的是
-
(3) 反应的化学方程式为
-
(4) Ⅱ.已知:Al、Fe的熔、沸点数据如下:
物质
Al
Fe
熔点(℃)
660
1 535
沸点(℃)
2 467
2 750
某同学猜测,铝热反应所得到的熔落物是铁铝合金。理由:该反应放热能使铁熔化,而铝的熔点比铁低,所以铁和铝能形成合金。你认为他的解释是否合理?(填“合理”或“不合理”)。设计一个简单的实验方案,证明上述所得的熔落物中含有金属铝:
|
实验步骤 |
实验现象 |
|
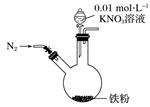
①打开弹簧夹,缓慢通入N2 |
|
|
②加入0.01 mol·L-1的酸性KNO3溶液100 mL |
铁粉部分溶解,溶液呈浅绿色;铁粉不再溶解后,剩余铁粉表面附着少量白色物质 |
|
③反应停止后,拔掉橡胶塞,将圆底烧瓶取下 |
烧瓶内气体的颜色没有发生变化 |
|
④将剩余固体过滤 |
表面的白色物质变为红褐色 |
-
(1) 通入N2并保持后续反应均在N2氛围中进行的实验目的是。
-
(2) 白色物质是(写化学式)。
-
(3) 为了探究滤液的成分,该同学进一步设计了下述实验:
实验步骤
实验现象
①取部分滤液于试管中,向其中加入KSCN溶液
溶液无变化
②将上述溶液分为两份,一份中滴入氯水,另一份中滴加稀硫酸
两份溶液均变为红色
③另取部分滤液于试管中,向其中加入浓NaOH溶液并加热,在试管口放置湿润的红色石蕊试纸
有气体生成,该气体使湿润的红色石蕊试纸变蓝
(ⅰ)根据以上实验现象,可以判断滤液中存在 (填离子符号)。
(ⅱ)步骤②中滴加稀硫酸后溶液会由浅绿色变成红色,请用离子方程式解释其原因:(写第一步反应)。
(ⅲ)步骤③中生成气体的离子方程式为。
|
编 号 |
温度 /℃ |
加入某盐 |
H2SO4 体积/ml |
H2O 体积 /ml |
铝粉 加入量/g |
铝粉 溶解量/g |
|
① |
20 |
不加 |
40 |
0 |
2.0050 |
0.0307 |
|
② |
80 |
不加 |
40 |
0 |
2.0050 |
0.1184 |
|
③ |
t1 |
不加 |
20 |
V1 |
2.0050 |
/ |
|
④ |
t2 |
5ml 0.01 mol·L-1 CuSO4溶液 |
20 |
V2 |
2.0050 |
/ |
-
(1) 实验①和②的目的是
为了获得铝粉溶解量,还需要测量的数据是。
-
(2) 实验①和③是为了研究硫酸的浓度对该反应的影响,则t1=℃.
-
(3) 实验③和④是为了研究加入CuSO4溶液对该反应的影响,则 V2=mL.
研究表明,在相同条件下加入少量CuSO4有利于Al的溶解。原因是。
-
(4) 纯铝与稀硫酸反应生成氢气的速率—时间图像如图所示:
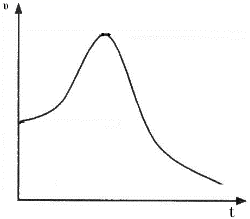
其原因为
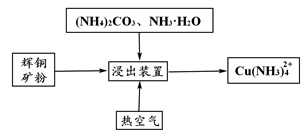
其反应机理如下:
① 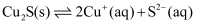 (快反应)
(快反应)
② 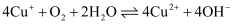 (慢反应)
(慢反应)
③ 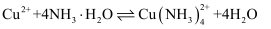 (快反应)
(快反应)
下列说法正确的是( )
 是还原产物
C . 在浸出装置中加入适量的(NH4)2S2O8 , 使平衡①、②正向移动,铜的浸出率增大
D . 提高铜的浸出率的关键因素是提高反应②的速率,原因是反应②的活化能比反应①、③的小
是还原产物
C . 在浸出装置中加入适量的(NH4)2S2O8 , 使平衡①、②正向移动,铜的浸出率增大
D . 提高铜的浸出率的关键因素是提高反应②的速率,原因是反应②的活化能比反应①、③的小
-
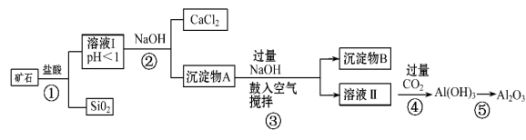
(1) 步骤①中加快反应速率的措施有(填一种)。
-
(2) 溶液Ⅰ中除了Ca2+外,还含有的金属阳离子有。
-
(3) 鼓入空气并充分搅拌的目的是。
-
(4) 工业上制取Al的反应方程式为。
-
(5) 试设计实验证明榴石矿中含有FeO(试剂任选,说明实验操作与现象)。
- 下列叙述中正确的是 A.含氧元素
- 电磁炉是利用高频电流在电磁炉内部线圈中产生磁场,磁化铁质锅底,使之形成无数个小涡流,加快锅底分子运动,锅底自身高速发热达
- 双曲线的离心率为 。
- “两个魔鬼胜过一个圣人”是一句英国格言,典型地说明了民主宪政的特点,政治就 是与魔鬼结盟,但立宪政治中与魔鬼结盟则是化敌
- Chinglish即“中式英语”,是指在使用英语时,因受汉语思维方式或文化的影响而生搬硬套、拼造出不符合英语表达习惯的、
- 下列词语中没有错别字的一项是() A羁旅 袅娜 蓦然回首 寓义深刻 B饯别 缄默 稼穑 以偏概全 C觊觎 筹画
- —Is this your jacket? —________. A.Yes, itis B.Yes,
- 下列关于生命活动变化关系的描述,不正确的是 A.细胞体积增大,与外界物质交换效率降低 B.细胞液浓度增大,植物细胞吸水能
- 农谚说:“有收无收在于水,收多收少在于肥”。这说明植物生长需要 ( )A.水和无机盐B.有机物C.维生素D.适
- 利用下图所示装置,当X、Y选用不同材料时,可将电解原理广泛应用于工业生产。下列说法中正确的是 ( ) A.氯碱
- When products made in factories _____, they are thrown away
- 纽芬兰岛等地的鳕鱼,因被过度捕捞而数量急剧下降。科学家发现,对鳕鱼的过度捕捞改变了鳕鱼的进化过程,导致了鳕鱼的早熟,使其
- 世界上现存最古老的石拱桥是: ( ) A. 苏州宝带桥B.北京玉带桥 C.赵州桥D.卢沟桥
- 下列关予溶液和胶体的叙述,正确的是
- After studying as an English major in college for four years
- (多选) 下列关于转基因生物与环境安全的叙述错误的是 A.重组的微生物在降解污染物的过程中可能产生二次污染 B.种
- 右图为用于基因工程的一个质粒示意图。用EcoRⅠ限制酶切割目的基因和该质粒,再用DNA连接酶连接形成重组质粒,然后导入大
- 阅读《红楼梦》中“宝玉挨打”的一段文字,回答问题。 “早听人一句话,也不至今日。别说老太太、太太心疼,就是我们看着,心里
- (本题满分8分)如图,AD是⊙O的弦,AB经过圆心O,交⊙O于点C.∠DAB=∠B=30°.(1)直线BD是否与⊙O相切
- 设,分别为具有公共焦点与的椭圆和双曲线的离心率,为两曲线的一个公共点,且满足,则的值为A.



