第2节 铝 金属材料 知识点题库
现有一块铝铁合金,欲测定其铝的质量分数,切下W g合金,溶于盐酸中,再加入过量NaOH溶液,滤出沉淀,将沉淀在空气中充分灼烧,最后得到W g红棕色粉末。则此合金中铝的质量分数约为( )
A . 20%
B . 30%
C . 70%
D . 80%
已知甲、乙、丙三种物质均含有同一种中学常见元素X,其转化关系如下:甲  乙
乙  丙,下列说法不正确的( )
丙,下列说法不正确的( )
 乙
乙  丙,下列说法不正确的( )
丙,下列说法不正确的( )
A . 若A为硝酸,X为金属元素,则甲与丙反应可生成乙
B . 若乙为NaHCO3 , 则丙一定是CO2
C . 若A为NaOH溶液,X为短周期的金属元素,则乙一定为白色沉淀
D . 若A为金属单质,乙的水溶液遇KSCN溶液变红,则甲可能为非金属单质
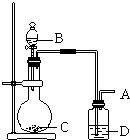
图为制取纯净干燥的气体A的装置图的一部分.生成A的速度可通过滴入液体B的速度控制.已知A是一种无色、无气味的气体,它不能使酸碱指示剂变色,也不能在空气中燃烧,但能使带火星的木条复燃.
-
(1) A是.
-
(2) 若C是一种淡黄色固体,则烧瓶中发生反应的化学方程式为.
-
(3) 若C是一种黑色粉末,则B物质是,C物质的作用是.
-
(4) 洗气瓶中的试剂是,其作用是.
(已知HCO3﹣+AlO2﹣+H2O═CO32﹣+Al(OH)3↓;将足量的KHCO3溶液不断滴入含等物质的量的KOH、Ba(OH)2、KAlO2的混合溶液中,生成沉淀的物质的量与滴入的KHCO3溶液体积的关系可表示为( )
A . 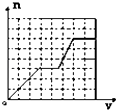 B .
B . 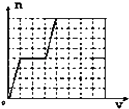 C .
C . 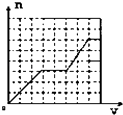 D .
D . 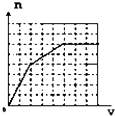
 B .
B .  C .
C .  D .
D . 
将5.1g镁铝合金,投入500mL 2.0mol•L﹣1盐酸中,金属完全溶解,再加入4.0mol•L﹣1的NaOH溶液,若要生成的沉淀最多,则加入NaOH溶液的体积是( )
A . 200mL
B . 425mL
C . 250mL
D . 560mL
将下列固体物质溶于水,再将其溶液加热、蒸发结晶、再灼烧,能得到化学组成与原固体物质相同的是( )
A . FeCl3
B . NaAlO2
C . NaHCO3
D . Na2SO3
A、B、C、D为四种可溶性的盐,它们的阳离子分别可能是Ba2+、Ag+、Na+、Cu2+中的某一种,阴离子分别可能是NO3﹣、SO42﹣、Cl﹣、CO32﹣的中的一种.
①若把四种盐分别溶解于盛有蒸馏水的四支试管中,只有C盐的溶液呈蓝色.
②若向①的四支试管中分别加入盐酸,B盐的溶液有沉淀生成,D盐的溶液有无色无味的气体逸出.
根据①②实验事实可推断它们的化学式为:
-
(1) A,C;
-
(2) 写出盐酸与D反应的离子反应方程式:;
-
(3) 写出C与Ba(OH)2溶液反应的离子方程式.
金属及其化合物转化关系是化学学习的重要内容之一。下列各组物质的转化关系中不能全部通过一步反应完成的是( )
A . Al→Al2O3→Al(OH)3→AlCl3
B . Fe→FeCl3→Fe(OH)3→Fe2O3
C . Mg→MgCl2→Mg(OH)2→MgSO4
D . Na→NaOH→Na2CO3→NaCl
下列离子方程式中,正确的是( )
A . 钠和冷水反应:Na+2H2O=Na++2OH-+H2↑
B . AlCl3溶液中加入足量的氨水:Al3++ 3OH-═Al(OH)3↓
C . 三氯化铁溶液中加入铁粉:Fe3++ Fe═ 2 Fe2+
D . FeCl2溶液跟Cl2反应:2Fe2++Cl2=2Fe3++2Cl-
在下图所示的物质转化关系中,A是常见的气态氢化物,B是能使带火星的木条复燃的无色无味气体,E的相对分子质量比D大17,G是一种紫红色金属单质。(部分反应中生成物没有全部列出,反应条件未列出)
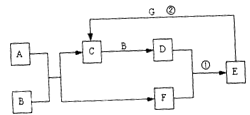
请回答下列问题:
-
(1) A、C的化学式分别为、。
-
(2) 反应①的化学方程式为。
-
(3) 反应②的离子方程式为。
-
(4) 向反应②后的溶液中通入少量的A,现象为。
将后者逐渐滴入(或通入)前者至过量,有沉淀产生且最终消失的是( )
A . 氯化铝、氨水
B . 氢硫酸、氧气
C . 硫酸铝、氢氧化钠
D . 氯化亚铁、氯气
由乙烯和其他无机原料合成环状酯E和高分子化合物H的示意图如图所示:
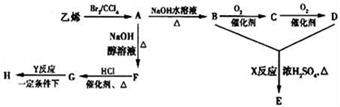
请回答下列问题:
-
(1) 写出以下物质的结构简式:B,G
-
(2) 写出以下反应的反应类型:X,Y.
-
(3) 写出以下反应的化学方程式:A→B:
-
(4) 若环状酯E与NaOH水溶液共热,则发生反应的化学方程式为.
下列说洪正确的是( )
A . 久置氯水会变成稀盐酸
B . 红热的铁丝在Cl2中剧烈燃烧,产生白烟
C . 钠在空气中变质,最终变成氢氧化钠
D . 钠在空气中燃烧得到白色固体Na2O
下列实验中,溶液颜色有明显变化的是( )
A . 少量明矾溶液加入到过量NaOH溶液中
B . 往FeCl3溶液中滴入KI溶液,再滴入淀粉溶液
C . 少量Na2O2固体加入到过量NaHCO3溶液中
D . 在酸性高锰酸钾溶液中滴入少量Fe2(SO4)3稀溶液
以不同类别物质间的转化为线索,认识钠及其化合物。
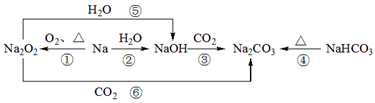
下列分析错误的是( )
A . 反应③表明CO2具有酸性氧化物的性质
B . 反应④说明NaHCO3的稳定性强于Na2CO3
C . 反应⑤、⑥可用于潜水艇中氧气的供给
D . Na放在空气中表面最终生成的是Na2CO3
A~E为中学化学常见纯净物,其中A可用于焙制糕点,B是生活中常用的一种调味品,也是重要的化工原料。D、E均为气体,F的水溶液是一种强酸。它们之间的转化关系如下。(部分反应物、生成物已略去)
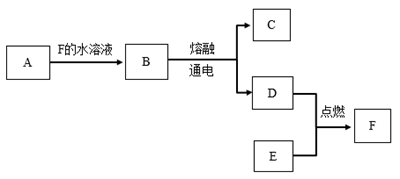
请回答下列问题:
-
(1) 写出下列物质的化学式:A,B,C。
-
(2) A→B的离子方程式是。
-
(3) D与E反应的化学方程式是,反应现象是。
三氯化铁在印刷、医药、颜料、污水处理以及有机合成催化剂方面有重要的应用。以硫铁矿(主要成分为FeS2,杂质不与盐酸反应)为原料制备三氯化铁晶体(FeCl3·6HO2)的工艺流程如图所示:
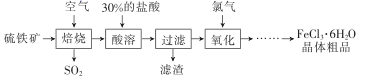
回答下列问题:
-
(1) “焙烧”过程中,理论上1molFeS2被氧化转移11mol电子,则该反应的氧化产物为。
-
(2) “酸溶”(填“能”或“不能”)用稀硫酸代替30%的盐酸,理由是。
-
(3) 现有试剂①稀盐酸②稀硫酸③稀硝酸④氯气⑤硫氰化钾溶液⑥高锰酸钾溶液⑦氢氧化钠溶液,为确认“酸溶”后的溶液中是否会含Fe2+ , 另取“焙烧”后的烧渣少许,用(从上述试剂中选择,填标号)溶解,将所得溶液滴入从上述试剂中选择,填标号)中,若,则说明“酸溶”后的溶液中含Fe2+。
-
(4) 从FeCl3溶液中得到FeCl3•6H2O的操作包括、冷却结晶、过滤,该过程需保持盐酸过量,结合必要的离子方程式说明原因:。
-
(5) 从FeCl3•6H2O中得到无水FeCl3的操作方法为。
-
(6) 若以a吨硫铁矿为原料,最终制得b吨FeCl3•6H2O,不计生产过程中的损失,则该硫铁矿FeS2的含量为(用含a、b的代数式表示)。
(NH4)2Fe(SO4)2•6H2O俗称“摩尔盐”,是一种重要的化学试剂。当隔绝空气加热至500℃时,摩尔盐可完全分解,某小组欲探究其分解产物,设计实验如下,请回答:
-
(1) 该小组认为分解产物可能有以下几种情况:A . Fe2O3、SO3、NH3、H2O B . FeO、SO3、NH3、H2O C . FeO、SO2、NH3、H2O D . Fe2O3、SO2、SO3、NH3、H2O
经认真分析,确定猜想___________不成立(填序号);
-
(2) 为进一步确认分解产物,该小组设计了如下实验装置探究:
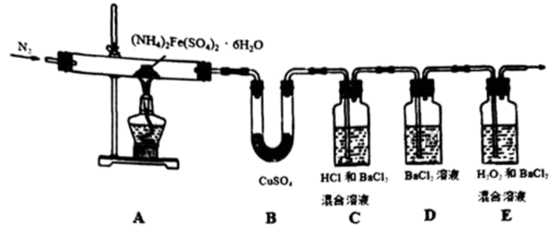 ①仪器B的名称为;
①仪器B的名称为;②加热前先通一段时间N2 , 加热至完全分解后再通入过量N2 , 实验过程中观察到装置D始终无明显现象,装置C和E均产生白色沉淀。
ⅰ.下列判断错误的是
A.C中的沉淀一定有BaSO4
B.C中的沉淀不可能含有BaSO3
C.加热至完全分解后再通入过量N2的目的是将分解产生的气体全部排到B、C装置中使其全部被吸收
D.D中无明显现象是因为SO2不能与BaCl2反应
ⅱ.写出E中所发生反应的化学方程式;
-
(3) 实验结束后,A中的固体变为红棕色,某同学猜测可能还有FeO,并设计实验验证:
第一步:该红色固体用溶解(填“盐酸”或“稀硫酸”);
第二步:为了检验是否存在Fe2+ , 向所得溶液中滴加试剂,观察是否褪色。
下图是以铝土矿(主要成分是  和少量
和少量  、
、  杂质)为原料制取铵明矾晶体
杂质)为原料制取铵明矾晶体  的一种工艺流程。
的一种工艺流程。
 和少量
和少量  、
、  杂质)为原料制取铵明矾晶体
杂质)为原料制取铵明矾晶体  的一种工艺流程。
的一种工艺流程。 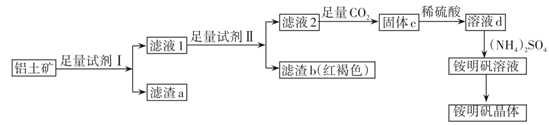
请回答:
-
(1) 试剂Ⅰ为,滤渣a可以“变废为宝”,写出它的一种用途。
-
(2) 证明铁元素已除尽的实验方法是。
-
(3) 滤液2中通入足量
 进行酸化得到固体c,则生成固体c的离子方程式为。
进行酸化得到固体c,则生成固体c的离子方程式为。
-
(4) 由溶液d制取铵明矾溶液的化学方程式为,从铵明矾溶液中获得铵明矾晶体的实验操作依次为蒸发浓缩、冷却结晶、、、干燥(填操作名称)。
某小组用下图所示装置(夹持装置省略)制备 , 并探究
, 并探究 与
与 溶液的反应。
溶液的反应。
 , 并探究
, 并探究 与
与 溶液的反应。
溶液的反应。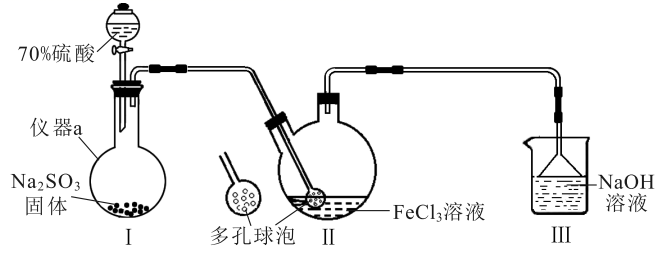
回答下列问题:
-
(1) 仪器
 的名称是,装置Ⅰ中反应的化学方程式为。
的名称是,装置Ⅰ中反应的化学方程式为。
-
(2) 多孔球泡的作用有、。
-
(3) 实验开始后,装置Ⅱ中溶液很快由黄色变为红棕色;停止通入
 , 放置一段时间后,Ⅱ中溶液又逐渐变为浅绿色。有同学认为此时该溶液中含有
, 放置一段时间后,Ⅱ中溶液又逐渐变为浅绿色。有同学认为此时该溶液中含有 , 并进行以下实验验证:
, 并进行以下实验验证:操作
现象
结论
取少量装置Ⅱ中溶液于试管中,先滴加溶液,再滴加适量
 溶液,振荡
溶液,振荡先无明显现象,加入
 溶液后,现象是
溶液后,现象是溶液中含有

-
(4) 为探究装置Ⅱ中溶液颜色变化的原因,查阅资料后提出假设:该装置中可能存在以下两种化学反应。将反应ii补充完整。
i.
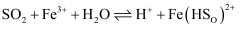 (红棕色);
(红棕色);ii.
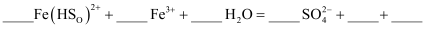
-
(5) 为检验反应ii中生成的
 , 可选用的化学试剂是。
, 可选用的化学试剂是。
最近更新
- 如图所示两个相同的验电器A和B,A带正电,B不带电用带绝缘手柄的金属棒把A、B连接起来后,B带 电,电荷移动的方
- 节能电动车为人类提供了绿色交通服务,国产某品牌电动汽车是一款高速纯电动轿车,其质量为1.2t,每个轮子与地面的接触面积为
- 设奇函数f(x)在(0,+∞)上为增函数,且f(2)=0,则不等式<0的解集为() A.(-2,0)∪(2,+∞)
- 如图所示,质量为2m的物体A经一轻质弹簧与下方地面上的质量为3m的物体B相连,弹簧的劲度系数为k,A、B都处于静止状态.
- 下列过程中,没有发生膜融合的是() A.植物体细胞杂交 B.受精作用 C.氧进入细胞中的线粒体 D.效应B细胞产生抗体
- 阅读下面的文言文,(完成4—11题。4-8每小题3分) (29分)(一)呜呼!以赂秦之地封天下之谋臣,以事秦之心礼天下之
- 如图所示,用直流电动机提升重物,重物的质量m=50 kg,电源供电电压为110 V,不计各处摩擦,当电动机以v=0.90
- 下列句子中,没有语病的一项是 A.今天老师又在班会上表扬了自己,但是我觉得还需要继续努力。 B.中国不存在纯种汉族人与长
- 有Fe2+、NO3-、Fe3+、NH4+、H+和H2O六种粒子,属于同一氧化还原反应中的反应物和生成物,下列叙述不正确的
- 纯碱和小苏打都是白色晶体,在日常生活中都可以找到。要在家庭将它们区分开,下面的方法可行的是 (
- ---Listen! David is talking happily with his mother in the n
- We at the suggestion to improve our plan by the scho
- 读下图,完成9~10题。9.图示区域在矿产资源的开发中,最容易产生的生态环境问题为() A.水土流失
- 双调·水仙子 重观瀑布 乔吉 天机织罢月梭闲,石壁高垂雪练寒。冰丝带雨悬霄汉,几千年晒未干。露华凉人怯衣单。似白
- 如图,要在公路M N旁修建一个货物中转站P,分别向A、B两个开发区运货。(分别在图上找出点P,并保留作图痕迹.)【小题1
- 我国研制的一种聚乙烯材料,超过40℃时完全熔化,低于15℃时完全凝固;有人设计,把这种材料制成小颗粒,掺在水泥中制成地板
- (6分)下表列出了①〜⑥六种元素在周期表中的位置: 族 周期 ⅠA0 1 ⅡA ⅢA ⅣA ⅤA ⅥA
- 已知正项数列{an} 满足a1=a(0<a<1=,且an+1=.求证:(1)0<an+1<;(2)an=;(3)+…+<
- 中国领导的多党合作和政治协商制度是我国的一项基本政治制度,是适合我国国情、具有中国特色的政党制度。回答下题。 我国政党制
- 将固体NH4I置于密闭容器中,在某温度下发生下列反应:NH4I(s)NH3(g)+HI(g);2HI(g)H2(g)+I



