第1节 碳的多样性 知识点题库
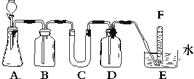
在呼吸面具和潜水艇中可用过氧化钠作为供氧剂.请选用适当的化学试剂和实验用品、用图中的实验装置进行实验,证明过氧化钠可作供氧剂.
(1)A是制取CO2的装置.写出A中发生反应的化学方程式: .
(2)填写表中空格:
仪器 | 加入试剂 | 加入该试剂的目的 |
B | 饱和NaHCO3溶液 |
|
C |
|
|
D |
|
|
(3)写出过氧化钠与二氧化碳反应的化学方程式: .
(4)试管F中收集满气体后,下一步实验操作是: .
下列说法不正确的是( )
A . 金刚石和石墨互为同素异形体
B . CH3﹣CH2OH和 CH3﹣O﹣CH3互为同分异构体
C .  He和
He和 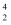 He互为同位素
D . 分子式为C4H10的物质为纯净物
He互为同位素
D . 分子式为C4H10的物质为纯净物
 He和
He和 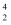 He互为同位素
D . 分子式为C4H10的物质为纯净物
He互为同位素
D . 分子式为C4H10的物质为纯净物
有下列各组微粒或物质:
A.O2和O3
B.  C和
C和  C
C
C.CH3CH2CH2CH3和 ![]()
D. 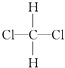 和
和 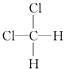
E.CH3CH2CH2CH3和 ![]()
-
(1) 组两种物质属于同系物.
-
(2) 组两种物质互为同素异形体.
-
(3) 组两物质互为同分异构体.
下列有关物质的性质与应用相对应的是( )
A . Cl2具有漂白性,可用作自来水的消毒
B . SiO2具有高沸点,可用作制备光导纤维
C . NH3具有还原性,可用作制冷剂
D . Na2O2能与CO2反应,可用作潜水艇内的供氧剂
钠及其化合物在自然界广泛存在,并有重要用途.
-
(1) 过氧化钠是钠的氧化物,写出过氧化钠中阴离子的电子式
-
(2) 把一定量过氧化钠和未知量碳酸氢钠混合物放置在密闭体系中,充分加热后,排出气体,固体残留物中一定含有的物质是(写化学式);
-
(3) 工业上可采取金属钠氧化法制取过氧化钠,其流程如下:
Na
 →Na2O
→Na2O  →Na2O2
→Na2O2如果把一定质量的过氧化钠按下列流程处理:
78克Na2O2
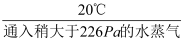 →222克A(固体)
→222克A(固体)写出A物质的化学式;
-
(4) 熔融态的过氧化钠是非常好的氧化剂,可用于工业上氧化FeSO4制高铁酸钠(Na2FeO4)(称为干法制备),干法制备中每1mol FeSO4参加反应转移4mol电子,产物中还有氧气生成.写出干法制取高铁酸钠的化学方程式:.
《馀冬录》中对胡粉[主要成分为2PbCO3·Pb(OH)2]的制法有如下描述:“嵩阳产铅,居民多造胡粉。其法:铅块悬酒缸内,封闭四十九日,开之则化为粉矣。化不白者,炒为黄丹。黄丹滓为密陀僧。”其中黄丹的主要成分为Pb3O4 , 密陀僧的主要成分为PbO。下列说法错误的是( )
A . 胡粉难溶于水
B . 胡粉和黄丹中均含有+2价的铅
C . 胡粉炒为黄丹的过程中发生的反应是非氧化还原反应
D . 密陀僧分别与物质的量浓度之比为1∶2的稀硫酸和稀硝酸反应,前者反应速率更慢
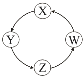
下列各组物质中,满足表中图示物质在一定条件下一步转化关系的组合有( )
序号 | X | Y | Z | W |
|
① | Si | Na2SiO3 | H2SiO3 | SiO2 | |
② | Na | NaOH | Na2CO3 | NaCl | |
③ | Cl2 | Ca(ClO)2 | HClO | HCl | |
④ | Fe | FeCl3 | FeCl2 | Fe(OH)2 |
A . ①②③
B . ①③④
C . ②③
D . ①④
某干燥粉末可能由Na2O、Na2O2、Na2CO3、NaHCO3、NaCl中的一种或几种组成。将该粉末与足量的盐酸反应有气体X逸出,X通过足量的NaOH溶液后体积缩小(同温、同压下测定),且有气体剩余。若将原来混合粉末在空气中用酒精灯加热,也有气体放出,且剩余固体的质量大于原混合粉末的质量。下列判断正确的是( )
①粉末中一定有Na2O、Na2O2、和NaHCO3
②粉末中一定不含有Na2CO3和NaCl
③粉末中一定不含有Na2O2和NaCl
④无法肯定粉末中是否含有Na2CO3和NaCl
A . ①②
B . ②③
C . ③④
D . ①④
向Na2CO3、 NaHCO3 , 混合溶液中逐滴加入稀盐酸,生成气体的量随盐酸加入量的变化关系如图所示。则下列离子组在对应的溶液中一定能大量共存的是( )
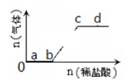
A . a点对应的溶液中:Na+、OH-、SO42-、NO3-
B . b点对应的溶液中:Al3+、Fe3+、MnO4-、Cl-
C . c点对应的溶液中:Na+、Ca2+、NO3-、Cl-
D . d点对应的溶液中:F-、NO3-、Fe2+、Ag+
下列说法正确的是( )
A . 硫酸铁既可用于净水,也可消毒杀菌
B . 工业用焦炭还原氧化铁在炼铁高炉中制铁
C . 工业上用饱和石灰水制备漂白粉
D . 二氧化硫可用于漂白纸浆
将CO2通至下列溶液中:①次氯酸钙溶液;②澄清石灰水;③氯化钙溶液;④饱和碳酸钠溶液;⑤氨的氯化钠饱和溶液,溶液会出现浑浊的有几种( )
A . 2种
B . 3种
C . 4种
D . 5种
1912年E. Beckmann冰点降低法获得了黄色的正交α- 型硫元素的一种同素异形体S8分子。1891年,M. R.. Engel 首次制得了一种菱形的ε-硫,后来证明含有S6分子。下列说法正确的是( )
A . S6和S8分子分别与铜粉反应,所得产物可能均为CuS
B . 推测Na2S8可能是一种复合分子材料
C . S6和S8分子分别与过量的氧气反应可以得到SO3
D . 等质量的S6和S8分子分别与足量的KOH反应,消耗KOH的物质的量相同
在给定条件下,下列选项中所示的物质间转化均能实现的是( )
A . SiO2  H2SiO3
H2SiO3  Na2SiO3
B . S
Na2SiO3
B . S  SO2
SO2 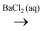 BaSO3
C . CuSO4
BaSO3
C . CuSO4  Cu(OH)2
Cu(OH)2 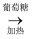 Cu2O
D . 饱和NaCl溶液
Cu2O
D . 饱和NaCl溶液  NaHCO3
NaHCO3  Na2CO3
Na2CO3
 H2SiO3
H2SiO3  Na2SiO3
B . S
Na2SiO3
B . S  SO2
SO2 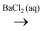 BaSO3
C . CuSO4
BaSO3
C . CuSO4  Cu(OH)2
Cu(OH)2 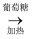 Cu2O
D . 饱和NaCl溶液
Cu2O
D . 饱和NaCl溶液  NaHCO3
NaHCO3  Na2CO3
Na2CO3
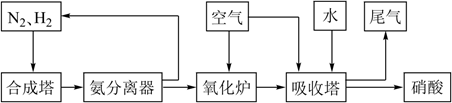
氨和硝酸是重要的工业产品,如图是工业合成氨及制备硝酸的流程示意图:
-
(1) 合成塔中发生反应的化学方程式为。
-
(2) 氨分离器中压强约为15MPa,温度约为-20℃,分离氨应用了氨的性质。
-
(3) 氧化炉中,NH3转化为NO的化学方程式为。
-
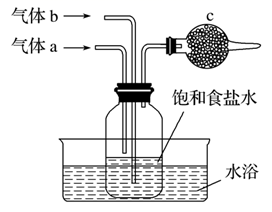
(4) 如图是在实验室中模拟“氨碱法”制取NaHCO3的部分装置。
完成下列填空:
①仔细观察两只通气导管内所处的位置,由此推断:气体a为,气体b为;两者的通入次序为。为防止尾气污染,c中可放入蘸(填写“酸”“碱”)溶液的脱脂棉。
②反应过程中可以看到上图装置饱和食盐水中有晶体逐渐析出,写出相关反应的化学方程式:。
(二)  、
、  、
、  等钠盐在生活、生产中都有着较广的应用。
等钠盐在生活、生产中都有着较广的应用。
 、
、  、
、  等钠盐在生活、生产中都有着较广的应用。
等钠盐在生活、生产中都有着较广的应用。 完成下列填空:
-
(1) 硫通常是一种淡黄色的晶体,高温下其蒸气有橙色、无色、红棕色等颜色,化学式分别为
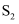 、
、 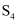 、
、  等,它们互为。
等,它们互为。
-
(2) 纺织工业中常用氯气作漂白剂,
 可以作为漂白后布匹的“脱氧剂”,试配平该化学方程式并标出电子转移的方向和数目:
可以作为漂白后布匹的“脱氧剂”,试配平该化学方程式并标出电子转移的方向和数目: 
若消耗标准状况下的
 气体
气体 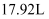 ,则转移电子数目是。
,则转移电子数目是。 -
(3) 向
 溶液中加入少许
溶液中加入少许 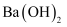 固体,忽略溶液体积变化,溶液中的
固体,忽略溶液体积变化,溶液中的  的变化是(选填“增大”、“减小”或“不变”)。
的变化是(选填“增大”、“减小”或“不变”)。
-
(4)
 的水溶液中存在如下等式,在横线处填上适当的微粒补充完整下列等式:
的水溶液中存在如下等式,在横线处填上适当的微粒补充完整下列等式:  +。
+。向
 溶液中滴加酚酞,溶液变为红色,若在该溶液中再滴加过量的
溶液中滴加酚酞,溶液变为红色,若在该溶液中再滴加过量的  溶液,现象为。
溶液,现象为。
下列实验装置不能达到实验目的的是( )
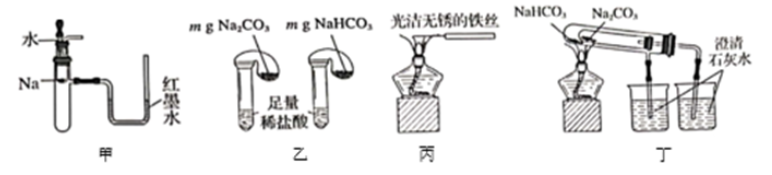
A . 图甲:验证 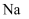 和水反应是否为放热反应
B . 图乙:鉴别碳酸钠和碳酸氢钠两种白色固体
C . 图丙:观察纯碱的焰色试验
D . 图丁比较
和水反应是否为放热反应
B . 图乙:鉴别碳酸钠和碳酸氢钠两种白色固体
C . 图丙:观察纯碱的焰色试验
D . 图丁比较  、
、  的稳定性
的稳定性
 和水反应是否为放热反应
B . 图乙:鉴别碳酸钠和碳酸氢钠两种白色固体
C . 图丙:观察纯碱的焰色试验
D . 图丁比较
和水反应是否为放热反应
B . 图乙:鉴别碳酸钠和碳酸氢钠两种白色固体
C . 图丙:观察纯碱的焰色试验
D . 图丁比较  、
、  的稳定性
的稳定性
下列说法错误的是( )
A . 研究物质组成时,常用原子吸收光谱确定物质中含有哪些金属元素
B . NaHCO3固体可以做干粉灭火剂,金属钠着火可以用其来灭火
C . 二氧化硫可以抑制酒中细菌生长,可在葡萄酒中微量添加
D . 液氨汽化时吸收大量的热,工业上可使用液氨作制冷剂
化学与社会生产和生活密切相关,下列叙述中错误的是( )
A . 缺铁性贫血患者服用补铁剂时,与维生素C同时服用效果更好
B . 咳嗽产生的飞沫分散到空气中形成气溶胶
C . 用于新版人民币票面文字等处的油墨中所含有的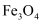 是一种磁性物质
D . 嫦娥5号带回的“快递”——“月壤”中含有珍贵的3He,它与4He互为同素异形体
是一种磁性物质
D . 嫦娥5号带回的“快递”——“月壤”中含有珍贵的3He,它与4He互为同素异形体
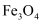 是一种磁性物质
D . 嫦娥5号带回的“快递”——“月壤”中含有珍贵的3He,它与4He互为同素异形体
是一种磁性物质
D . 嫦娥5号带回的“快递”——“月壤”中含有珍贵的3He,它与4He互为同素异形体
侯德榜为我国的制碱工业做出了突出贡献。侯氏制碱法流程如下:
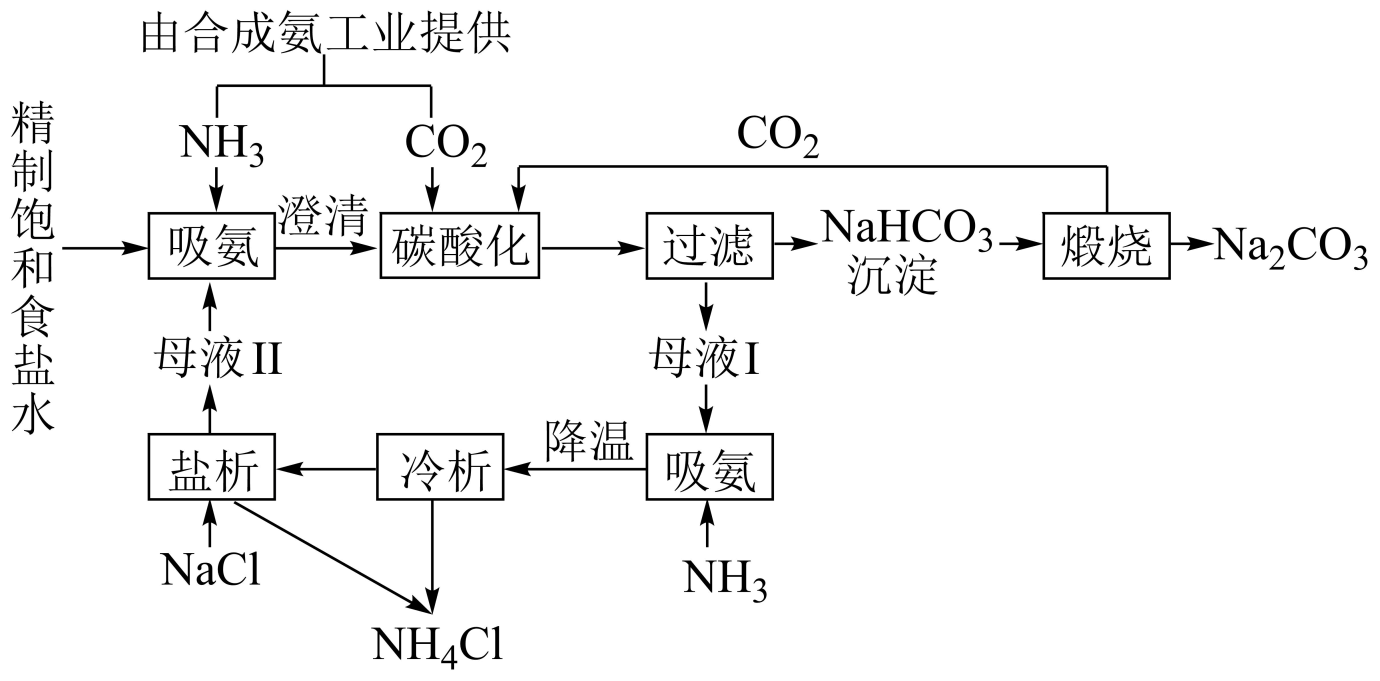
下列说法不正确的是( )
A . 精制饱和食盐水的操作依次为:取样、溶解、沉淀、过滤、蒸发浓缩、冷却结晶、过滤、洗涤、烘干
B . 该生产工艺制得纯碱的同时也得到了化学肥料
C . 吸氨操作的目的是把溶液中的碳酸氢盐转化为碳酸盐并增大铵根离子的浓度
D . 盐析环节中加入NaCl,对析出氯化铵起到了促进作用
下列说法正确的是( )
A .  和
和  互为同位素
B .
互为同位素
B .  、
、  、
、  互为同素异形体
C . 正丁烷和异丁烷互为同分异构体
D .
互为同素异形体
C . 正丁烷和异丁烷互为同分异构体
D . 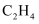 和
和  一定互为同系物
一定互为同系物
 和
和  互为同位素
B .
互为同位素
B .  、
、  、
、  互为同素异形体
C . 正丁烷和异丁烷互为同分异构体
D .
互为同素异形体
C . 正丁烷和异丁烷互为同分异构体
D . 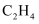 和
和  一定互为同系物
一定互为同系物
最近更新
- 如图,过正方形的顶点作直线,过作的垂线,垂足分别为.若,,则的长度为 .
- —The 5Gtechnology can help doctors treat patients who are hu
- 下列各项中,哪项是构成生物体蛋白质的氨基酸 ( )
- 2006年,商代“子龙鼎”等四件珍贵文物入藏国家博物馆。“子龙鼎”是已发现的商代青铜圆鼎中形体最大的一件,也是带有“龙”
- 1.下列加横线的成语使用正确的一项是( ) A.越来越多的青壮年背井离乡进城务工,其身后是一个个独守家园的“留守老
- 每年的《感动中国》年度人物评选被誉为“中国人的年度精神史诗”。13位来自唐山的农民,在2008年初特大雪灾袭击华南地区时
- 函数y = - xcosx的部分图象是 ( )
- 电冶金(1)金属冶炼的实质是__________________。(2)古代湿法炼铜的离子方程式为:__________
- (湘郡生试题) I was really surprised to find out that the first
- 观察下列等式:解答下面的问题:21+22+23+24+25+26+…+22015的末位数字是
- 15.补写出下列句子中的空缺部分 (1)周敦颐在《爱莲说》中说自己爱莲的原因是:“ ________________,_
- 方程|x-1|=1的解是 ;
- 为了弄清铜绿的组成和铜生成铜绿的条件,某化学实验小组进行了如下探究:(1)探究铜绿的组成。 【查阅资料】通过查阅资料知道
- 在“噬菌体侵染细菌的实验”中,噬菌体与细菌保温时间长短与放射性高低的关系图可能如下,下列关联中最合理的是(标记的噬菌体
- 默写(1) 雪山低头迎远客,。,。(2) 耳朵里有不可捉摸的声响,极远的又是极近的,极洪大的又是极细切的,像,像,像 ,
- 在2L容器中发生反应N2+3H2 2NH3,经一段时间后NH3的物质的量增加了2.4 mol,这段时间内用氢气表示的反
- 如图12-6-14所示,在坐标原点O和x=3 m处的A点放有两个完全相同的声源,声源发声的波长均为1 m.则在y轴正方向
- —Let’s go fishing if it _____ this weekend.—But nobody knows
- 居民消费是不断变化的。人们通常所说的“三大件”的变化就是生动的事例。在20世纪50—60年代,“三大件”是指缝纫机、手表
- 15.在某报《自测健康状况》的报道中,自测血压结果与相应年龄的统计数据如下表.观察表中数据的特点,用适当的数填入表中空白