课题三 综合实验设计 知识点题库
某无机盐M是一种优良的氧化剂,为确定其化学式,某小组设计并完成了如下实验: 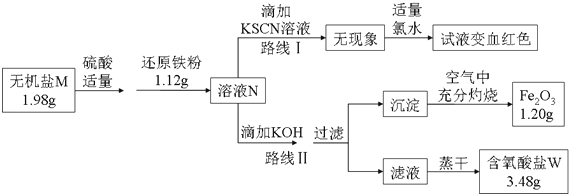
已知:①无机盐M仅由钾离子和一种含氧酸根组成,其分子中的原子个数比为2:1:4;
②如图中,将1.98g该无机盐溶于水,滴加适量稀硫酸后,再加入1.12g还原铁粉,恰好完全反应得混合溶液N.
③该小组同学将溶液N分为二等份,分别按路线Ⅰ、路线Ⅱ进行实验.
④在路线Ⅱ中,首先向溶液N中滴加适量KOH至元素X刚好沉淀完全,过滤后将沉淀在空气中充分灼烧得纯净的Fe2O3粉末1.20g;再将滤液在一定条件下蒸干,只得到3.48g纯净的不含结晶水的正盐W.
请按要求回答下列问题:
-
(1) 由路线Ⅰ的现象可知,溶液N中含有的阳离子是;
-
(2) 由实验流程图可推得,含氧酸盐W的化学式是 ;由路线Ⅱ可知,1.98g无机盐M中所含钾元素的质量为g;
-
(3) 无机盐M与1.12g还原铁粉恰好完全反应生成溶液N的化学反应方程为.
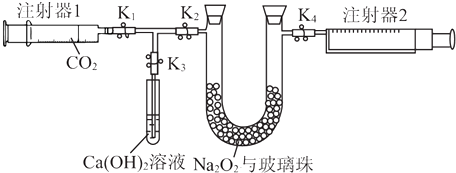
注射器1中抽取了100 mL CO2 , U型管中装有适量小玻璃珠和约1.5 gNa2O2粉末.实验开始时,打开K1、K2、K4止水夹,关闭K3止水夹,推动注射器1活塞,缓缓将CO2压至U形管,注射器2活塞缓缓向外移动.回答下列问题:(本题不考虑注射器内壁的摩擦阻力)
-
(1) U形管内的玻璃珠并不参与反应,其所起的作用除防止过氧化钠粉末被吹走外,另一个重要作用是.
-
(2) U形管中可观察到的反应现象是.
-
(3) 注射器1活塞推到底后,注射器2中收集到的气体大于50 mL,其原因除可能仍还含CO2外,还有一个重要原因是.
-
(4) 为了使剩余气体中二氧化碳能反应完,接下来的操作是.
-
(5) 要证明反应产物之一为氧气,最为方便的实验方法是.
-
(6) 本实验结束后固体产物板结,难以从U型管中取出,为了要证明固体产物中含有碳酸盐,实验时还需要从如图所示仪器和试剂中选择(填字母).当装置和药品都安装完毕后,接下来的操作步骤是.
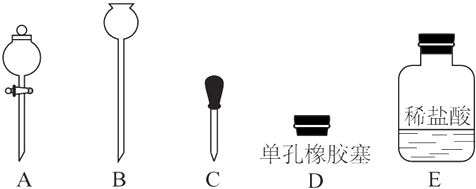
C2H5OH+HBr→C2H5Br+H2O
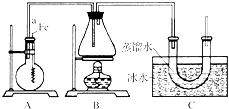
主要实验步骤如下:①连接好装置,检查装置的气密性;②向烧瓶中加入一定量的苯和液溴.向锥形瓶中加入乙醇和浓H2SO4的混合液至稍高于进气导管口处;③将A装置中的纯铁丝小心向下插入混合液中;④点燃B装置中的酒精灯,用小火缓缓对锥形瓶加热10min.
请填写下列空白:
-
(1) 写出制取溴苯的化学方程式:.
-
(2) 步骤③中观察到的现象是:.
-
(3) C装置中U形管内部用蒸馏水封住管底的作用是:.
-
(4) 反应完毕后,U形管内的现象是:.分离溴乙烷时所用的最主要仪器的名称是(只填一种).
-
(5) 实验结束,从烧瓶的混合物中分离出粗制黄色的溴苯,产生黄色的原因是其中含有(填化学式).欲得到无色的溴苯的方法是(填试剂和操作名称).
-
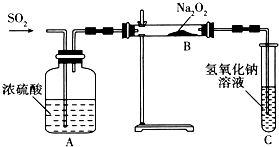
(1) 第1小组同学认为Na2O2与SO2反应生成了Na2SO3和O2 , 该反应的化学方程式是.
-
(2) 请设计一种实验方案证明Na2O2与SO2反应生成的白色固体中含有Na2SO3 . .
-
(3) 第2小组同学认为Na2O2与SO2反应除了生成Na2SO3和O2外,还有Na2SO4生成.为检验是否有Na2SO4生成,他们设计了如下方案:
将B中反应后的固体溶解于水
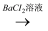 白色沉淀
白色沉淀 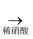 仍有部分白色沉淀不溶解,证明有Na2SO4生成
仍有部分白色沉淀不溶解,证明有Na2SO4生成上述方案是否合理?.请简要说明两点理由:
①;②.
-
(1) 实验I 制取氯酸钾和氯水利用如图所示的实验装置进行实验.
(i)盛放浓盐酸的实验仪器名称是.
(ii)A中发生反应的化学方程式是.
(iii)B中生成氯酸钾的离子反应方程式是
(iv)若对调B和C装置的位置,(填“能”或“不能”)提高B中氯酸钾的产率,原因是.
-
(2) 实验II 测定圆底烧瓶中反应残余液中盐酸的浓度
圆底烧瓶中所发生的反应会因盐酸浓度下降而停止.为测定反应残余液中盐酸的浓度,探究小组同学提出下列实验方案:
甲方案:采用酸碱中和滴定法测定.
乙方案:与足量Zn反应,测量生成的H2体积.
继而进行下列实验:
①进行甲方案实验:准确量取冷却后的残余清液,稀释一定的倍数后作为试样.
a.量取试样20.00ml,用0.10mol•L﹣1NaOH标准溶液滴定,到达滴定终点时,消耗标准溶液24.00ml,则该次滴定所测的试样中盐酸浓度为;
b.重复滴定三次后获得实验结果.
②进行乙方案实验:装置如图所示(夹持器具已略去)
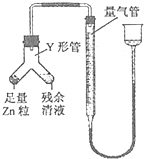 .
.(i)使Y形管中的残余清液与锌粒反应的正确操作是将转移到中,否则会造成实验结果偏低.
(ii)反应完毕,读取H2的体积,读数时应注意:a.冷却至室温b. c.视线与凹液面最低处相切.
-
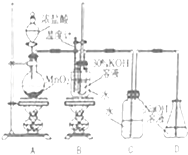
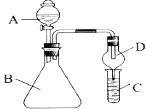
(1) 仪器A的名称为,干燥管D的作用是.
-
(2) 若要证明非金属性:Cl>I,则A中加浓盐酸,B中加(填名称),C中加淀粉﹣碘化钾溶液,观察到C中溶液的现象,即可证明.从环境保护的观点,此装置的不足之处是.
-
(3) 若要证明非金属性:C>Si,则在A中加盐酸,B中加CaCO3 , C中加(填试剂)即可证明.乙同学认为此方案有不足之处,应在B、D两装置间加装有(填试剂)的洗气瓶.
他们为了探究新制饱和氯水的组成和性质而进行了科学实验:先观察了氯水的外观性质以后,又用胶头滴管将该氯水逐滴滴入含有酚酞的KOH溶液中,边滴边振荡,并连续观察现象,发现溶液的红色逐渐褪去而得无色溶液.以下的问题需要请你来配合回答:
-
(1) 请写出新制饱和氯水中含有氯元素物质的化学式:.
-
(2) 若不再进行更多的实验,请说明能快速判断氯水中含有Cl2的主要依据:.
-
(3) 根据预测,实验中溶液红色褪去的原因可能有两种,请用简要的文字说明之:①;②.
-
(4) 他们又要通过实验进一步探究溶液红色褪去的原因究竟是上述中的①还是②,请你简述实验的方法、现象和结论:.
-
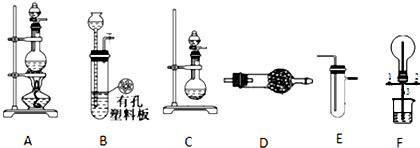
(1) I.探究氯气与氨气的反应
为制取干燥氨气,可将装置C与(填装置编号)连接;装置C中的烧瓶内固体宜选用.
a.碱石灰 b.氯化钙 c.五氧化二磷 d.生石灰
-
(2) 装置A、E、E连接可制取纯净、干燥的氯气,则两个E装置内的药品依次是.
-
(3) 装置F可用于探究氯气与氨气(已知氯气与 氨气可发生反应:3Cl2+2NH3=N2+6HCl)的反应.实验时打开开关1、3,关闭2,先向烧瓶中通入,然后关闭1、3,打开2,向烧瓶中缓慢通入一定量的另一种气体.实验一段时间后烧瓶内出现浓厚的白烟并在容器内壁凝结,请设计一个实验方案鉴定该固体中的阳离子.
-
(4) Ⅱ.探究某些物质的性质
利用装置A、E,可设计实验比较Cl﹣和Br﹣的还原性强弱,能证明结论的实验现象是.
-
(5) 若利用装置A、E进行乙烯与溴水反应的实验,写出反应的化学方程式.
-
(6) 将装置B、C分别与F相连后,进行H2S与SO2反应的实验.F的烧瓶中发生反应的化学方程式为;F的烧杯所起的作用是.
实验目的 | 实验操作及现象 | |
A | 检验Na2SO3溶液是否变质 | 向Na2SO3溶液中加入Ba(NO3)2溶液,出现白色沉淀,再加入稀硝酸,沉淀不溶解 |
B | 证明酸性条件下H2O2氧化性强于I2 | 向淀粉KI溶液中滴入3滴稀硫酸,未见溶液变蓝; 再加入10%的H2O2溶液,溶液立即变蓝色 |
C | 证明碳的非金属性强于硅 | 将浓盐酸滴入Na2CO3固体中,生成的气体通入盛有Na2SiO3溶液的试管中,出现浑浊 |
D | 证明SO2具有漂白性 | 将SO2通入酸性KMnO4溶液中,溶液紫色褪去 |
-
(1) 在25℃下,控制光照强度、废水样品初始浓度和催化剂用量相同,调节不同的初始pH和一定浓度草酸溶液用量,作对比实验,完成以下实验设计表(表中不要留空格)。
实验编号
初始pH
废水样品体积/mL
草酸溶液体积/mL
蒸馏水体积/mL
①
4
b=
10
30
②
5
60
10
d=
③
a=
60
c=
20
测得实验①和②溶液中的Cr2O72-浓度随时间变化关系如图所示。
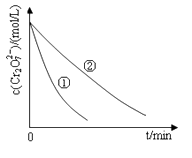
-
(2) 上述反应后草酸被氧化为(填化学式);
-
(3) 实验①和②的结果表明;
-
(4) 该课题组对铁明矾[Al2Fe(SO4)4 ·4H2O]中起催化作用的成分提出如下假设,请你完成假设二和假设三:
假设一:Fe2+起催化作用;假设二:;假设三:;……
-
(5) 请你设计实验验证上述假设一,完成下表中内容。(除了上述实验提供的试剂外,可供选择的药品有K2SO4、FeSO4、K2SO4·Al2(SO4)3·24H2O、Al2(SO4)3等。(溶液中Cr2O72-的浓度可用仪器测定)
实验方案(不要求写具体操作过程)
预期实验结果和结论
取代替实验①中的铁明矾,控制其他反应条件与实验①相同,进行对比实验
反应进行相同时间后,
若溶液中的Cr2O72-浓度则假设一成立;
若溶液中的Cr2O72-浓度则假设一不成立;
-
(6) 铁明矾长期存放,其中的亚铁离子可能会变质。为测定铁明矾中亚铁离子的质量分数。取5.6g铁明矾晶体,将其配制为100ml的溶液,取出20ml置于锥形瓶中。用0.01mol/L的标准KMnO4溶液进行滴定(还原产物为Mn2+),平行做4组实验,得出如下表数值。
组数
1
2
3
4
消耗V(KMnO4)/ml
20.04
20.00
18.90
19.96
请计算铁明矾中亚铁离子的质量分数:。若滴定结束后读数时仰视,测定结果(填“偏大”“不影响”或“偏小”)
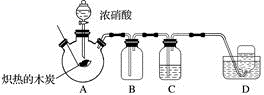
请回答下列问题:
-
(1) 检查装置气密性后,将燃烧匙中的木炭在酒精灯上加热至红热状态,伸入三口烧瓶中,并塞紧瓶塞,滴加浓硝酸,可观察到三口烧瓶中气体的颜色为,产生该气体的化学方程式是。
-
(2) 装置C中盛有足量Ba(OH)2溶液,炽热的木炭与浓硝酸反应后可观察到C中出现白色沉淀,该白色沉淀为(填化学式)。
-
(3) 装置B的作用是。
-
(4) 装置D中收集到了无色气体,部分同学认为是NO,还有部分同学认为是O2。
①下列对该气体的检验方法合适的是。
A.敞口观察装置D中集气瓶内气体的颜色变化
B.将湿润的蓝色石蕊试纸伸入集气瓶内,观察蓝色石蕊试纸是否变红
C.将带火星的木条伸入集气瓶中,观察木条是否复燃
②如果D中集气瓶中收集的无色气体是氧气,则氧气的来源是。
-
(1) Ⅰ:将钠、铁、镁、铝各1 mol分别投入到足量的同浓度的盐酸中,试预测实验结果:与盐酸反应最剧烈。
-
(2) 向Na2S溶液中通入氯气出现黄色浑浊,可证明Cl的非金属性比S强,反应的离子方程式为。
-
(3) Ⅱ:利用如图装置可验证同主族元素非金属性的变化规律。
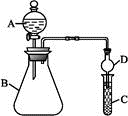
仪器B的名称为,干燥管D的作用为防止。
-
(4) 若要证明非金属性:Cl>I- , 则A中加浓盐酸,B中加KMnO4 , KMnO4与浓盐酸常温下反应生成氯气,C中加淀粉-碘化钾混合溶液,观察到C中溶液(填现象),即可证明。从环境保护的观点考虑,此装置缺少尾气处理装置,可用溶液吸收尾气。
-
(5) 若要证明非金属性:
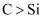 ,则在A中加盐酸、B中加
,则在A中加盐酸、B中加 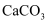 、C中加
、C中加  溶液。观察到C中溶液
溶液。观察到C中溶液  填现象
填现象  ,即可证明。但有的同学认为盐酸具有挥发性,可进入C中干扰实验,应在两装置间添加装有溶液的洗气瓶除去。
,即可证明。但有的同学认为盐酸具有挥发性,可进入C中干扰实验,应在两装置间添加装有溶液的洗气瓶除去。
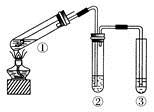
| 选项 | 叙述I | 叙述Ⅱ |
| A | 硝基苯的沸点比苯的沸点高 | 硝基苯和苯可通过蒸馏初步分离 |
| B | 乙二酸可与KMnO4溶液发生反应 | 乙二酸具有酸性 |
| C | Na2S 还原性强 | Na2S用于除去废水中的Cu2+和Hg2+ |
| D | 酸性:HCl>H2S | 非金属性:Cl>S |
-
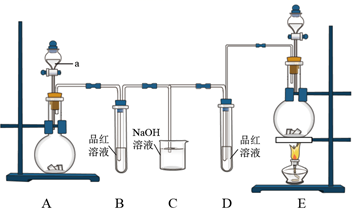
(1) 仪器a的名称是。
-
(2) 他们制备SO2的反应原理为
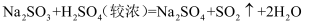 ,根据反应特点,制备SO2应选用上图中的装置。(填A或E)
,根据反应特点,制备SO2应选用上图中的装置。(填A或E)
-
(3) 在制备Cl2时他们使用了浓盐酸,结合另一发生装置的特点,请你写出制备Cl2的反应方程式,该反应在含4mol浓盐酸的反应体系中充分反应,生成的Cl2在标准状况下的体积为22.4L。(填“>”或“<”或“=”)
-
(4) 反应开始后,发现B、D两支试管中的品红溶液都褪色,停止通气后,分别加热两支试管中的液体,B试管中的现象是。
-
(5) C烧杯中NaOH溶液的作用是。
-
(6) 该小组同学将两种气体混合后通入品红溶液,一段时间后,品红溶液几乎不褪色。查阅资料得知:两种气体按体积比1:1混合,再与水反应可生成两种常见的酸,因而失去漂白作用,写出反应的化学方程式。
实验序号 | 实验操作 | 实验现象 |
1 | 向7.5 mL1mol·L-1NaHCO3溶液中加入长3cm的镁条 | 持续快速产生大量气泡,溶液略显浑浊 |
-
(1) I.探究反应产生的气体成分。
经检验反应产生的气体有H2 , 实验室检验H2的方法为。
-
(2) 小组成员认为反应产生的气体中可能有CO2 , 并对此进行了如下实验(图1、图2中曲线②均为对应加入镁条的数据):
实验序号
实验操作
2
分别称取两份6.0 mL 1 mol·L-1NaHCO3溶液于两个相同塑料瓶中(其中一个加入0.1g镁条),塞紧CO2气体传感器,采集数据,各重复实验1次,得到图1所示曲线
3
分别称取两份30.0 mL 1 mol·L-1NaHCO3溶液于两个相同烧杯中(其中一个加入1.1g镁条),插入pH传感器,搅拌并采集数据,得到图2所示曲线
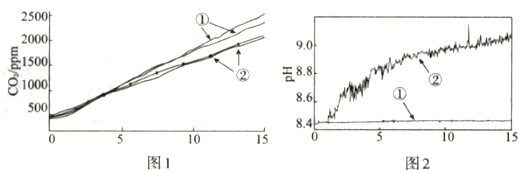
图1中曲线②对应的CO2含量逐渐增大的原因为 (用化学方程式表示);结合实验3解释,随着时间推移,图1中曲线②的数值低于曲线①的原因为。
-
(3) II.探究Mg与NaHCO3溶液反应比与热水反应快的原因。
小组成员推测可能是溶液中的Na+或HCO
 加快了该反应的发生,对比实验1设计实验如下:
加快了该反应的发生,对比实验1设计实验如下:
结合实验1和4,可知溶液中的HCO实验序号
实验操作
实验现象
4
向 溶液中加入长3 cm的镁条
持续快速产生大量气泡,溶液略显浑浊
 加快了反应的发生。
加快了反应的发生。
①实验4中横线处内容为。
②查阅文献可知,Mg(OH)2质地致密,MgCO3质地疏松,请结合必要的文字和化学用语解释HCO
 能加快该反应的原因为。
能加快该反应的原因为。 -
(4) III.探究固体浑浊物的组成。
文献显示,固体浑浊物为Mg(OH)2和MgCO3的混合物。甲、乙两位同学设计不同方案,测定混合物组成。
甲同学借助下图装置(可重复选用),通过测定固体热分解产物水及二氧化碳的质量,测定其组成。按照该方案,装置的连接顺序为(填字母编号)。
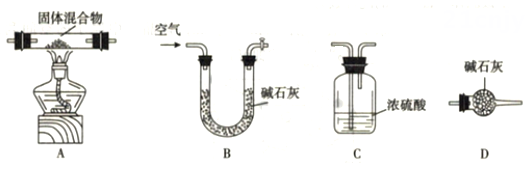
-
(5) 乙同学只测定了固体浑浊物在热分解前后的质量分别为3.42 g和2.00g,据此计算出固体浑浊物中n[Mg(OH)2]:n[MgCO3]=。
选项 | 实验操作 | 试剂A | 现象 | 结论 |
A |
| 酸性KMnO4溶液 | 紫色褪去 | SO2具有还原性 |
B | 新制氯水 | 黄绿色褪去 | SO2具有漂白性 | |
C | H2S溶液 | 出现淡黄色浑浊 | SO2具有氧化性 | |
D | 盐酸酸化的BaCl2溶液 | 无明显变化,一段时间后产生白色沉淀 | 硫元素从+4价被氧化到+6价 |
选项 | 实验操作和现象 | 结论 |
A | 将一块用砂纸打磨过的铝条放入试管,再加入98%浓硫酸3mL,铝条表面无明显现象 | 铝与浓硫酸常温下不反应 |
B | 向试管中加入3mL稀KMnO4酸性溶液,再通入SO2气体,紫红色褪去 | SO2具有漂白性 |
C | 室温下,向 FeCl3溶液中滴加少量KI溶液,再滴加几滴淀粉溶液,溶液变蓝色 | Fe3+的氧化性比I2的强 |
D | 将溶液X与稀盐酸反应产生的气体通入澄清石灰水,石灰水变浑浊 | 溶液X中一定含有CO32- |
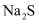 溶液中通入足量
溶液中通入足量 , 生成淡黄色沉淀,证明
, 生成淡黄色沉淀,证明 具有氧化性
B . 向淀粉水解溶液中滴加少量新制
具有氧化性
B . 向淀粉水解溶液中滴加少量新制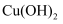 悬浊液,加热无砖红色沉淀,证明淀粉未水解
C . 向丙烯醇中滴加酸性
悬浊液,加热无砖红色沉淀,证明淀粉未水解
C . 向丙烯醇中滴加酸性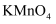 溶液,溶液褪色,证明丙烯醇中含有碳碳双键
D . 某溶液中加入盐酸,生成使澄清石灰水变浑浊的气体,则溶液中一定含有
溶液,溶液褪色,证明丙烯醇中含有碳碳双键
D . 某溶液中加入盐酸,生成使澄清石灰水变浑浊的气体,则溶液中一定含有 或
或

- .已知分别是双曲线的左、右顶点,是双曲线右支上位于第一象限的动点,设的斜率分别,则的取值范围是 A. B.
- 下列物质的用途与其化学性质相关的是()A. 用铝作导线 B. 用汽油去除衣物上的油污 C. 用天然气作燃料煮饭 D. 用
- 配制100 mL、1.0 mol·L-1的NaOH溶液,下列情况会导致溶液浓度偏高的是( )A.容量瓶使用前经蒸馏
- 小磊要制作一个三角形的钢架模型,在这个三角形中,长度为x(单位:cm)的边与这条边上的高之和为40cm,这个三角形的面积
- AB垂直于所在的平面,,当的面积最大时,点A到直线CD的距离为 。
- 下图中人物在2000年的世纪之交曾被西方主要媒体评选为“千年风云人物”,他离开我们已有一百多年,但其学说仍然在深刻地影响
- 关于右图所示装置的叙述,错误的是 A.锌是负极,其质量逐渐减小 B.氢离子在铜表面被还原,产生
- NO和CO都是汽车尾气中的有害物质,它们能缓慢地起反应,反应的化学方程式为2CO+2NO=N2+2CO2,为了控制大气污
- 中国是农业古国,每年立春日,都十分重视“鞭牛迎春”这一传统活动,唱词为“一鞭曰风调雨顺,二鞭曰国泰民安,三
- 请从下列词语中找出错别字,并将正确的字填入空格中。(4分)慷慨淋漓 锋芒必露
- —May I yourdictionary? —Sorry, I itat home. A
- 读某地景观素描图,完成16——17题。16.该地地质构造属于 ( ) A.断层 B.山岭
- (上海)右图表示植物细胞亚显微结构,请据图回答: [请在[ ]中填编号,横线上填文字。] (1)此图表示植物细胞的模式
- 下列装置图中,中间的试管收集浓硝酸与铜丝反应所生成的气体,何者可使收集到的气体中空气的含量最少()
- 下列叙述正确的是()A. 氢氧化钠的摩尔质量是40g B. 1molNaOH的质量是40g/mol C. 1gH2和1g
- 节约资源,保护环境,从我们身边的小事做起。高飞是一个注重“低碳”生活的中学生,假设你是他, 请以 “MyLow-carb
- 设函数与的图象的交战坐标为(a,b),则的值为__________.
- 对于蜡烛燃烧与食物腐烂的相同点,下列说法正确的是( ) A.都发光 B.都剧烈地产生热量 C.都是氧化反应
- 设NA为阿伏加德罗常数,下列说法正确的是 A.标准状况下NA个SO3的体积为22.4 L B.1 mol Fe与足量的
- 若双曲线的渐近线方程为,它的一个焦点是,则双曲线的方程是__________.