课题三 综合实验设计 知识点题库
某同学在常温下设计以下实验流程探究Na2S2O3的化学性质:pH=8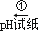 Na2S2O3溶液
Na2S2O3溶液 白色沉淀B
白色沉淀B
下列说法正确的是( )
提出猜想
问题1:在周期表中,铜与铝的位置很接近,铜不如铝活泼,氢氧化铝具有两性,氢氧化铜也有两性吗?
问题2:铁和铜都有变价,一般情况下,正二价铁的稳定性小于正三价的铁,正一价铜的稳定性也小于正二价的铜吗?
问题3:氧化铜有氧化性,能被H2、CO还原,它也能被氮的某种气态氢化物还原吗?
实验探究
-
(1) I.解决问题1
a.需用到的药品除1mol•L﹣1CuSO4溶液、稀硫酸外还需(填试剂的化学式)溶液.
b.用胆矾晶体配制1mol•L﹣1CuSO4溶液250mL,选用的仪器除烧杯、托盘天平、药匙、
玻璃棒、胶头滴管外,还有(填仪器名称).
c.为达到实验目的,请你补全实验内容和步骤:
①用CuSO4溶液制备Cu(OH)2;
②.
-
(2) Ⅱ.解决问题2
取一定量I中制备获得的氢氧化铜固体于坩埚中灼烧,当温度达到80~100℃得到黑色固体粉末;继续加热至1000℃以上,黑色粉末全部变成红色粉末氧化亚铜;取适量红色氧化亚铜粉末于洁净试管中,加入过量的稀硫酸(或盐酸),得到蓝色溶液,同时观察到试管底部还有红色固体存在.根据以上实验现象回答问题.
a.写出氧化亚铜与稀硫酸(或盐酸)反应的离子方程式:.
b.从实验Ⅱ可得出的结论是在高温下正一价铜比正二价铜(填稳定或不稳定),
溶液中正一价铜比正二价铜(填稳定或不稳定).
-
(3) Ⅲ.解决问题3
设计如下装置(夹持装置未画出):
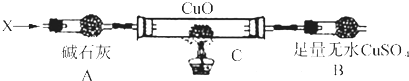
当氮的某种气态氢化物(X)缓缓通过灼热的氧化铜时,观察到氧化铜由黑色变成了红色,无水硫酸铜变成蓝色,生成物中还有一种无污染的单质气体Y;将X通入灼热的CuO燃烧管完全反应后,消耗0.01mol X,测得B装置增重0.36g,并收集到0.28g气体Y.
a.仪器A的名称是.
b.X的化学式为.
-
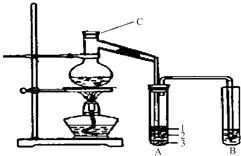
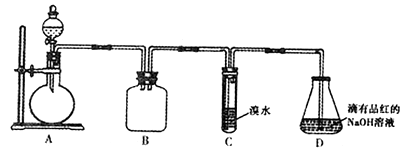
(1) 装置图中C仪器的名称为,向C中加入的反应物是溴化钠、和1:1的硫酸.配制体积比1:1的硫酸所用的定量仪器为(选填编号).
a.天平 b.量筒 c.容量瓶 d.滴定管
-
(2) 写出加热时烧瓶中发生的主要反应的化学方程式.
-
(3) 将生成物导入盛有冰水混合物的试管A中,冰水混合物的作用是.
如图所示试管A中的物质分为三层,产物在第层.
-
(4) 试管A中除了产物和水之外,还可能存在、(写出化学式).
-
(5) 用浓的硫酸进行实验,若试管A中获得的有机物呈橙红色,除去其中杂质的最合理的方法是(选填编号).
a.蒸馏 b.氢氧化钠溶液洗涤
c.用四氯化碳萃取 d.用亚硫酸钠溶液洗涤
若试管B中的酸性高锰酸钾溶液褪色,使之褪色的物质的名称应该是.
-
(6) 实验员老师建议把上述装置中的仪器连接部分都改成标准玻璃接口,其原因是:.
-
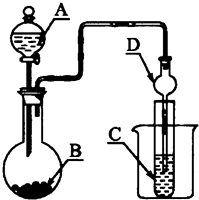
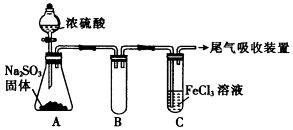
(1) 反应开始一段时间后,装置C中的现象为.
-
(2) 根据以上现象,该小组同学认为SO2与FeCl3溶液发生了氧化还原反应.
①写出SO2与FeCl3溶液反应的离子方程式:.
②向装置C中通入足量SO2发生反应后,检验生成的Fe2+的方法是.
③该小组同学向反应后的装置C的试管中加入硝酸酸化的BaCl2溶液,若出现白色沉淀,则证明反应生成了SO42﹣ . 该做法不合理的理由是.
-
(3) 若将装置C中FeCl3溶液更换为Fe(NO3)3和BaCl2的混合液,可观察到装置C中出现白色沉淀,该小组对装置C中产生沉淀的原因提出下列假设(不考虑各因素的叠加):
假设1:装置A中白雾进人装置C中参与反应.
假设2:.
假设3:在酸性条件下NO3﹣能氧化SO2 .
-
(4) 请你设计实验验证上述假设3,写出实验步骤、预期现象和结论.
实验步骤(简述操作过程)
预期现象和结论
③
②
③
-
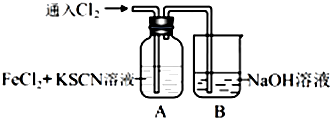
(1) B中反应的化学方程式是;
-
(2) 为了探究A中溶液由红色变为黄色的原因,甲同学进行如下实验.取A中黄色溶液于试管中,加入NaOH溶液,有红褐色沉淀生成,则溶液中一定存在;
-
(3) 甲同学猜想SCN﹣可能被Cl2氧化了,他进行了如下研究:
取A中黄色溶液于试管中,加入用盐酸酸化的BaCl2溶液,产生白色沉淀,由此证明SCN﹣中被氧化的元素是;
-
(4) 8.12天津港特大爆炸事故现场有700吨左右氰化钠,氰化钠剧毒.有少量因爆炸冲击发生泄漏.这些泄露的氰化钠可通过喷洒氧化剂双氧水的方式来处理,以减轻污染.
请写出NaCN的电子式,偏碱性条件下,氰化钠溶液的CN﹣被双氧水氧化为HCO3﹣ , 同时放出NH3 , 该反应的离子方程式为.
试回答:
-
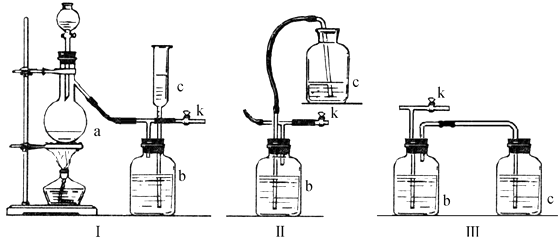
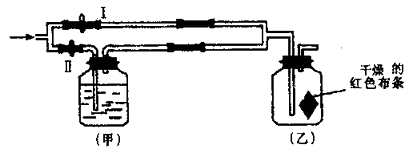
(1) 若用[Ⅰ]制取氯气,b瓶加入的液体一般为.在选取试剂正确且适量的前题下,反应开始后,当关闭活塞K时,如若发现c中液面不明显上升,你分析可能的原因是,检查的简单方法是.
-
(2) 装置(Ⅰ)中b能防止多余气体逸散的原因是:.
-
(3) 欲用[Ⅱ]或[Ⅲ]代替[Ⅰ]中的b~c部分(选用液体相同),是否可行?说明理由.
[Ⅱ]是否可行(填“是”或“否”)理由是:.
[Ⅲ]是否可行(填“是”或“否”)理由是:.
-
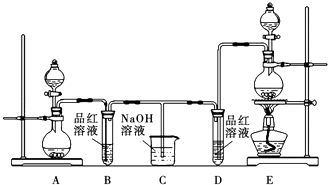
(1) 实验室制备Cl2依据的原理是:,应选用上图A~E装置中的(填序号)制Cl2 .
-
(2) 反应开始后,发现B、D两个试管中的品红溶液都褪色,停止通气后,给B、D两个试管中的液体加热,B试管中的现象是.
-
(3) 装置C的作用是.
-
(4) 若装置B、D中的品红溶液均换成紫色石蕊溶液,则B试管中的现象是.
-
(5) SO2与Cl2以体积比1:1混合后通入水中,是否还有漂白性(填“是”或“否”),原 因是(用化学方程式表示):,如何用实验证明SO2与Cl2是否恰好完全反应.
①浓H2SO4 ②浓NaOH溶液 ③KI溶液 ④饱和NaCl溶液
-
(1) 装置B的作用是。
-
(2) 装置C的目的是检验SO2的性。装置D中NaOH全部转化为NaHSO3的标志是。
-
(3) 请设计简单实验证明:室温下,NaHSO3溶液中HSO3-的电离平衡常数Ka与水解平衡常数Kb的相对大小关系。
-
(4) 向装置D所得NaHSO3溶液中加入NaClO溶液时,反应有下列三种可能的情况:
Ⅰ.HSO3-与ClO-恰好反应 Ⅱ. NaClO不足 Ⅲ. NaClO过量
甲同学分别取上述混合溶液于试管中,通过下列实验确定该反应属于哪一种情况,请完成下表:(已知酸性:H2SO3>H2CO3>HClO)
实验序号
实验操作
现象
结论
①
加入几小块CaCO3固体
有气泡产生
Ⅰ或Ⅱ
②
滴加少量淀粉KI溶液,振荡
Ⅲ
③
滴加少量溴水,振荡
Ⅱ
④
滴加少量酸性KMnO4溶液,振荡
溶液呈紫色
-
(5) 测定某葡萄酒中抗氧化剂的残留量(以游离SO2计算)的方案如下:

(已知:滴定时反应的化学方程式为SO2+I2 +2H2O=H2SO4+2HI)
①按上述方案实验,消耗标准I2溶液25.00mL,该次实验测得样品中抗氧化剂的残留量(以游离SO2计算)为g·L-1。
②在上述实验过程中,若有部分HI 被空气氧化,则测得结果(填“偏高”、偏低”或“不变”)。
-
(1) 常温下,下列事实能证明HA是弱电解质的是。
①某NaA溶液的pH=9
②用HA溶液做导电实验,灯泡很暗
③等浓度、等体积的硫酸和HA溶液分别与足量锌反应,硫酸产生的氢气多
④0.1mol·L-1HA溶液的pH≈2.8
⑤配制相同浓度的硫酸和HA,分别测定两溶液的pH,硫酸的pH小于HA的pH
-
(2) 某温度时,0.1mol·L-1的HA溶液中的c(H+)与0.01mol·L-1的HA溶液中的c(H+)的比值(填“大于”“小于”或“等于”)10。
-
(3) 已知:25 ℃时,HA的电离平衡常数为6.25×10-7。
①求该温度时,0.1mol·L-1的HA溶液中c1(H+)=mol·L-1。[水电离出的c(H+)、c(OH-)忽略不计,下同]
②若该温度时向该溶液中加入一定量的NH4A(假设溶液体积不变),使溶液中c(A-)变为5×10-2mol·L-1 , 则此时c2(H+)=mol·L-1。
-
(4) 已知:常温下,NH3·H2O的电离平衡常数为1.74×10-5;则NH4A溶液呈性,NH4A溶液中物质的量浓度最大的离子是(填化学式)。
-
(5) 现用某未知浓度(设为c′)的CH3COOH溶液及其他仪器、药品,通过实验测定一定温度下CH3COOH的电离平衡常数,需测定的数据有(用简要的文字说明):
①实验时的温度;②;③用(填一种实验方法)测定CH3COOH溶液浓度c′。
| 实验操作 | 实验目的 | |
| A | 取绿豆大小、等体积的钠块分别投入等体积的水和乙醇中 | 证明乙醇羟基中的氢原子不如水分子中的氢原子活泼 |
| B | 将形状、大小均相等的铁片分别投入等体积的稀盐酸和浓盐酸中 | 证明溶液浓度越大,反应速率越快 |
| C | 用苯与浓H2SO4和浓HNO3制备硝基苯,将产物倒入NaOH溶液中,静置,分液 | 除去硝基苯中混有浓H2SO4和浓HNO3 |
| D | 在淀粉溶液中加入稀硫酸,水浴加热,一段时间后,再加入少量新制的氢氧化铜悬浊液并加热煮沸 | 验证淀粉已水解 |
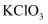 和
和 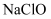 ,探究其氧化还原性质。
,探究其氧化还原性质。 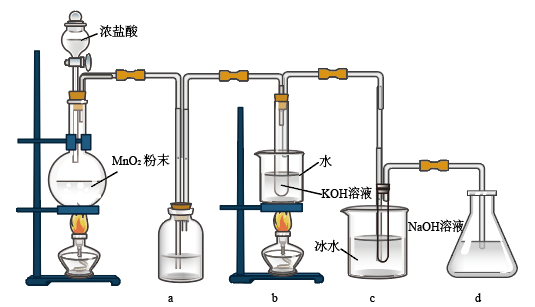
回答下列问题:
-
(1) 盛放MnO2粉末的仪器名称是,a中的试剂为,b中采用的加热方式是,c中化学反应的离子方程式是。
-
(2) 反应结束后,取出b中试管,经冷却结晶,,,干燥,得到
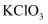 晶体。d的作用是,可选用试剂 (填编号)。
晶体。d的作用是,可选用试剂 (填编号)。 a.
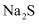 b.
b.  c.
c. 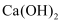 d.
d. 
-
(3) 取少量
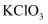 和
和 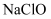 溶液分别置于1号和2号试管中,滴加中性
溶液分别置于1号和2号试管中,滴加中性  溶液。1号试管溶液颜色不变。2号试管溶液变为棕色,加入
溶液。1号试管溶液颜色不变。2号试管溶液变为棕色,加入  振荡,静置后
振荡,静置后  显色。可知该条件下
显色。可知该条件下 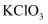 的氧化能力
的氧化能力 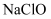 (填“大于”或“小于”)。
(填“大于”或“小于”)。
-
(4) 制备
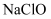 时,温度过高会生成
时,温度过高会生成 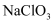 。当
。当 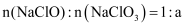 时,该反应中
时,该反应中 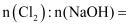 。
。
②2CuCl2+4KSCN=2CuSCN↓(白色)+(SCN)2+4KCl——该反应速率很快
③(SCN)2 , 拟卤素,化学性质和氯气相似。
Cu(过量)与 FeCl3 溶液反应,静置后取上层清液,小明将 KSCN 溶液滴加到混合液中,他观察到瞬间产生白色沉淀,局部出现红色;振荡试管,红色又迅速褪去。请你判断下列说法正确的是( )
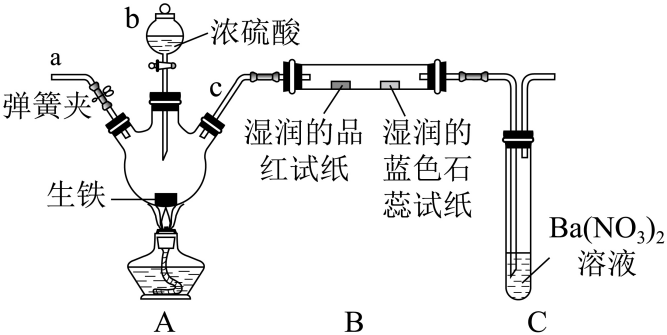
选项 | A | B | C | D |
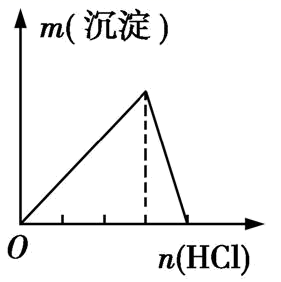
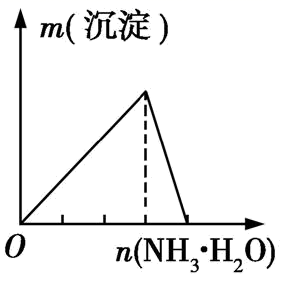
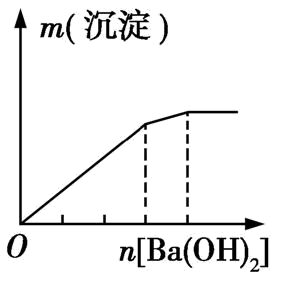
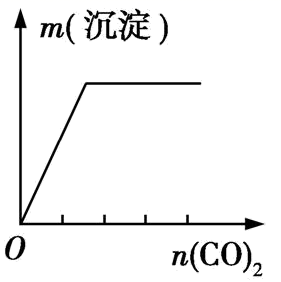
实验 | NaAlO2溶液中逐滴滴加盐酸至过量 | AlCl3溶液中逐滴滴加氨水至过量 | 明矾溶液中逐滴滴加Ba(OH)2溶液至过量 | 澄清石灰水中缓慢通入CO2至过量 |
图像 |
|
|
|
|
-
(1) 甲同学按上图所示装置进行实验(夹持装置及尾气处理装置未画出)。仪器b的名称为实验开始前打开弹簧夹,向a处通入
 , 其目的是,实验过程中将浓硫酸加入装置A中的操作是。
, 其目的是,实验过程中将浓硫酸加入装置A中的操作是。
-
(2) 要证明
 具有漂白性,在装置B中观察到现象。装置C中有白色沉淀生成,写出该反应的离子方程式:。
具有漂白性,在装置B中观察到现象。装置C中有白色沉淀生成,写出该反应的离子方程式:。
-
(3) 乙同学认为装置A中还会产生
 气体,请写出产生
气体,请写出产生 的化学方程式:,为了验证装置A中产生的气体中含有
的化学方程式:,为了验证装置A中产生的气体中含有 , 应先从下列①~④中选出必要的装置连接A装置中c处管口,从左到右的顺序为c→( )→( )→( )(填序号) 。
, 应先从下列①~④中选出必要的装置连接A装置中c处管口,从左到右的顺序为c→( )→( )→( )(填序号) 。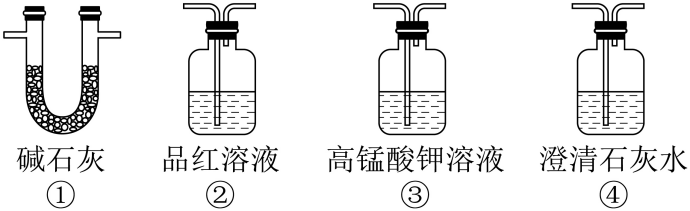
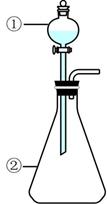
| 选项 | ①中溶液 | ②中物质 | 预期②中现象 |
| A | 稀硫酸 | 碳酸钠溶液 | 立即产生无色气体 |
| B | 浓硝酸 | 打磨后的铝条 | 产生红棕色气体 |
| C | SO2的饱和溶液 | 品红溶液 | 溶液红色逐渐褪去 |
| D | 浓硫酸 | 木炭粉 | 产生无色气体 |
选项 | 实验操作 | 实验现象 | 结论 |
A | 向某盐溶液中先加入氯水,再滴加KSCN溶液 | 溶液变红色 | 一定含有Fe2+ |
B | SO2缓慢通入滴有酚酞的NaOH溶液中 | 溶液红色褪去 | SO2具有漂白性 |
C | 少量Zn粉加入1.0mol/L Fe2(SO4)3溶液中 | 溶液颜色变浅 | 金属Zn比Fe活泼 |
D | 取少量某无色溶液,先滴加氯水,再加入少量CCl4 , 振荡、静置 | 溶液分层,下层呈紫红色 | 原无色溶液中一定有I- |
 , 请选择下列部分装置制备二氯异氰尿酸钠并探究其性质。
, 请选择下列部分装置制备二氯异氰尿酸钠并探究其性质。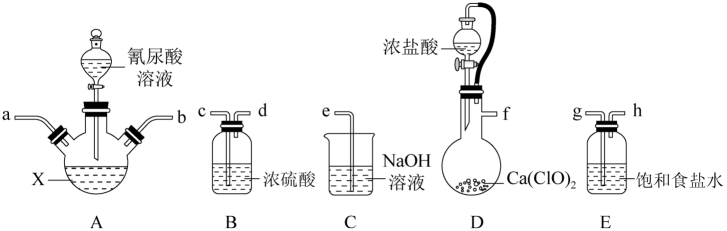
请回答下列问题:
-
(1) 选择合适装置,按气流从左至右,导管连接顺序为(填小写字母)。
-
(2) 将D中试剂换成氯酸钾后发生反应的化学方程式为。
-
(3) 仪器X中的试剂是。
-
(4) 实验时,先向A中通入氯气,生成高浓度的NaClO溶液后,再加入氰尿酸溶液。在加入氰尿酸溶液后还要继续通入一定量的氯气,其原因是。
-
(5) 反应结束后,A中浊液经过滤、、得到粗产品mg。
-
(6) 粗产品中NaC3N3O3Cl2含量测定。将mg粗产品溶于无氧蒸馏水中配制成100mL溶液,取10.00mL所配制溶液于碘量瓶中,加入适量稀硫酸和过量KI溶液,密封在暗处静置5min。用c mol/L Na2S2O3标准溶液进行滴定,加入淀粉指示剂,滴定至终点,消耗
 溶液。(假设杂质不与
溶液。(假设杂质不与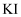 反应,涉及的反应为:C3N3O3Cl
反应,涉及的反应为:C3N3O3Cl +3H++4I- = C3H3N3O3+2I2+2Cl- ,
+3H++4I- = C3H3N3O3+2I2+2Cl- ,  )
)①滴定终点现象是。
②则NaC3N3O3Cl2的含量为
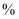 。(用含m,c,V的代数式表示)
。(用含m,c,V的代数式表示)
- When I was twelve years old, my father took me to see Zig Zi
- 与汽车中长途客运相比,高铁具有速度快、能耗低、安全性能高等优势,更能满足人们基于快捷、经济、安全等综合考虑的出行
- 正确的实验操作对实验结果、人身安全都非常重要.下列实验操作正确的是() A. B. C. D.
- 对下列有关实验的描述正确的是A. 在做乙醇的消去反应实验时,要使液体温度迅速升到140℃B. 苯中混有苯酚,加浓溴水,然
- 与直线平行,并且距离等于的直线方程是____________。
- 如图所示的电路中,两平行金属板A、B水平放置,两板间的距离d=40 cm。电源电动势E=24V,内电阻r=1 Ω,电阻R
- 下列有关细胞结构的说法,正确的是 A.蓝藻细胞与豌豆叶肉细胞都有核糖体和叶绿体 B.内质网、液
- 古希腊哲学家普罗泰戈拉认为“人是万物的尺度”。下列说法与其观点一致的是 A.天行有常,不为尧存,不为桀亡 B.物是
- 如图,点E在正方形ABCD内,满足∠AEB=90°,AE=3,BE=4,则阴影部分的面积是() .A. 19
- 下图是气体物质的粒子示意图,图中“●”和“○”分别表示两种不同的原子,其中表示单质的是() A. B. C.
- 如图所示,直线是一簇未标明方向的由点电荷产生的电场线,曲线是某一带电粒子通过电场区域时的运动轨迹,a、b是轨迹上的两点.
- She took the boy _____ the hand and led him _____ the zero.
- 下列现象或新技术应用中,不涉及胶体性质的是( )A.在饱和氯化铁溶液中逐滴加入NaOH溶液,产生红褐色沉淀B.用可见
- I prefer to have _______one ofthe two T-shirts _______some
- 亚洲、欧洲流经国家最多的国际性河流分别是A.阿姆河、多瑙河B.长江、莱茵河C.湄公河、多瑙河D.锡尔河、莱茵河
- 汶川地震后,某电视台法制频道在端午节组织发起“绿丝带行动”,号召市民为四川受灾的人们祈福.人们将绿丝带剪成小段,并用别针
- 回答有关人体代谢及调节的问题。 (1)下图表示血脂代谢及调节示意图,其中甲、乙、丙、丁分别代表不同的场所,字母代表物质,
- 某校男子足球队16名队员的年龄如下:17 17 18 18 16 18 17 15 18 18 17
- 已知,当时,有,则必有( ) A. B. C. D.
- ......