实验4-3 含氯消毒液性质、作用的探究 知识点题库
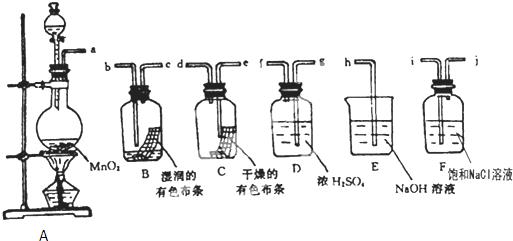
某兴趣小组拟利用如下图装置探究验证干燥的Cl2和潮湿的Cl2有无漂白性.
回答下列问题:
(1)A装置中的主要玻璃仪器有:导管、酒精灯、圆底烧瓶、 .
A装置中发生反应的化学方程式是 .
(2)按气体从左向右流向将各装置依次连接起来(填接口标号):a 接 , 接 , 接 , 接 , 接 .
(3)A装置中发生反应,产生Cl2后,从集气瓶B、C中有色布条的现象可得出的结论是 ;其中发生反应的化学方程式为 .
(4)F装置中饱和NaCl溶液作用为 .D装置中浓 H2SO4作用为 .
(5)烧杯E中发生反应的化学方程式为 .
(6)工业生产漂白粉的化学方程式
在反应中消耗2mol氯气,则转移了 mol电子.
(7)工业上可用氨与Cl2反应检验输送氯气的管道是否漏气,反应方程式如下:8NH3+3Cl2═6NH4Cl+N2 . 该反应中, 是还原剂;若反应中有1.5mol氧化剂参与反应,则发生转移的电子的物质的量为 mol,被氧化的物质有 mol.
①黄绿色 ②密度比空气大 ③有毒 ④较易液化 ⑤能溶解于水.
A | B | C | D | |
X | SO2 | Cl2 | NH3 | SO2 |
Y | H2S | CO2 | CO2 | Cl2 |
①二氧化硅是电子工业中常用的半导体材料
②氢氧化铝可用于治疗胃酸过多
③氯气与烧碱溶液或石灰乳反应都能得到含氯消毒剂
④天然气、石油和煤均属于不可再生能源
⑤用食醋清洗热水瓶中的水垢
⑥用纯碱溶液洗涤餐具上的油污
⑦用米汤检验含碘盐中的碘酸钾
⑧医疗上可用碳酸钡作x射线透视肠胃的内服药,是因为碳酸钡不溶于水
⑨某雨水样品放置一段时间后pH由4.68变为4.00,是因为水中溶解的CO2增多
⑩加碘食盐中添加碘酸钾而不用碘化钾,是因为碘酸钾能溶于水而碘化钾不溶于水.
-
(1) 工业上可用Cl2氧化NaClO2溶液制取ClO2 . 写出该反应的离子方程式.
-
(2) 某地污水中的有机污染物主要成分是三氯乙烯(C2HCl3),向此污水中加入KMnO4(高锰酸钾的还原产物为MnO2)溶液可将其中的三氯乙烯除去,氧化产物只有CO2 , 写出该反应的化学方程式.
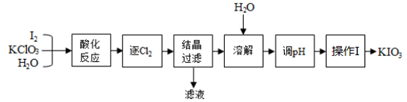
已知:“酸化反应”所得产物有KH(IO3)2、Cl2和KCl。
-
(1) KIO3所含的化学键有。
-
(2) 逐出的Cl2可用检验;“滤液”中的溶质主要是;“调pH”中所用的试剂是。
-
(3) 已知KIO3在水中的溶解度随温度升高而增大,则操作I包含的操作应该是、、过滤。
-
(4) 为测定“加碘食盐”中碘元素含量:①称取50.000g食盐,配成250mL溶液;②量取25.00mL溶液于锥形瓶中,加入足量KI,并用少量稀硫酸酸化,使KIO3与KI反应完全;③以淀粉为指示剂,用2.0×10-4mol/L的Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液体积为30.00mL。已知:KIO3+KI+H2SO4→K2SO4+I2+H2O(未配平),2Na2S2O3+I2→Na2S4O6+2NaI。测定过程中,所需仪器在使用前必须检查是否漏液的有。
-
(5) 判断滴定终点的依据是。
-
(6) 配平:KIO3+KI+H2SO4→K2SO4+I2+H2O
-
(7) 该食盐中碘元素的含量是mg/kg。
-
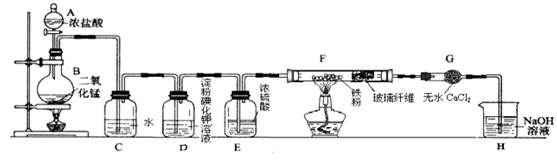
(1) 仪器A的名称是 ,实验中制备氯气的反应方程式为 。
-
(2) C中发生反应的化学方程式为 .若将干燥的有色布条放入C中,观察到的现象是 ,原因是 。
-
(3) 实验中观察到D溶液变蓝色,查资料得知淀粉碘化钾溶液是淀粉和碘化钾(KI)的混合溶液,写出D装置中发生反应的离子方程式。
-
(4) F中氯气与铁粉反应制备无水三氯化铁,查资料知该化合物呈棕红色、易吸水潮解, 100℃左右时升华.双通管F中玻璃纤维(不参与反应)的作用是 ;在F和H装置之间安装G装置的目的是。
-
(5) H中NaOH溶液的作用是 。
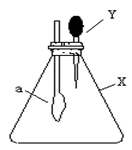
| X | Y | |
| A | HCl | 饱和食盐水 |
| B | H2 | 浓硫酸 |
| C | HCl | 2mol/L NaOH溶液 |
| D | Cl2 | 6mol/L NaOH 溶液 |
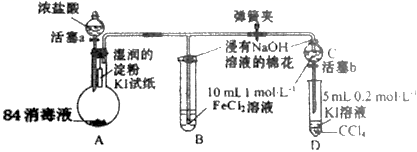
实验过程:
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸。
Ⅱ.当B和C 中的溶液都变为黄色时,夹紧弹簧夹。
Ⅲ.向B中加入一定量KSCN溶液,混合液显红色,一段时间后,B 中溶液红色加深,关闭活塞a。
Ⅳ……
-
(1) 盛浓盐酸溶液的仪器名称是;A中产生黄绿色气体,写出A中发生反应的离子方程式。
-
(2) 验证氯气的氧化性强于碘单质的实验现象是。
-
(3) B中溶液发生的离子方程式。
-
(4) 为验证Fe3+的氧化性强于碘单质,过程Ⅳ的操作和现象是,对应反应的离子方程式是。
-
(5) 浸有氢氧化钠溶液的棉花作用是。
-
(6) 过程Ⅲ实验的目的是。
 B .
B .  C .
C .  D .
D . 
-
(1)
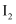 的一种制备方法如下图所示:
的一种制备方法如下图所示: 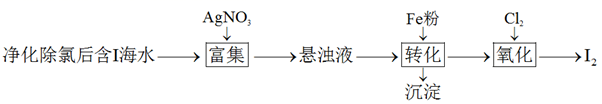
①加入
 粉进行转化反应的离子方程式为,生成的沉淀与硝酸反应,生成后可循环使用。
粉进行转化反应的离子方程式为,生成的沉淀与硝酸反应,生成后可循环使用。②通入
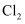 的过程中,若氧化产物只有一种,反应的化学方程式为;若反应物用量比
的过程中,若氧化产物只有一种,反应的化学方程式为;若反应物用量比 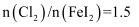 时,氧化产物为;当
时,氧化产物为;当 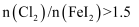 ,单质碘的收率会降低,原因是。
,单质碘的收率会降低,原因是。 -
(2) 以
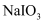 为原料制备
为原料制备 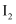 的方法是:先向
的方法是:先向 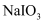 溶液中加入计量的
溶液中加入计量的  ,生成碘化物;再向混合溶液中加入
,生成碘化物;再向混合溶液中加入 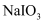 溶液,反应得到
溶液,反应得到 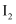 ,上述制备
,上述制备 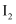 的总反应的离子方程式为。
的总反应的离子方程式为。
-
(3)
 溶液和
溶液和 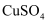 溶液混合可生成
溶液混合可生成 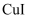 沉淀和
沉淀和 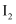 ,若生成
,若生成 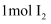 ,消耗的
,消耗的  至少为
至少为 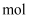 。
。 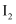 在
在  溶液中可发生反应
溶液中可发生反应  。实验室中使用过量的
。实验室中使用过量的  与
与 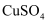 溶液反应后,过滤,滤液经水蒸气蒸馏可制得高纯碘。反应中加入过量
溶液反应后,过滤,滤液经水蒸气蒸馏可制得高纯碘。反应中加入过量  的原因是。
的原因是。
①钠在空气中燃烧生成淡黄色的氧化钠
②钠投入硫酸铜溶液中有红色固体产生
③氢气在氯气中燃烧产生苍白色烟雾
④铁丝在氯气中燃烧生成棕黄色的FeCl3
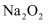 和
和 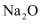 均可做供氧剂
B . 公共场所消毒所用的75%酒精过氧乙酸(
均可做供氧剂
B . 公共场所消毒所用的75%酒精过氧乙酸( 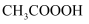 )均属于纯净物
C . “84”消毒液可有效杀灭“新冠病毒”,其有效成分是
)均属于纯净物
C . “84”消毒液可有效杀灭“新冠病毒”,其有效成分是 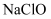 D . 医用口罩可以水洗后重复使用
D . 医用口罩可以水洗后重复使用
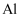 、
、 ),硬度大,密度小,抗腐蚀
B . 铁红(
),硬度大,密度小,抗腐蚀
B . 铁红( ),可用作红色油漆的颜料
C . 液氯(
),可用作红色油漆的颜料
C . 液氯( ),黄绿色气体,具有漂白性
D . 小苏打(
),黄绿色气体,具有漂白性
D . 小苏打( ),可用于治疗胃酸过多
),可用于治疗胃酸过多
-
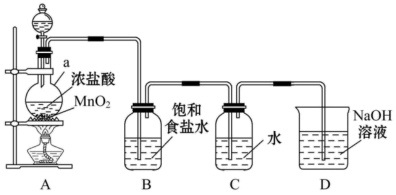
(1) 仪器a的名称是。
-
(2) 实验室制取氯气的化学方程式是,该反应中氧化剂是,装置B的作用是除去氯气中混有的。
-
(3) 装置D的作用是,反应的离子方程式为。
- 双曲线2x2-y2=k的焦距是6,求k的值.
- --The film “Avatar”(阿凡达)_______ on the TV next month.--Reall
- “神舟六号”发射时,“长征二号”捆绑式火箭尾部的火焰如果直接喷到发射台,发射架要熔化,为了保护发射架,就在发射台底建了一
- 如果实数x,y满足不等式组目标函数z=kx+y的最大值为12,最小值为3,那么实数k的值为 A.2 B.-2 C.1
- 有关亚洲位置和范围的叙述,正确的是( ) A.亚洲是世界上跨经度最少的一洲 B.亚洲是世界上跨
- 阅读下面的文字,回答下列题。 通感得“道” “妙”,在中国古典哲学、文论、画论、书论中是一重要范畴,可以称之为中国古典文
- 下列函数中,既是偶函数又在(0,+∞)上是单调递增的是A.y=2|x+1|
- “为什么现代科学只在欧洲而没有在中国文明(或印度文明)中发展起来?……为什么在公元前1世纪至公元15世纪之间,中国文明
- 建设社会主义精神文明的中心环节是( )A.努力提升我国综合国力B.加强教育、科学、文化建设C.提高公民基本科学素养D.
- 把下面的一句话改成设问句。(2分)英模的行为不是一时的冲动,而是崇高人格的长期养成,强烈社会责任感的驱使,社会正气的集中
- 学者李涛在《美国的梦想》一书中写道:“(18世纪)欧洲的思想之花,终于在美国结出了果子。”对此理解较为准确的是 () A
- P是△ABC内一点,,则△ABC与△ABP 的面积之比为( ) A.2 B.3
- I’d been 16 for six days and was already prepared to deal wi
- (2分)一定温度下,将一瓶接近饱和的KNO3溶液变为饱和溶液,且不改变溶液的浓度的方法是________________
- 计算( ). A. B. C. D.
- 把盛有碎冰块的大试管插入烧杯里的碎冰块中,用酒精灯在烧杯底部慢慢加热,如图所示。当烧杯中的冰块大部分熔化时,试管中的冰:
- 我国使用“长征3号甲”运载火箭的动力是由高氯酸铵(NH4ClO4)分解所提供的,反 应方程式为2NH4ClO4N2
- —Are you going to have a holiday this year? —I'd love to.
- 甲、乙、丙、丁四人。甲是某国有控股企业的总工程师,并有一项技术专利卖给该企业;乙是一日本在中国独资企业的职工;丙是某农贸
- 关于西北地区的叙述,正确的是( ) A、阿尔泰山位于塔里木盆地和准噶尔盆地之间 B、塔里木盆地是天山断层陷落而形成的



