第三单元 物质的检测 知识点题库
选项 | 待提纯的物质 | 除杂的试剂 | 操作方法 |
A | NO2(NO) | O2 | 收集气体 |
B | CO2(HCl) | 饱和Na2CO3溶液 | 洗气 |
C | FeCl2溶液(FeCl3) | 足量铁粉 | 过滤 |
D | KCl溶液(MgCl2) | NaOH溶液 | 过滤 |

-
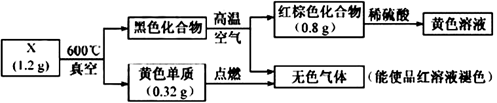
(1) X中的非金属元素是。
-
(2) 黑色化合物高温空气红棕色化合物的化学方程式是。
-
(3) 设计实验方案检验黄色溶液中的金属阳离子。
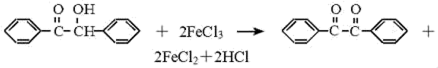
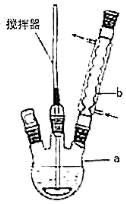
在反应装置中,加入原料及溶剂,搅拌下加热回流。反应结束后加热煮沸,冷却后即有二苯基乙二酮粗产品析出,用70%乙醇水溶 液重结晶提纯。重结晶过程:
加热溶解→活性炭脱色→趁热过滤→冷却结晶→抽滤→洗涤→干燥
请回答下列问题:
-
(1) 写出装置图中玻璃仪器的名称:b。
-
(2) 趁热过滤后,滤液冷却结晶。一般情况下,下列哪些因素有利于得到较大的晶体:。
A.缓慢冷却溶液 B.溶液浓度较高 C.溶质溶解度较小 D.缓慢蒸发溶剂
如果溶液中发生过饱和现象,可采用等方法促进晶体析出。
-
(3) 抽滤所用的滤纸应略(填“大于”或“小于”)布氏漏斗内径,将全部小孔盖住。 烧杯中的二苯基乙二酮晶体转入布氏漏斗时,杯壁上往往还粘有少量晶体,需选用液体将杯壁上的晶体冲洗下来后转入布氏漏斗,下列液体最合适的是。
A.无水乙醇 B.饱和NaCl溶液 C.70%乙醇水溶液 D.滤液
-
(4) 抽滤过程中要及时观察吸滤瓶内液面高度,当快达到支管口位置时应进行的操作为。
-
(5) 上述重结晶过程中的哪一步操作除去了不溶性杂质:。
-
(6) 某同学采用薄层色谱(原理和操作与纸层析类同)跟踪反应进程,分别在反应开始、回流15min、30min、45min和60min时,用毛细管取样、点样、薄层色谱展开后的斑点如图所示。该实验条件下比较合适的回流时间是_____。
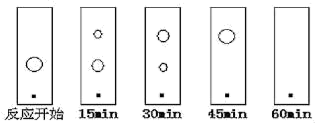 A . 15min B . 30min C . 45min D . 60min
A . 15min B . 30min C . 45min D . 60min
①验证蛋壳能否溶于酸②检验白酒中是否含有甲醇③鉴别食盐和小苏打④检验自来水中是否含有氯离子
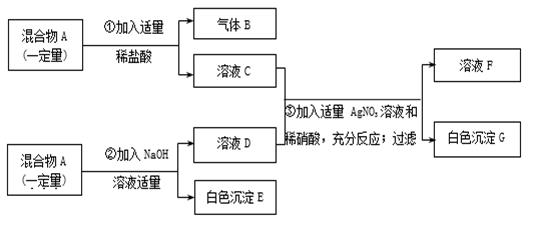
试根据实验过程和发生的现象做出判断,填写以下空白:
-
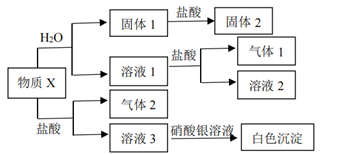
(1) 气体B的化学式为。
-
(2) 在混合物A里,上述四物质中肯定不存在的物质是(写化学式)。
-
(3) 在溶液F中,主要含有种溶质,其中大量含有的酸根离子符号是。
-
(4) 写出1个生成白色沉淀G的化学方程式:。
 =CO2↑+ H2O
=CO2↑+ H2O
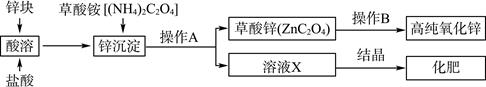
-
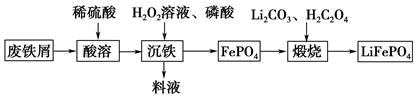
(1) “酸溶”所达到的目的是将锌块转化为可溶于水的(填产物名称)。
-
(2) 由草酸铵的化学式推测草酸的化学式为。
-
(3) “锌沉淀”过程中发生反应的离子方程式为。
-
(4) “操作A”的名称是;在实验室完成其过程需要用的玻璃仪器有。
-
(5) “操作B”是高温灼烧,该过程除生成氧化锌外,还有两种气态碳氧化物生成,则草酸锌分解的化学方程式为。
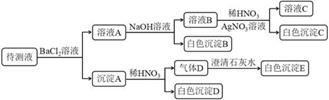
注:①稀硝酸具有强氧化性;②每步实验所加试剂均过量。下列说法不正确的是( )
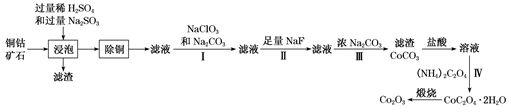
回答下列问题:
-
(1) “浸泡”过程中,钴(III)可转化为CoSO4 , 写出该转化的化学方程式:。
-
(2) “除铜”若选用MnS,计算常温下该“除铜”反应的平衡常数K=。[保留2位有效数字;已知常温下Ksp(MnS)=2.5×10–13 , Ksp(CuS)=1.3×10–36]
-
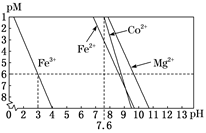
(3) ①步骤I中加入NaClO3反应的离子方程式为。
②常温下,溶液中金属离子(Mn+)的pM[pM=–lgc(Mn+)]随溶液pH变化关系如图所示,设加入NaClO3后,溶液中的c(CO2+)为0.1mol•L–1 , 依据如图分析,步骤I中加入Na2CO3调整溶液pH范围为。[当c(Mn+)≤10–6 mol•L–1 , 即认为该金属离子沉淀完全]
-
(4) 步骤II中加入足量NaF的目的是。
-
(5) 过滤出的CoC2O4•2H2O固体经洗涤后,证明固体已洗净的操作为。
-
(6) 若某工厂用m1kg该铜钴矿石制备了m2kgCo2O3 , 假设产率为a,则该矿石中钴元素的百分含量为。

-
(1) 仪器P的名称是,B装置中试剂是,C中浓硫酸的作用是。
-
(2) 写出装置A烧瓶内发生反应的化学方程式:。
-
(3) 实验室制备ClO2的原理是:2NaClO2+Cl2=2ClO2+2NaCl。E中盛有CCl4 , 其作用是,ClO2和Cl2作氧化剂还原产物均为Cl- , 含等量氯元素的ClO2和Cl2其得电子数目之比为。
-
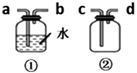
(4) F为ClO2收集装置,应选用的装置是(填序号)。
-
(5) 亚氯酸钠(NaClO2)也具有强氧化性,常用“间接碘量法”测定某NaClO2·3H2O样品(杂质与I-不发生反应)的纯度:取一定质量样品配成VmL溶液,加入足量KI固体和适量稀H2SO4 , 再滴加几滴做指示剂,(已知:
 +4I-+4H+=2H2O+2I2+Cl-),然后用cmol·L-1Na2S2O3标准溶液滴定,判断滴定终点的方法为(已知:I2+2
+4I-+4H+=2H2O+2I2+Cl-),然后用cmol·L-1Na2S2O3标准溶液滴定,判断滴定终点的方法为(已知:I2+2  =
=  +2I-)。
+2I-)。
 2LiFePO4+3CO2↑+H2O
D . 煅烧过程中,每消耗1molH2C2O4 , 转移电子4mol
2LiFePO4+3CO2↑+H2O
D . 煅烧过程中,每消耗1molH2C2O4 , 转移电子4mol
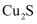 , 含
, 含 及少量
及少量 )为原料制备碱式碳酸铜,工业流程如图:
)为原料制备碱式碳酸铜,工业流程如图: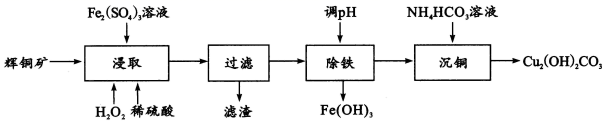
回答下列问题:
-
(1) 滤渣可能含S、(填化学式)。
-
(2) ①“浸取”时能提高辉铜矿
 浸取率的措施有(填2条)。
浸取率的措施有(填2条)。②某小组测得
 浸取率随
浸取率随 浓度及温度影响的变化曲线如图:
浓度及温度影响的变化曲线如图: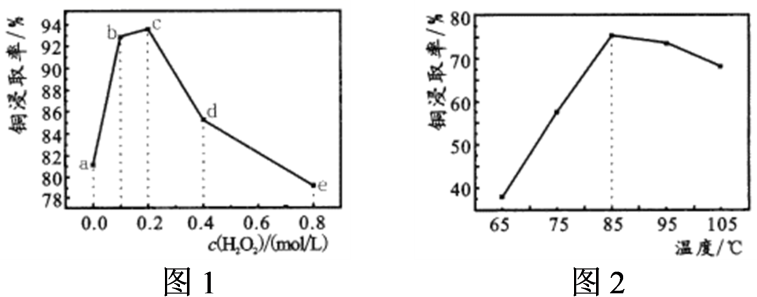
由图1可知
 适宜的浓度范围为;浸取时
适宜的浓度范围为;浸取时 也起到了氧化辉铜矿的作用,证据可由图1中的点(填字母序号)分析,该反应的离子方程式为;图2中高于85℃时
也起到了氧化辉铜矿的作用,证据可由图1中的点(填字母序号)分析,该反应的离子方程式为;图2中高于85℃时 浸取率下降的原因是。
浸取率下降的原因是。 -
(3) “除铁”步骤调pH可加入试剂(填选项字母);
a.氨气 b.
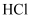 c.
c.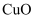 d.
d.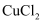
常温下,“过滤”后的滤液中
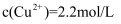 , 则“除铁”步骤调pH应小于[常温下
, 则“除铁”步骤调pH应小于[常温下 ]。
]。
- 下面这首诗形象地写出了诗歌的特点,请你用自己的话概括出其中的两点。 一首诗北村 诗应该是能吟诵的/能上口上心/能在饥饿时
- 四棱锥P-ABCD中,底面ABCD为菱形,且, 侧面PAD是正三角形,其所在的平面垂直于底面ABCD, 点G为AD的中点
- 2009年5月,世界卫生组织召开成员国会议研究防控甲型HIN1流感的对策。中国政府表示,在做好国内疫情防控的同时,将加强
- 《海国图志》中记载:“(某国)都城有公会所,内分两所,一日爵房,一日乡绅房。爵房者,有爵位贵人及耶稣教师处之;乡绅房者,
- 定温度下,向饱和NaOH溶液中投入一小块金属钠,充分反应后恢复到原来温度。下列叙述中,不合理的是()A.NaOH溶液浓度
- 关于我国人口分布情况的错误叙述是( ) A.我国人口分布不均 B.我国人口分布是东部地区人口密度大,西部
- 如图5所示,mA>mB,设地面对A的支持力为FN,绳子对A的拉力为F1,地面对A的摩擦力为F2,若水平方向用力F拉
- 在含有 Cl-、Br-、I-的强酸性混合液中,若要使 Br-、I-氧化成Br2和 I2,而不使 Cl-氧化,应选用的试剂
- 人们认识世界,改造世界,都需要智慧,学习哲学可以使人们拥有智慧。哲学的智慧产生于( ) A.人的头脑 B.人
- 2.下列各组词语中,没有错别字的一组是( ) A.告诫 披肝沥胆 徇私舞敝 莫逆之交 B.渎职
- 与善人居,如入芝兰之宣,久而不闻其香,即与之化矣。与不善人居,如入鲍鱼之肆(店铺),久而不闻其臭,亦与之化矣。丹
- 补写出下列名句名篇中的空缺部分。 23.淇则有岸, 。总角之宴, 。 24.举酒属客,
- Learning a second language Nowadays,more and more people
- (2011辽宁沈阳,8,3分)小明乘出租车去体育场,有两条路线可供选择:路线一的全程是25千米,但交通比较拥堵;路线二的
- 给试管中的液体加热时,若出现试管破裂的现象,其原因不可能是() A.加热前试管外壁有水 B.加热不均匀,局部
- Though he had often made his sister _____, today, he was mad
- 在同温同压下,是8 g SO2所占体积2倍的氧气的质量是( ) A.8 g B.16 g
- 在荠菜胚的发育过程中,从周围组织中吸收并运送营养物质供球状胚体发育的结构是( ) A.胚芽
- 有些药物常被封装在淀粉制成的胶囊中服用,以避免对胃产生刺激。从淀粉在消化道内的消化特点来看,其原因是( ) A.胃能
- 2003年10月15日我国成功发射了第一艘载人航天飞船——“神舟”五号,2005年10月12日“神舟”六号飞船成功发射,



