第三单元 物质的检测 知识点题库
①称取10.0g试样,加水溶解,配成250mL试样溶液
②用酸式滴定管分别量取25.00mL试样溶液两份于锥形瓶中
③第一份溶液中加2~3滴指示剂,用0.2500mol•L﹣1NaOH溶液滴定,消耗NaOH溶液20.00mL
④第二份溶液用0.1000mol•L﹣1的酸性高锰酸钾溶液滴定,消耗高锰酸钾溶液16.00mL
回答下列问题:

-
(1) 写出NaHC2O4溶液与NaOH溶液反应的离子方程式.
-
(2) 步骤①配制试样溶液时所需要的玻璃仪器有烧杯、玻璃棒、量筒、.
-
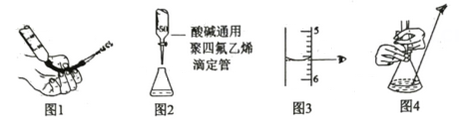
(3) 步骤③若滴定终点时溶液的pH=8.3,则选择的指示剂为.若用某部分刻度模糊不清的50mL滴定管进行实验,当滴定管中的液面处于如图所示的刻度处,则管内液体的体积(填代号).
a.等于23.60mL b.等于27.60mL c.小于23.60mL d.大于27.60mL
-
(4) 滴定时边滴边摇动锥形瓶,眼睛应观察.
-
(5) 完成并配平下列离子方程式:
C2O42﹣+MnO4﹣+H+=CO2↑+Mn2++
-
(6) 步骤③中,高锰酸钾溶液应装在 滴定管里;该步判断滴定终点的方法是.
-
(7) 试样中Na2SO4的质量分数为(保留3位有效数字).
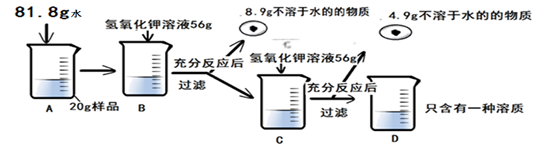
-
(1) 上述实验过程中发生反应的化学方程式为。
-
(2) 根据已知条件列出求解C烧杯中参加反应的硫酸铜质量(X)的比例式。
-
(3) 配制上述实验所用的氢氧化钾溶液,需要质量分数为40%的氢氧化钾溶液的质量为。
-
(4) 样品中硫酸铜的质量分数为。
-
(5) D烧杯溶液中溶质的质量分数为。
-
(6) 若用湿法冶金的方法冶炼出100kg含杂质4%的铜,需要这种硫酸铜的质量为多少?(写出计算过程)
 、Cl-、
、Cl-、  、
、 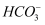 等离子。某同学收集雾霾样品,经必要的预处理配成试样溶液,设计如下实验探究其中含有的离子。
等离子。某同学收集雾霾样品,经必要的预处理配成试样溶液,设计如下实验探究其中含有的离子。
①取一定体积的溶液, 加人足量BaCl2溶液,产生白色沉淀,继续滴加足量盐酸,沉淀不溶解,同时得到无色气体。
②另取一定体积的溶液,加人足量NaOH溶液,产生白色沉淀,继续滴加足量稀盐酸,沉淀全部溶解。下列判断错误的是( )
 C . 肯定含有Mg2+、
C . 肯定含有Mg2+、  、
、 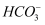 D . 一定不存在Ba2+、Fe3+、Cl-
D . 一定不存在Ba2+、Fe3+、Cl-
-
(1) I.固体化合物X由三种元素组成。某学习小组进行了如下实验:
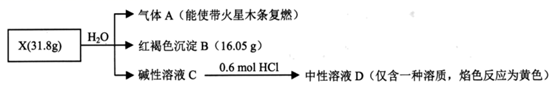
请回答:
组成X的三种元素是,X的化学式为。
-
(2) 固体X与水反应的化学方程式是。
-
(3) 固体X可由两种常见的氧化物在气体A氛围中加热制得,该反应的化学方程式是。
-
(4) II.水合肼(N2H4·H2O)是一种强还原性的碱性液体,是一种用途广泛的化工原料,实验室用下图装置制备(部分装置省略)。已知:3NaClO=2NaCl+NaClO3
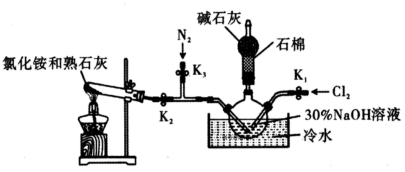
步骤1:关闭K2、K3 , 打开K1 , 制备NaClO。
步骤2:操作A,制备N2H4·H2O。
NH3与NaClO反应生成N2H4·H2O的化学方程式为。
-
(5) 步骤2中操作A为。
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向淀粉溶液中滴加稀硫酸,加热,再加碘水 | 溶液变蓝 | 淀粉没有水解 |
| B | 将 | | 有乙烯生成 |
| C | 向 | 产生砖红色沉淀 | 葡萄糖具有还原性 |
| D | 将乙醇加入浓硫酸中,快速加热到170℃,将产生的气体通入溴水 | 溴水褪色 | 不能证明有乙烯生成 |

-
(1) 步骤①中为了提高酸浸的速率可采取的措施有。
-
(2) FeTiO3与稀硫酸反应的离子方程式为。
-
(3) 步骤②③④中,均需进行的操作是(填操作名称),若在实验室中进行步骤⑤操作,需要的硅酸盐材质的仪器有酒精灯、泥三角、。
-
(4) 步骤④中选择热水的原因是。
-
(5) 步骤③中实现混合物的分离是利用物质的(填字母序号)。
a 熔、沸点差异 b 溶解性差异 c 氧化性、还原性差异
-
(6) 工业上用4.0吨钛铁矿制得1. 6吨的二氧化钛,则钛铁矿中钛元素的质量分数是。(假设生产过程中钛没有损失)
 的合成路线如下:
的合成路线如下: 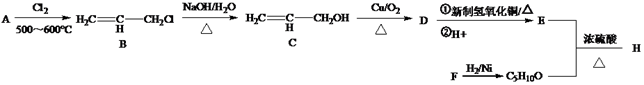 已知:①F的分子式
已知:①F的分子式  且核磁共振氢谱显示F只有两组峰,且峰面积之比为
且核磁共振氢谱显示F只有两组峰,且峰面积之比为 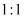 ;
;
② 
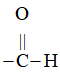
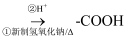
回答下列问题:
-
(1) A的系统命名为,
 的反应类型为。
的反应类型为。
-
(2) F的结构简式为,
 的反应类型为。
的反应类型为。
-
(3) D含有官能团的名称为,
-
(4)
 的化学方程式为。
的化学方程式为。
-
(5) 下列有关化合物E的说法正确的是(填标号)。
a.与
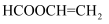 互为同分异构体
互为同分异构体b.在一定条件可发生加聚反应,所得聚合物为纯净物
c.同系物中:碳原子数越多,支链数越多,沸点越高
d.分子中所有的碳原子一定在同一平面上
-
(6) 有机化合物M与G互为同分异构体(不考虑立体异构体),则:
①M中含有碳氧双键的结构有种。
②M中含有羟基和碳碳双键的结构有种(形成碳碳双键的碳原子不与羟基相连)。
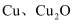 组成的混合物,某研究性学习小组为了探究其组成情况,取
组成的混合物,某研究性学习小组为了探究其组成情况,取 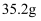 该混合物加入
该混合物加入 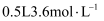 的稀硝酸中,固体物质完全反应,溶液中铜元素均为
的稀硝酸中,固体物质完全反应,溶液中铜元素均为 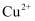 ,且生成
,且生成 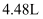 (标准状况)的
(标准状况)的  。向所得溶液中加入
。向所得溶液中加入 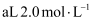 的
的  溶液,恰好使溶液中的
溶液,恰好使溶液中的 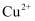 沉淀完全。
沉淀完全。
-
(1)
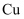 与稀硝酸反应的离子方程式为;
与稀硝酸反应的离子方程式为;
-
(2)
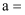 L。
L。
-
(3) 求混合物中
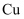 的质量分数?(没有计算过程不得分)
的质量分数?(没有计算过程不得分)
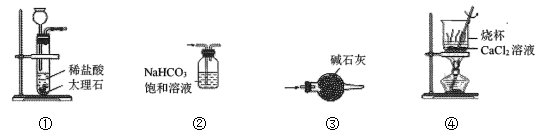
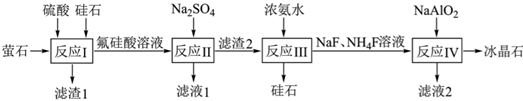
已知:无水氟硅酸(H2SiF6)为易溶于水、不稳定的强酸;滤渣2的主要成分为Na2SiF6。
下列说法错误的是( )
-
(1) 合成该物质的步骤如下:
步骤1:配制0.5mol·L-1 MgSO4溶液和0.5mol·L-1 NH4HCO3溶液。
步骤2:用量筒量取500mL NH4HCO3溶液于1000mL三颈烧瓶中,开启搅拌器。温度控制在50℃。
步骤3:将250mL MgSO4溶液逐滴加入NH4HCO3溶液中,1min内滴加完后,用氨水调节溶液pH到9.5。
步骤4:放置1h后,过滤,洗涤。
步骤5:在40℃的真空干燥箱中干燥10h,得碳酸镁晶须产品(MgCO3·nH2O n=1~5)。
①步骤2控制温度在50℃,较好的加热方法是。
②步骤3生成MgCO3·nH2O沉淀的化学方程式为。
③步骤4检验沉淀是否洗涤干净的方法是。
-
(2) 测定生成的MgCO3·nH2O中的n值。
称量1.000碳酸镁晶须,放入如图所示的广口瓶中加入适量水,并滴入稀硫酸与晶须反应,生成的CO2被NaOH溶液吸收,在室温下反应4~5h,反应后期将温度升到30℃,最后将烧杯中的溶液用已知浓度的盐酸滴定,测得CO2的总量;重复上述操作2次。
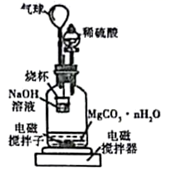
①图中气球的作用是。
②上述反应后期要升温到30℃,主要目的是。
③测得每7.8000g碳酸镁晶须产生标准状况下CO2为1.12L,则n值为。
-
(3) 碳酸镁晶须可由菱镁矿获得,为测定某菱镁矿(主要成分是碳酸镁,含少量碳酸亚铁、二氧化硅)中铁的含量,在实验室分别称取12.5g菱镁矿样品溶于过量的稀硫酸并完全转移到锥形瓶中,加入指示剂,用0.010mol/L H2O2溶液进行滴定。平行测定四组。消耗H2O2溶液的体积数据如表所示。
实验编号
1
2
3
4
消耗H2O2溶液体积/mL
15.00
15.02
15.62
14.98
①H2O2溶液应装在(填“酸式”或“碱式”)滴定管中。
②根据表中数据,可计算出菱镁矿中铁元素的质量分数为 %(保留小数点后两位)。
-
(1) 检验葡萄汁含葡萄糖的方法是:向其中加碱调至碱性,再加入新制备的Cu(OH)2 , 加热,其现象是。
-
(2) 葡萄在酿酒过程中,葡萄糖转化为酒精的过程如下,补充完成下列化学方程式。
C6H12O6(葡萄糖)
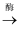 2+2C2H5OH
2+2C2H5OH -
(3) 葡萄酒密封储存过程中生成了有香味的酯,酯也可以通过化学实验来制备。实验室用右图所示装置制备乙酸乙酯:
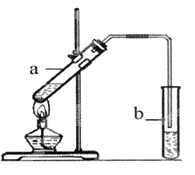
①试管a中生成乙酸乙酯的化学方程式是 。
②实验开始时,试管b中的导管不伸入液面下的原因是。
③若分离出试管b中生成的乙酸乙酯,需要用到的仪器是(填序号)。
a. 漏斗 b. 分液漏斗 c. 长颈漏斗
-
(4) 某有机物的结构简式为HOOC—CH=CHOH。验证该有机物中含有-COOH官能团常采用的方法是,产生的现象为。
选项 | 实验操作 | 现象 | 结论 |
A | 向某溶液中加入稀盐酸酸化,再加入BaCl2溶液 | 酸化后溶液中无现象,再加溶液后观察到有白色沉淀生成 | 该溶液中存在SO |
B | 向苯酚浊液中加入Na2CO3溶液 | 溶液变澄清 | 酸性:苯酚>碳酸 |
C | 用洁净的铂丝蘸取某溶液进行焰色反应 | 焰色呈黄色 | 该溶液为钠盐溶液 |
D | 向FeCl2溶液中滴加KSCN溶液 | 溶液变红 | FeCl2已完全变质 |
- 12.2003年诺贝尔生物学奖授予美国的两位科学家,以表彰他们在细胞膜通道(水通道和离子通道)方面做出的贡献。这两位科学
- 某市个别地方、个别单位、个别人员的“庸、懒、散”问题影响了党的声望和政府公信力,损害了干部队伍的整体形象,必须要继续推进
- Excuse me, but can you tell me ___________? A. where can I
- 下列词语中注音的字,读音全都正确的一组是 ( ) A、落叶(luò) 落(lào)枕 萎靡(mí) 相(
- 如图所示电路,断开电键S时,电压表示数为6 V,电流表示数为0.5 A,电源电压为9 V.由此可知电阻R1=______
- 2015年3月5日,国务院总理李克强在《政府工作报告》指出:大道至简,有权不可任性。要加大简政放权、放管结合改革力度。今
- This necklace is beautiful but it doesn’t _____ the color of
- 下面是生物兴趣小组同学探究某些条件与大豆种子萌发关系的实验。 (一)实验步骤: ①取三个无色透明的玻璃杯,分别标记A、B
- 如图,AD是⊙O的直径,AB为⊙O 的弦,OP⊥AD,OP与AB的延长线交于点P.点C在OP上,且BC=PC. (1)求
- 将固体NH4I置于密闭容器中,在某温度下发生下列反应:NH4I(s)NH3(g)+HI(g) 2HI(g)H2(g)+I
- 1912年到1919年中国民族工业获得短暂发展,其原因有( ) ①民族资产阶级倡导实业救国 ②帝国主义
- 实验室欲配制0.5 mol/L的NaOH溶液500 mL有以下仪器:①烧杯②100 mL量筒③1000mL容量瓶④500
- 某学者写道:“衰落是一个容易使人上当的词,因为它包含了两个相去的 概念:一是外部力量的减弱,一是内部力量的衰败……拿意大
- 豌豆高茎对矮茎为显性,现在有高茎豌豆进行自交,后代既有高茎又有矮茎,比例为3:1,将后代中全部高茎豌豆再进行自交,则所有
- 先化简,再求值: ,其中x=3.
- 右图为日光灯的结构示意图,若按图示的电路连接,关于日光灯发光的情况,下列说法正确的是( ) A.S1接通,S2
- 已知反应+6I-+6H+====R-+3I2+3H2O,则R元素原子的最外层电子数为( ) A.5个
- 用分子的知识解释下列现象,正确的是 A.缉毒犬能根据气味发现毒品,是由于分子不断运动 B.铁丝在空
- He had an expression of resentment(不高兴), as if Martin___a fo
- 警察常从案发现场的人体气味来获取有用线索。人体气味的成分中含有以下化合物:①辛酸;②壬酸;③环十二醇;④5,9十一烷酸内
 溶液中
溶液中
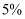
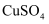 溶液,再加入
溶液,再加入  离子
离子


