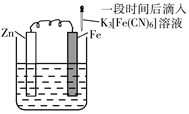
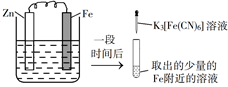
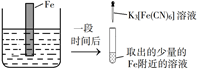
第一单元 从实验走进化学 知识点题库
提出猜想
问题1:在周期表中,铜与铝的位置很接近,铜不如铝活泼,氢氧化铝具有两性,氢氧化铜也有两性吗?
问题2:铁和铜都有变价,一般情况下,正二价铁的稳定性小于正三价的铁,正一价铜的稳定性也小于正二价的铜吗?
问题3:氧化铜有氧化性,能被H2、CO还原,它也能被氮的某种气态氢化物还原吗?
实验探究
-
(1) I.解决问题1
a.需用到的药品除1mol•L﹣1CuSO4溶液、稀硫酸外还需(填试剂的化学式)溶液.
b.用胆矾晶体配制1mol•L﹣1CuSO4溶液250mL,选用的仪器除烧杯、托盘天平、药匙、
玻璃棒、胶头滴管外,还有(填仪器名称).
c.为达到实验目的,请你补全实验内容和步骤:
①用CuSO4溶液制备Cu(OH)2;
②.
-
(2) Ⅱ.解决问题2
取一定量I中制备获得的氢氧化铜固体于坩埚中灼烧,当温度达到80~100℃得到黑色固体粉末;继续加热至1000℃以上,黑色粉末全部变成红色粉末氧化亚铜;取适量红色氧化亚铜粉末于洁净试管中,加入过量的稀硫酸(或盐酸),得到蓝色溶液,同时观察到试管底部还有红色固体存在.根据以上实验现象回答问题.
a.写出氧化亚铜与稀硫酸(或盐酸)反应的离子方程式:.
b.从实验Ⅱ可得出的结论是在高温下正一价铜比正二价铜(填稳定或不稳定),
溶液中正一价铜比正二价铜(填稳定或不稳定).
-
(3) Ⅲ.解决问题3
设计如下装置(夹持装置未画出):
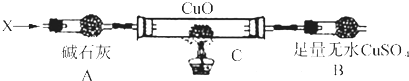
当氮的某种气态氢化物(X)缓缓通过灼热的氧化铜时,观察到氧化铜由黑色变成了红色,无水硫酸铜变成蓝色,生成物中还有一种无污染的单质气体Y;将X通入灼热的CuO燃烧管完全反应后,消耗0.01mol X,测得B装置增重0.36g,并收集到0.28g气体Y.
a.仪器A的名称是.
b.X的化学式为.
 处,手持试管夹长柄末端,进行加热
C . 制备乙酸乙酯时,将乙醇和乙酸依次加入到浓硫酸中
D . 把玻管插入橡胶塞孔时,用厚布护手,紧握用水湿润的玻管插入端,缓慢旋进塞孔中
处,手持试管夹长柄末端,进行加热
C . 制备乙酸乙酯时,将乙醇和乙酸依次加入到浓硫酸中
D . 把玻管插入橡胶塞孔时,用厚布护手,紧握用水湿润的玻管插入端,缓慢旋进塞孔中
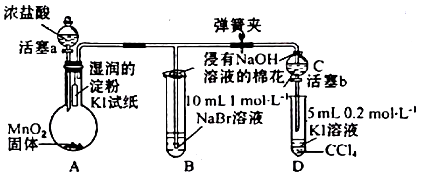
实验过程;
I.打开弹簧夹,打开活塞a,清加浓盐酸.
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹.
Ⅲ.当B中溶液由黄色变为棕色时,关闭活塞a.
Ⅳ…
-
(1) A中产生的是黄绿色气体,其离子方程式为,在该反应中浓盐酸表现了性.
-
(2) 验证氯气的氧化性强于碘的实验现象是.
-
(3) B中溶液发生反应的离子方程式是.
-
(4) 为验证溴的氧化性强于碘,过程Ⅳ的操作和现象是.
-
(5) 浸有NaOH溶液的棉花作用是;离子方程式为.
-
(6) 氯、溴、碘单质的氧化性逐渐减弱的原因:同主族元素从上到下,得电子能力逐渐减弱.
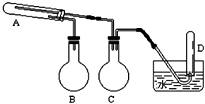
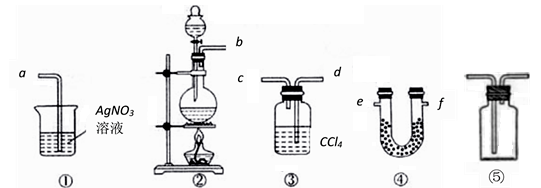
-
(1) 根据甲同学的意图,连接相应的装置,接口顺序为:b接,接,接a。
-
(2) 在连接好装置之后实验开始之前必须要进行的一项操作是:。
-
(3) U形管中所盛试剂的化学式为;装置③中CCl4的作用是。
-
(4) 乙同学认为甲同学实验有缺陷,不能证明最终通入AgNO3溶液中的气体只有一种。为了确保实验结论的可靠性,证明最终通入AgNO3溶液的气体只有一种,乙同学提出在某两个装置之
间再加装置⑤,你认为装置⑤应加在之间(填装置序号),瓶中可以放入。
-
(5) 若在装置完好的前提下,用浓度为10mol/L的浓盐酸600ml与过量的的MnO2反应,最终生成的氯气1.5mol(填大于、小于或等于),其主要原因是,可以通过向反应后的溶液中加入来证明上述结论。
A.锌粒
B.氢氧化钠溶液
C.硝酸酸化的硝酸银溶液
D.碳酸钠溶液
| ① | ② | ③ |
| | | |
| 在Fe表面生成蓝色沉淀 | 试管内无明显变化 | 试管内生成蓝色沉淀 |
下列说法不正确的是( )
 B .
B . 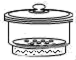 D .
D . 
|
选项 |
实 验 |
现 象 |
|
A |
向氢氧化钠溶液中滴加FeCl3饱和溶液 |
有氢氧化铁胶体产生 |
|
B |
在酒精灯上加热铝箔 |
铝箔熔化,失去光泽,熔化的铝滴落下来 |
|
C |
向滴有酚酞的溶液中加入足量Na2O2粉末 |
溶液变红 |
|
D |
加热放在坩埚中的小块钠 |
钠先熔化成光亮的小球,燃烧时火焰为黄色,燃烧后生成淡黄色固体 |
 B .
B . 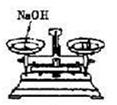 C .
C . 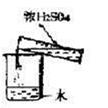 D .
D . 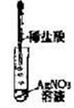
-
(1) 若要预测NaNO2的化学性质和变化,依据所学知识我们一般先从和两个角度进行预测。
-
(2) NaNO2中N元素的化合价为。在酸性条件下,可将KI转变为I2 , 自身转化为NO,该过程的离子反应方程式为,该实验事实证明NaNO2具有性。
-
(3) 已知NaNO2在空气中暴露会生成硝酸钠,反应的化学方程式为,该事实证明NaNO2具有性。
-
(4) 实验室常用NaNO2溶液与NH4Cl溶液反应来制取N2。反应原理为:NaNO2+NH4Cl
 NaCl+N2↑+2H2O,请选择合适的制气装置________(填序号)。
A .
NaCl+N2↑+2H2O,请选择合适的制气装置________(填序号)。
A .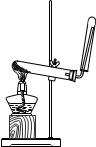 B .
B . 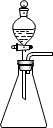 C .
C . 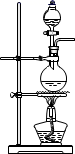 D .
D . 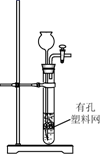
-
(5) 误食NaNO2会导致血红蛋白中Fe2+转化为Fe3+而中毒,依据所学化学知识,写出一条合理的解毒方案。
-
(1) 二氧化硫的水溶液
 易溶于水,常温常压下溶解度为1:40,溶于水生成
易溶于水,常温常压下溶解度为1:40,溶于水生成 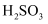 。已知
。已知 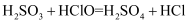 ,欲验证酸性:
,欲验证酸性:  ,设计以下实验达到目的(部分夹持装置已省略)。装置图中
,设计以下实验达到目的(部分夹持装置已省略)。装置图中  处发生的反应的方程式为,装置
处发生的反应的方程式为,装置 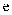 的作用是。能证明
的作用是。能证明 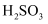 的酸性强于
的酸性强于 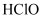 的实验现象为。
的实验现象为。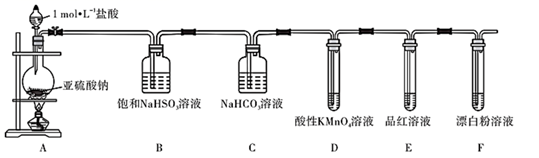
-
(2) ①请设计简单实验方案比较室温下
 溶液中
溶液中 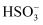 的电离平衡常数
的电离平衡常数  与水解平衡常数
与水解平衡常数  的相对大小:。
的相对大小:。 ②
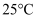 时,
时, 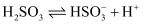 的电离常数
的电离常数  ,则该温度下
,则该温度下 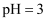 、
、 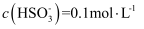 的
的  溶液中
溶液中  。
。 -
(3) 亚硫酰氯(俗称氯化亚砜,
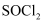 )是一种液态化合物,沸点
)是一种液态化合物,沸点 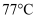 ,在农药、制药行业、有机合成等领域用途广泛。
,在农药、制药行业、有机合成等领域用途广泛。 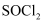 遇水剧烈反应,液面上产生白雾,并伴有刺激性气味的气体产生。蒸干
遇水剧烈反应,液面上产生白雾,并伴有刺激性气味的气体产生。蒸干  溶液不能得到无水
溶液不能得到无水  ,使
,使 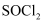 与
与  混合加热可得到无水
混合加热可得到无水  ,试解释原因:。
,试解释原因:。
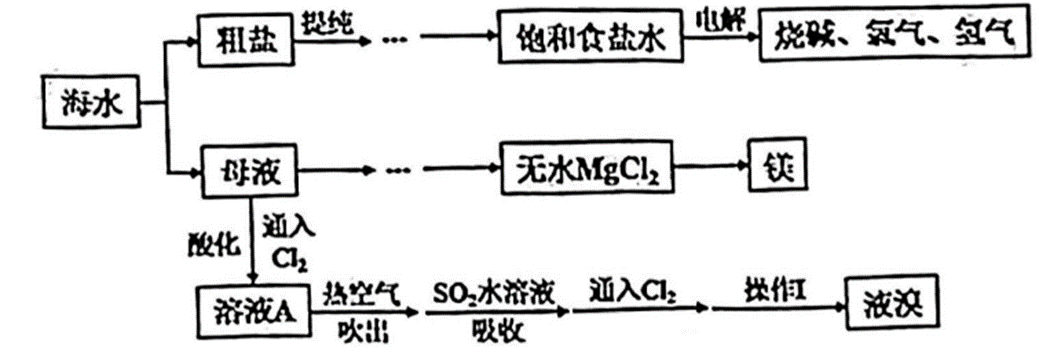
回答下列问题:
-
(1) 用于电解的食盐水需先除去其中
 、
、 、
、 等可溶性杂质。为制得纯净的食盐晶体,操作简述如下:
等可溶性杂质。为制得纯净的食盐晶体,操作简述如下:a.溶解;
b.依次加入过量的溶液、
 溶液、溶液;
溶液、溶液;c.充分反应后,静置,;
d.向滤液中加入适量盐酸;
e.。
①请补全上述操作中缺少的反应试剂和实验步骤。
②检验步骤b中
 已沉淀完全的方案:静置后,向上层清液中滴加,若,则说明
已沉淀完全的方案:静置后,向上层清液中滴加,若,则说明 已沉淀完全。
已沉淀完全。 -
(2) 镁可从母液中提取。工业上由无水
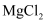 制取
制取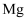 的化学方程式为
的化学方程式为
-
(3) 海水提溴工艺流程主要包括氧化、吹出、吸收、分离等环节。
①向母液中通入适量的
 , 其目的是(用离子方程式表示)。
, 其目的是(用离子方程式表示)。②已知溴的沸点为59℃。上述流程中“操作I”应为。
-
(4) 下列有关说法正确的是____。A . 海水中含量最多的元素是
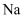 、
、 B . 海水淡化的主要方法有蒸馏法、电渗析法和离子交换法
C . 工业上通过电解饱和食盐水制备金属钠和氯气
D . 海水提溴工艺中“吹出”和“吸收”两环节的目的是富集溴
B . 海水淡化的主要方法有蒸馏法、电渗析法和离子交换法
C . 工业上通过电解饱和食盐水制备金属钠和氯气
D . 海水提溴工艺中“吹出”和“吸收”两环节的目的是富集溴
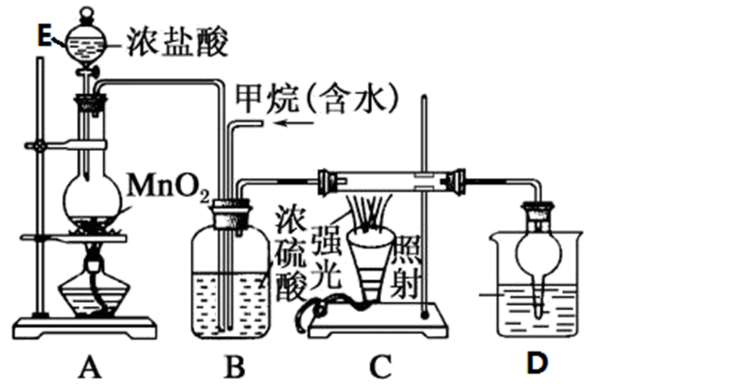
根据设计要求回答:
-
(1) 装置E的名称是,D装置中使用球形干燥管的作用。
-
(2) 写出CH4与Cl2生成一氯代物的化学反应方程式,该反应的类型是
-
(3) B装置有三种功能:①控制气体流速;②干燥气体;③。
-
(4) 若D装置中盛有AgNO3溶液,现象是有白色沉淀产生。此现象并不能说明该有机反应的类型。为了证明该反应有HCl生成,将装置进行改进:
①在A、B装置间增加一个盛有的洗气瓶;②。
-
(5) 在C装置中,经过一段时间的强光照射,发现硬质玻璃管内壁有黑色小颗粒产生,写出置换出黑色小颗粒的化学方程式:
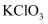 )可用于烟花、医药、火箭推进剂等。实验室中用下图装置制取氯气,并用氯气与
)可用于烟花、医药、火箭推进剂等。实验室中用下图装置制取氯气,并用氯气与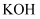 溶液反应制取氯酸钾(部分仪器已省略)。
溶液反应制取氯酸钾(部分仪器已省略)。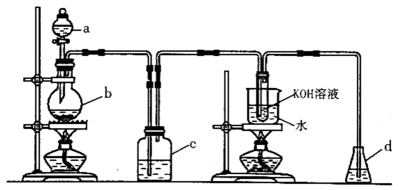
-
(1) 仪器b的名称是,b中发生反应的化学方程式是。
-
(2) 仪器c中盛放的液体是,其作用是。
-
(3) 氯气与
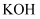 溶液反应时,采用水浴加热的优点是(答一条)。
溶液反应时,采用水浴加热的优点是(答一条)。
-
(4) 仪器d中盛放的液体是,其作用是。
- 下图为体液免疫示意图,下列叙述正确的是A.①过程体现了细胞膜的流动性 B.⑤过程主要发生在细胞质基质中 C.浆细胞能特异
- 下图是反射弧的局部结构示意图,刺激c点,检测各位点电位变化。下列说法错误的是( ) A.电表①不偏转,电表②偏转
- —Now that you like the car so much, why not drive it back?
- Jeremy Kerr, a researcher at the University of Ottawa in Can
- 下列命题中,真命题是( )①当b>0时,a>b>1 ②当b>0时,a<b<1 ③当a>0,b>0时,>1a>b
- 代糖是一种人工合成的甜味剂(sweetener),由于它不会被消化而变为能量供给身体所需,所以适合一些减肥人士食用。目前
- 4.下列各句中,加点的成语使用恰当的一项是( ) (2分)A.他性格比较内向,平时沉默寡言,但是一到课堂上就变得振振
- 如图8是一台电冰箱的铭牌,其中“耗电量0.50(kW·h/24h)这个参数的含义是,该冰箱正常使用24h消耗的电能为
- 下列说法不正确的是 A.酸碱度和温度是通过影响酶来影响果汁产量的B.酶的数量越多,果汁产量越多 C.酶的催化反应时间能够
- 下列函数中,自变量x的取值范围是的函数是( ) A.
- 如下图是a、b两种固体物质的溶解度曲线,下列说法中错误的是( )A.a中含有少量b时,可以用结晶法提纯aB.20
- 一质点从静止开始做直线运动,第1s内以加速度a1=1m/s2运动,第2s内加以速度a2=-1m/s2运动,如此反复.照这
- 下列物质所含分子物质的量最多的是( ) A.4 ℃时2.7 mL水
- 阅读下面的文章,完成后面题。 有泪水的牲口 (1)我离开马坊好多年了。我熟悉的那些人,尽管有一大群已经回到土里去了,但在
- 甲状腺细胞可以将氨基酸和碘合成甲状腺球蛋白,并且将甲状腺球蛋白分泌到细胞外,其过程如下图所示。下列叙述错误的是
- 37. There are many harbors on the east ____ of our land. A.
- Our teachersaid that light______ faster than sound. A. trav
- 17.历史上最早应用的还原性染料是靛蓝,其结构简式如图所示,下列关于靛蓝的叙述中错误的是()A.靛蓝由碳、氢、氧、氮四种
- 美籍华裔科学家钱永健、日本科学家下修村和美国科学家马丁·沙尔菲因在发现和研究绿色荧光蛋白(GFP)方面做出突出贡献而分享
- 压路机上的碾子质量很大,这是通过 ▲ 的方法来 ▲ 压强(“增大”或“减小”);在高山上做饭通常要使用高