第三节 电解池 知识点题库
如图所示,将两烧杯用导线如图相连,Pt、Mg、Al、C分别为四个电极,当闭合开关S后,以下表述正确的是( )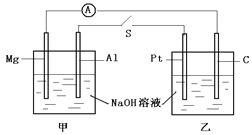
-
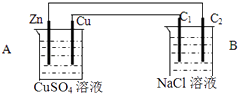
(1) 判断装置的名称:A池为 B池为
-
(2) 铜极为极,电极反应式为
-
(3) 石墨棒C1为极,电极反应式为.
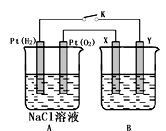
某化学兴趣小组用下图所示装置进行电化学原理的实验探究,回答下列问题:
-
(1) 通O2的Pt电极为电池极(填电极名称),其电极反应式为。
-
(2) 若B电池为电镀池,目的是在某镀件上镀一层银,则X电极材料为,电解质溶液为。
-
(3) 若B电池为精炼铜,且粗铜中含有Zn、Fe、Ag、Au等杂质,在电极(填“X”或“Y”)周围有固体沉积,沉积固体的成分为。
-
(4) 若X、Y均为Pt,B电池的电解质溶液为500 mL 1.0mol/L的NaCl溶液,当电池工作一段时间断开电源K,Y电极有560mL(标准状况)无色气体生成(假设电极产生气体完全溢出,溶液体积不变)。恢复到常温下,B电池溶液的pH=,要使该溶液恢复到原来的状态,需加入(填物质并注明物质的量)。
-
(5) 若X、Y均是铜,电解质溶液为NaOH溶液,电池工作一段时间,X极附近生成砖红色沉淀,查阅资料得知是Cu2O,试写出该电极发生的电极反应式为。
-
(6) 若X、Y均是Pt,电解质溶液为饱和Na2SO4溶液,通电一段时间后,在阴极上逸出c mol气体,同时有N g Na2SO4•10H2O 晶体析出,若温度不变,此时剩余溶液的溶质的质量分数为。
(学法题)通过以上题目,请总结书写电极反应式的关键 。
-
(1) Ⅰ.工业上可利用CO2来制备清洁燃料甲醇,有关化学反应如下:
反应A:CO2(g)+3H2(g)
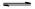 CH3OH(g)+H2O(g) △H1=-49.6kJ·mol-1
CH3OH(g)+H2O(g) △H1=-49.6kJ·mol-1反应B:CO2(g)+H2
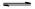 H2O(g)+CO(g) △H2=+41kJ·mol-1
H2O(g)+CO(g) △H2=+41kJ·mol-1写出用CO(g)和H2(g)合成CH3OH(g)反应的热化学方程式:。
-
(2) 反应A可自发进行的温度条件是(填“低温”或“高温”)。
-
(3) 写出两个有利于提高反应A中甲醇平衡产率的条件。
-
(4) 在Cu-ZnO/ZrO2催化下,CO2和H2混和气体,体积比1∶3,总物质的量amol进行反应,测得CO2转化率、CH3OH和CO选择性随温度、压强变化情况分别如图所示(选择性:转化的CO2中生成CH3OH或CO的百分比)。
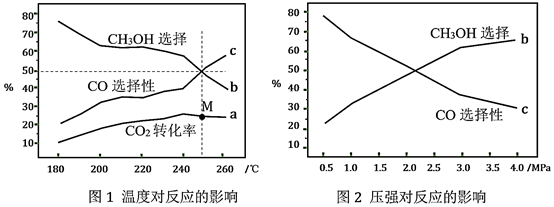
①由上图可知,影响产物选择性的外界条件是。
A.温度 B.压强 C.催化剂
②图1中M点温度为250℃,CO2的平衡转化率为25%,该温度下反应B的平衡常数为(用分数表示)。
-
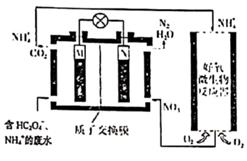
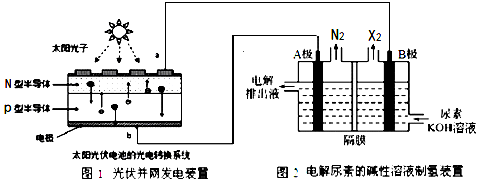
(5) Ⅱ.实验室模拟“间接电化学氧化法”处理氨氮废水中NH4+的装置如图所示。以硫酸铵和去离子水配制成初始的模拟废水,并以NaCl调节溶液中氯离子浓度,阳极产物将氨氮废水中的NH4+氧化成空气中的主要成分。
阳极反应式为。
-
(6) 除去NH4+的离子反应方程式为。
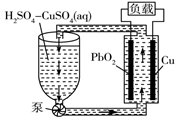
 =PbSO4+2H2O
D . 电池工作过程中,两个电极的质量均减小
=PbSO4+2H2O
D . 电池工作过程中,两个电极的质量均减小
-
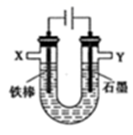
(1) 实验一:电解饱和食盐水
实验约需40mL饱和食盐水,配置450mL饱和食盐水所需的玻璃仪器有:烧杯、_____。
A . 450mL容量瓶 B . 500mL容量瓶 C . 电子天平 D . 玻璃棒 E . 量筒 F . 胶头滴管 -
(2) 电解饱和食盐水的化学方程式为。
-
(3) Y电极附近产物的检验方法:。
-
(4) 实验二:电解不饱和食盐水及产物分析。相同条件下,电解1mol/L NaCl溶液并收集两极产生的气体。在X处收集到V1 mL气体。同时,在Y处收集到V2 mL气体,停止电解。结果发现V2<V1 , 且与电解饱和食盐水相比,Y处收集到的气体颜色明显较浅。经讨论分析,导致上述现象的原因有:
i.有部分Cl2溶于NaCl溶液中;
ii.有O2生成。
设计实验证明有部分Cl2溶于NaCl溶液中,实验方案为。
-
(5) 证明有O2生成并测定O2的体积。按如图所示装置进行实验,通过注射器缓缓地将在Y处收集到V2 mL气体全部推入装置A(盛有足量试剂NaOH溶液)中,最终,量气管中收集到V3 mL气体(设V1、V2、V3均在相同条件下测得)。
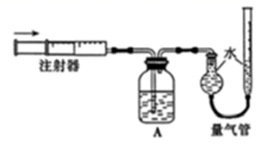
①装置A的作用是。
②本实验中,观察到的现象,说明石墨电极上有O2生成。
③实验中是否需要预先除尽装置中的空气?(填“是”或“否”)。
④实验二中,在石墨电极上产生的Cl2的总体积为mL(用代数式表示)。
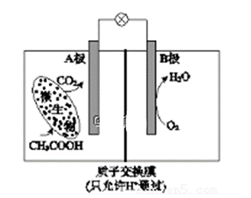
CO(g)+ 2H2(g)  CH3OH(g) △H
CH3OH(g) △H
-
(1) 已知2CO(g) + O2(g) = 2CO2(g) △H=-566kJ•mol-1;
2H2(g) + O2(g) = 2H2O(l) △H=-572kJ•mol-1;
且CH3OH(g)+
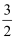 O2(g)
O2(g)  CO2(g)+2H2O(l) △H=-761kJ•mol-1;
CO2(g)+2H2O(l) △H=-761kJ•mol-1;则CO(g)+ 2H2(g)
 CH3OH(g)的△H= 。
CH3OH(g)的△H= 。 -
(2) 为了提高CO和H2制备甲醇生产效率和产量,工业生产中通常采取的措施是。(写出两点)
-
(3) 实验室模拟用CO和H2反应来制甲醇,在250 ℃下,将一定量的CO和H2投入10 L的密闭容器中,各物质的物质的量浓度(mol·L-1)变化如下表所示:
2 min
4 min
6 min
CO
0.07
0.05
0.05
H2
x
0.10
0.10
CH3OH
0.03
0.05
0.05
①250℃时,该反应的平衡常数K=;
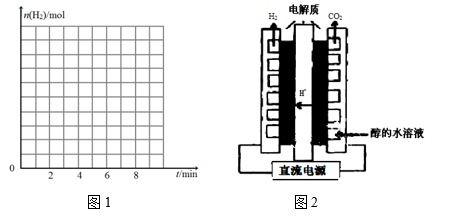
②在图1中画出反应开始至第6 min时H2的物质的量的变化曲线,并标出合适的纵坐标。
-
(4) 利用电解甲醇水溶液制备氢气最大的优点就是需要的电压低,装置如图2,写出阳极电极反应方程式,电解的总反应化学方程式。
下列说法错误的是( )
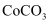 。炼锌产生的废渣中含钴10~18%、锌15~20%左右,还含有少量锰、铁、铜、镉等金属。
。炼锌产生的废渣中含钴10~18%、锌15~20%左右,还含有少量锰、铁、铜、镉等金属。 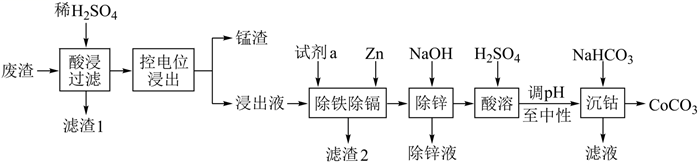 已知:
已知: 
-
(1) 滤渣1的成分是,提高“酸浸”浸出率的措施有。(任写一条措施)
-
(2) “控电位浸出”是控制合适的氧化电位电解除锰,将溶液中
 变为
变为  除去,写出阳极电极反应式。
除去,写出阳极电极反应式。
-
(3) 已知浸出液含金属离子为
 、
、  、
、  、
、 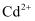 ,试剂a是
,试剂a是  和
和 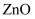 的悬浊液,试剂a除铁的原理是(文字表述);滤渣2成分是。(写化学式)
的悬浊液,试剂a除铁的原理是(文字表述);滤渣2成分是。(写化学式)
-
(4) “沉钴”的离子方程式是,该步骤选择
 ,而不用
,而不用  的原因是。
的原因是。
-
(5)
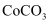 与
与 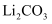 按一定比例在700℃下烧结,可得重要的电极材料钴酸锂(
按一定比例在700℃下烧结,可得重要的电极材料钴酸锂( 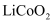 ),烧结反应化学方程式是。
),烧结反应化学方程式是。
 LiLaZrTaO+6C
LiLaZrTaO+6C 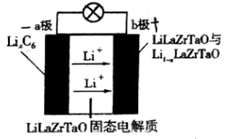
下列说法错误的是( )
-
(1) I.已知:①2Cu2S(s)+3O2(g)=2Cu2O(s)+2SO2(g) ΔH=−768.2 kJ∙mol−1
②2Cu2O(s)+Cu2S(s)=6Cu(s)+SO2(g) ΔH=+116.0 kJ∙mol−1
则Cu2S(s)+O2(g)=2Cu(s)+SO2(g) ΔH=。 -
(2) II.如图所示,E为浸过含酚酞的Na2SO4溶液的滤纸;A、B均为铂片,压在滤纸两端;R、S为电源的电极;M、N是用多微孔的Ni制成的电极,在碱溶液中可视为惰性电极:G为电流计;K为开关;C、D和电解池中都充满浓KOH溶液。若在滤纸中央滴一滴紫色的KMnO4溶液,将开关K打开,接通电源一段时间后,C、D中有气体产生。
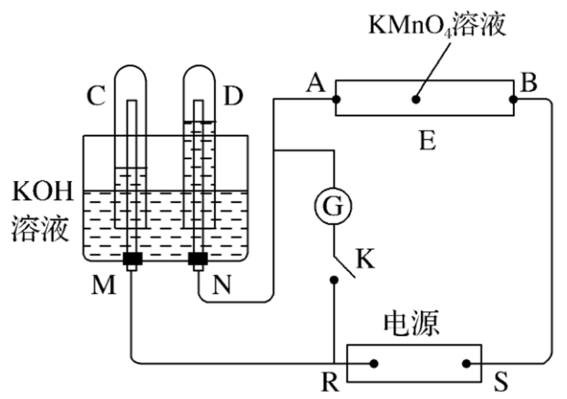
回答下列问题:
R为(填“正”或“负”)极。
-
(3) 通电一段时间后,M极附近溶液的pH(填“变大”、“变小”或“不变”);B极区的电极反应式为。
-
(4) 滤纸上的紫色点向(填“A”或“B”)方向移动。
-
(5) 通电一段时间后,C、D中的气体产生到一定量时,切断外电源并接通开关K,C、D中的气体逐渐减少,C中的电极反应式为。
-
(1) 某ClO2泡腾片的有效成分为NaClO2 , NaHSO4 , NaHCO3 , 其溶于水时,NaClO2和NaHSO4反应生成ClO2和Cl- , 并逸出大量气体,逸出气体的主要成分是(填化学式)。
-
(2) 测定某水样中ClO
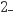 浓度可采用氧化还原滴定法:量取25.00mL水样于碘量瓶中,加水稀释至50.00mL,加入过量KI,再滴入适量稀硫酸,充分反应后,滴加1mL淀粉溶液,用0.01000mol·L-1Na2S2O3标准溶液滴定至终点,消耗标准溶液20.00mL。
浓度可采用氧化还原滴定法:量取25.00mL水样于碘量瓶中,加水稀释至50.00mL,加入过量KI,再滴入适量稀硫酸,充分反应后,滴加1mL淀粉溶液,用0.01000mol·L-1Na2S2O3标准溶液滴定至终点,消耗标准溶液20.00mL。已知:ClO
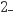 +4I−+4H+=2H2O+2I2+Cl− , I2+2S2O
+4I−+4H+=2H2O+2I2+Cl− , I2+2S2O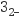 =2I−+S4O
=2I−+S4O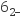
①滴定终点的现象是:。
②下列关于滴定分析的操作,不正确的是。
A.用量筒量取25.00mL水样
B.滴定时要适当控制滴定速度
C.装标准溶液的滴定管,滴定前尖嘴处有气泡,滴定后气泡消失,造成测定结果偏低
D.终点读数时俯视滴定管液面,会造成测定结果偏低
E.再次滴定时,须重新装液并调节液面至“0”刻度或“0”刻度以下
③计算水样中ClO
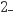 的浓度
的浓度 -
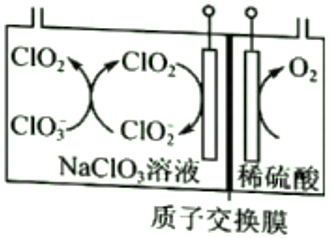
(3) ClO2可用隔膜电解NaClO3制备,装置如图所示。制备时先在NaClO3溶液中通入少量ClO2气体,写出阴极上的电极反应式:。
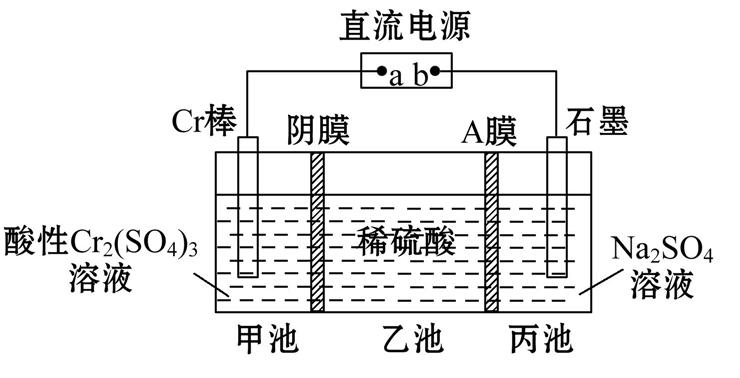
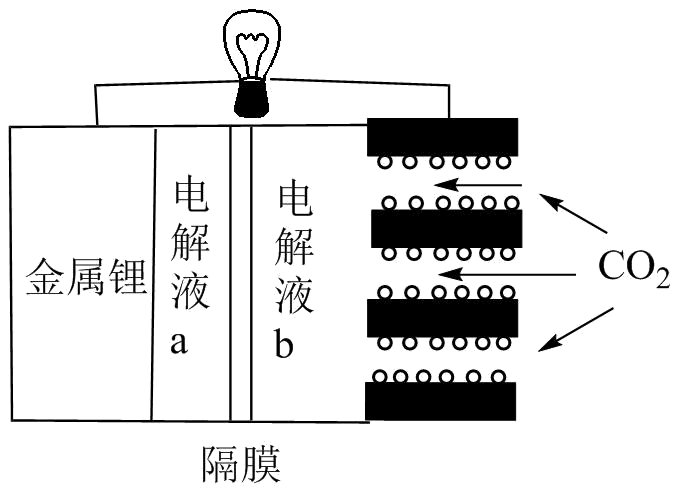
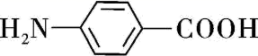 )是一种用途广泛的化工产品和医药中间体,以对硝基苯甲酸(
)是一种用途广泛的化工产品和医药中间体,以对硝基苯甲酸(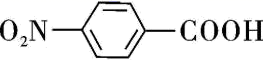 )为原料,采用电解法合成对氨基苯甲酸的装置如图。
)为原料,采用电解法合成对氨基苯甲酸的装置如图。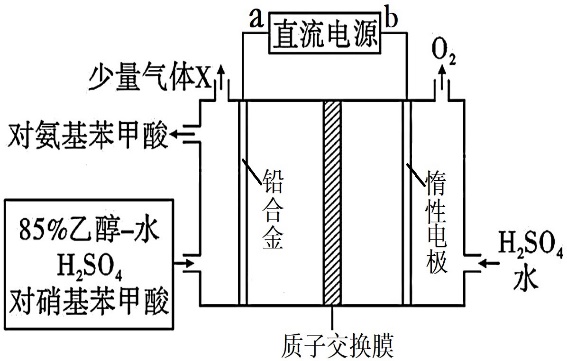
下列说法错误的是( )
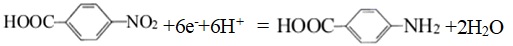
-
(1) I.工业用H2和CO2在一定条件下合成乙烯:6H2(g)+2CO2(g)
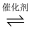 CH2=CH2(g)+4H2O(g) ΔH1
CH2=CH2(g)+4H2O(g) ΔH1已知:①2H2(g)+O2(g)=2H2O(1) ΔH2=-571.4kJ·mol-1
②CH2=CH2(g)+3O2(g)→2CO2(g)+2H2O(1) ΔH3=-1411kJ·mol-1
③H2O(g)=H2O(1) ΔH4=-44kJ·mol-1
ΔH1=
-
(2) 在密闭容器中充入体积比为3:1的H2和CO2 , 不同温度对CO2的平衡转化率和催化剂催化效率的影响如图所示,下列说法正确的是____。
 A . 为了提高乙烯的产率应尽可能选择低温 B . 生成乙烯的速率:v(M)可能小于v(N) C . 平衡常数:KM<KN D . M点时的压强一定小于N点时的压强
A . 为了提高乙烯的产率应尽可能选择低温 B . 生成乙烯的速率:v(M)可能小于v(N) C . 平衡常数:KM<KN D . M点时的压强一定小于N点时的压强 -
(3) II.工业用甲烷催化法制取乙烯:2CH4(g)=C2H4(g)+2H2(g) ΔH>0,T℃时,向4L的恒容反应器中充入2molCH4 , 仅发生上述反应,反应过程中CH4的物质的量随时间变化如图所示:
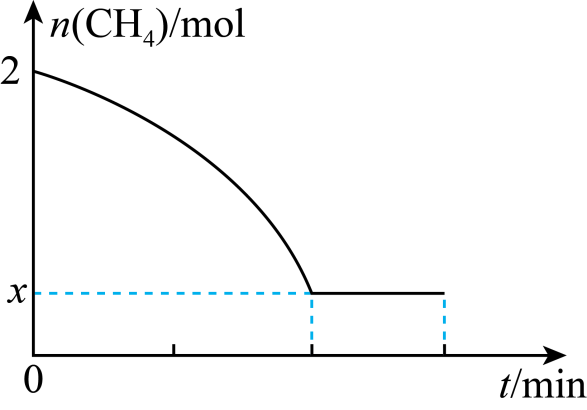
实验测得v正=k正c2(CH4),v逆=k逆c(C2H4)·c2(H2),k正、k逆为速率常数,只与温度有关,T℃时k正与k逆的比值为(用含x的代数式表示);若将温度升高,速率常数增大的倍数:k正(填“>”“=”或“<”)k逆。
-
(4) III.乙烷裂解制乙烯:C2H6(g)
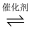 C2H4(g)+H2(g)。
C2H4(g)+H2(g)。T℃时,将乙烷与氦气体积比2:1混合后,通入一密闭容器中发生反应。平衡时容器压强为P0Pa,若乙烷的平衡转化率为50%,反应的平衡常数Kp=(用分压表示,分压=总压×物质的量分数)。
IV.电化学法还原二氧化碳制乙烯原理如下图所示。
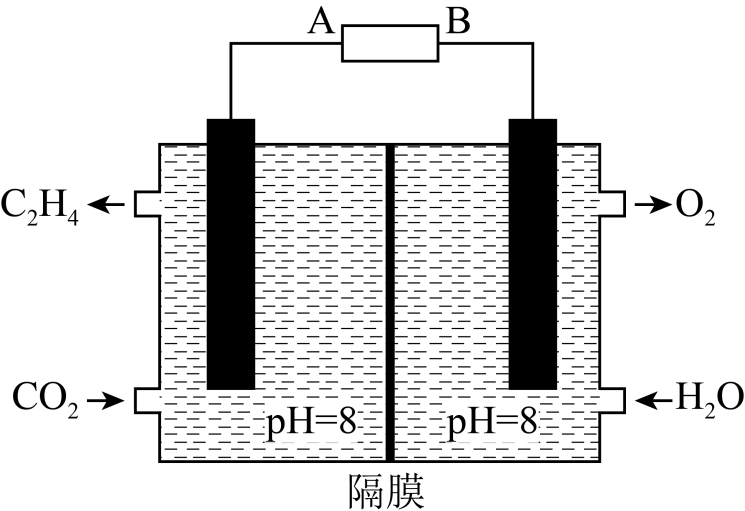
-
(5) 阴极电极反应式为:,电路中转移0.6mol电子,两极共收集气体L(标准状况)。
- 已知数列的前项和,则 .
- 如图5所示的电路中,电源电压不变,R1为定值电阻,电键S闭合后,滑动变阻器滑片向左滑动时,电流表的示数,电压表示数与电流
- 1878年,征战四方的日本海军因食用精米白面,约有三分之一的人得了一种疾病,病人全身浮肿、肌肉疼痛、四肢无力,脚肿得象酒
- 35. She is __________ being pleased about it; she is very an
- 根据西周分封制,诸侯必须( ) ①定期向周天子朝贡 ②随从周天子作战 ③服从周天子命令 ④按田亩向周天子纳
- 下列哪个不是植物繁殖的新途径 A.微型繁殖 B.作物脱毒 C.
- 上海宝山钢铁工业发展的条件是( ) A.煤炭丰富 B.铁矿丰富 C.优惠的政策
- 读下列材料和地图,回答各小题。材料:坦赞铁路东起坦桑尼亚首都达累斯萨拉姆,西至赞比亚的卡皮里姆波希,由中国专家和工程技术
- 下列属于组织培养的是() A.花粉培养成单倍体植株 B.芽发育成枝条 C.根尖分生区发育成成熟区 D.受精卵发育成植株
- 为探讨盐对某种植物幼苗光合作用的影响,在不同浓度NaCl条件下,对其净光合速率、胞间CO2浓度、光合色素含量等进行测定,
- 对比分析不同物质的共性与差异性是学习化学的有效方法。下列关于CO2和CO的各项对比,有错误的是() 选项 共性 差异性
- 已知等差数列{an}的前n项和为Sn,且a1=2,S5=30,数列{bn}的前n项和为Tn,且Tn=2n﹣1. (Ⅰ)求
- 纪念全国人民代表大会成立50周年的隆重集会上强调:人民代表大会制度是我国的根本政治制度,这是我党把马克思主义基本原理同中
- 前不久在台湾抗震救灾中,某地将甲、乙两个仓库的粮食全部转移到A、B两个仓库.甲库有粮食100吨,乙库有粮食80吨,而A库
- 阅读下面文字,完成14―17分。宇宙中“第五种力”之争 早在17世纪,伟大的意大利物理学家・枷利略,曾以一次具有深
- 某企业2014年的经济效益为120%,利润为200万;2015年由于市场需求下降,生产萎缩,生产总值减少了20%。要保证
- 如图所示装置,电流计的指针发生偏转,正极变粗,负极变细,符合这种情况的是( ) A.正极Cu,负极Zn,S为稀H2
- 是某有机物加氢后的还原产物,那么原有机物可能是A.乙醛的同分异构体 B.丁醛的同分异构
- 已知全集,集合,,则集合 =( )A. {3} B. {4,5} C. {3,4,5} D. {1,2,
- 下列物质中,属于合成材料的是() A.棉花



