第三节 电解池 知识点题库
查处酒后驾驶采用的“便携式乙醇测量仪”以燃料电池为工作原理,在酸性环境中,理论上乙醇可以被完全氧化为CO2 , 但实际乙醇被氧化为X,其中一个电极的反应式为:CH3CH2OH-2e-→X+2H+。下列说法中正确的是( )
A . 电池内部H+由正极向负极移动
B . 另一极的电极反应式为:O2+4e-+2H2O=4OH-
C . 乙醇在正极发生反应,电子经过外电路流向负极
D . 电池总反应为:2CH3CH2OH+O2→2CH3CHO+2H2O
在水中加等物质的量的Ag+、Ba2+、Na+、SO42-、NO3-、Cl- , 将该溶液放在用惰性电极作电极的电解槽中,通电片刻,则氧化产物与还原产物的质量比为 ( )
A . 35.5∶108
B . 16∶207
C . 8∶1
D . 108∶35.5
化学用语是学习化学的重要工具,下列用来表示物质变化的化学用语中,正确的是( )
A . 电解饱和食盐水时,阳极的电极反应式为:2Cl﹣﹣2e﹣═Cl2↑
B . 氢氧燃料电池的负极反应式:O2+2H2O+4e﹣═4OH﹣
C . 粗铜精炼时,与电源正极相连的是纯铜,电极反应式为:Cu﹣2e﹣═Cu2+
D . 钢铁发生电化学腐蚀的正极反应式:Fe﹣2e﹣═Fe3+
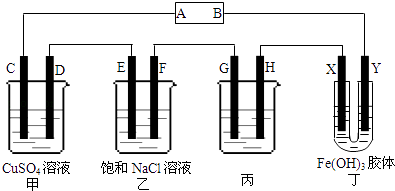
课题式研究性学习是培养学生创造性思维的良好方法,某研究性学习小组将下列装置如图链接,C、D、E、F、X、Y都是惰性电极.将电源接通后,向乙中滴入酚酞试液,在F极附件先显红色.试回答下列问题:
-
(1) 电源A极的名称是
-
(2) 甲装置中电解反应的总化学方程式:
-
(3) 如果收集乙装置中产生的气体,相同状况下两种气体的体积比是.
-
(4) 欲用丙装置给铜镀银,G应该是(填“铜”或“银”),电镀液的溶质是(填化学式).
-
(5) 装置丁中的现象是.
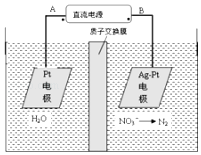
电化学降解法可用于治理水中硝酸盐的污染.电化学降解NO3﹣的原理如图,请写出阴极的电极反应式.
化学用语是学习化学的重要工具,下列用来表示物质变化的化学用语中,正确的是( )
A . 用惰性电极电解饱和食盐水时,阳极的电极反应式为2Cl﹣﹣2e﹣═Cl2↑
B . 氢氧燃料电池的负极反应式:O2+2H2O+4e﹣═4OH﹣
C . 粗铜精炼时,与电源正极相连的是纯铜,阳极反应式为Cu﹣2e﹣═Cu2+
D . 钢铁发生电化学腐蚀的正极反应式:Fe﹣2e﹣═Fe2+
某课外活动小组研究电解饱和食盐水。甲、乙两位同学均采用了以下仪器和试剂:烧杯、直流电源、铁钉、碳棒、导线以及滴加了两滴酚酞试液的饱和NaCl溶液。
-
(1) 甲同学设计的电解装置中,铁钉与直流电源的负极相连。通电后,很快可以观察到铁钉附近出现的现象为。但继续通电下,不久该现象就会消失,你认为其中的原因是。
甲同学的电解实验中,阳极反应式为,阴极反应式为。
-
(2) 乙同学设计的电解装置中,铁钉与直流电源的正极相连。若通电后,预期铁钉附近出现的现象为。
用惰性电极电解如下物质可制得对应金属的是( )
A . 电解熔融AlCl3获取金属铝
B . 电解MgCl2溶液获取金属镁
C . 电解CuCl2溶液获取金属铜
D . 电解饱和食盐水来获取金属钠
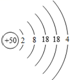
锡(Sn)是很早便被发现和使用的金属,其原子结构示意图见图。完成下列填空:
-
(1) 锡为主族元素,在元素周期表中的位置是。有一种锡的单质具有金刚石型结构,则该单质内存在的化学键是。
SnCl4
SnBr4
SnI4
熔点/℃
-33
31
144.5
沸点/℃
114.1
202
364
-
(2) 解释下表中卤化锡的熔、沸点的变化规律。
-
(3) SnO2能与NaOH反应生成钠盐,写出反应的化学方程式。
-
(4) 锡溶于盐酸得到溶液A,向A中通入氯气,氯气被还原。写出在A中反应的化学方程式
-
(5) 马口铁是在铁表面镀一层锡。一个马口铁罐装的桔子罐头发生了“涨罐”和马口铁罐穿孔的现象。经检测罐头内食物没有腐败,则罐头内导致“涨罐”的气体可能是,说明理由
设NA表示阿伏加德罗常数值,下列说法正确的是( )
A . 含NA个CO32-的Na2CO3溶液中,Na+数目小于2 NA
B . 100g质量分数为46%的乙醇水溶液中氧原子数为4NA
C . 常温下,1L pH=3的醋酸溶液稀释到10 L时,溶液中H+的数目大于0.01NA
D . 用惰性电极电解KOH溶液,若阳极产生5.6 L气体,则电路中通过0.5NA电子
我国科研团队成功研究出高比能量、低成本的钠离子二次电池,其工作原理示意图如下。已知电池反应:Na1-xMnO2+NaxCn  NaMnO2+nC。下列说法正确的是( )
NaMnO2+nC。下列说法正确的是( )
 NaMnO2+nC。下列说法正确的是( )
NaMnO2+nC。下列说法正确的是( )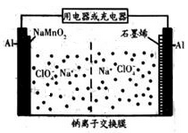
A . 电池放电过程中,NaMnO2/Al上的电势低于石墨烯/Al上的电势
B . 电池放电时,正极可发生反应Na1-xMnO2+xNa++xe-=NaMnO2
C . 电池充电时,外接电源的负极连接NaMnO2/Al电极
D . 电池充电时,Na+由NaMnO2/Al电极移向石墨烯/Al电极
碳酸锂是生产锂离子电池的重要原料。
-
(1) 碳酸锂制取锂的反应原理为:
①
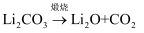 ;
;②
 。
。锂原子的电子排布式为;CO2的结构式为;反应②中物质涉及的化学键类型有。
-
(2) 碳原子核外电子有种不同能量的电子,其中有两个电子的能量最高且能量相等,这两个电子所处的轨道分别是。
-
(3) 氢化锂(LiH)是离子化合物,写出其阴离子的电子式,氢负离子(H-)与锂离子具有相同电子层结构,试比较两者微粒半径的大小,并用原子结构理论加以解释:。
-
(4) 用
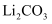 、氨水和液溴制备
、氨水和液溴制备  。除生成
。除生成  外,还产生了两种参与大气循环的气体,补全产物并配平该反应的化学方程式:
外,还产生了两种参与大气循环的气体,补全产物并配平该反应的化学方程式: 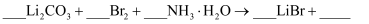 ,。
,。
-
(5) 磷酸亚铁锂电池总反应为:
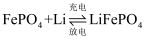 ,放电时,负极为(填写化学式)。若用该电池电解饱和食盐水(电解池电极均为惰性电极),当电解池两极共有
,放电时,负极为(填写化学式)。若用该电池电解饱和食盐水(电解池电极均为惰性电极),当电解池两极共有 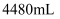 气体(标准状况)产生时,该电池消耗锂的质量为。
气体(标准状况)产生时,该电池消耗锂的质量为。
“充电5秒钟,使用半个月”的石墨烯电池目前正处于实验研发阶段。它是利用锂离子能在石墨烯表面和电极之间快速大量穿梭运动的特性制作的一种新型二次电池。其工作原理如图所示,电池反应式为LixC6+Li1-xCoO2  C6+LiCoO2。下列关于该电池的说法错误的是( )
C6+LiCoO2。下列关于该电池的说法错误的是( )
 C6+LiCoO2。下列关于该电池的说法错误的是( )
C6+LiCoO2。下列关于该电池的说法错误的是( ) 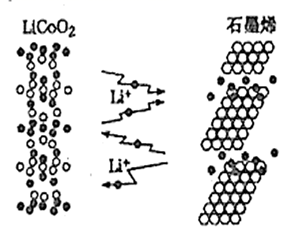
A . 充电时,Li+移向石墨烯
B . 充电时,转移0.5mol电子理论上阴极材料质量增加3.5g
C . 放电时,LiCoO2极发生的电极反应为LiCoO2-xe-=Li1-xCoO2+xLi+
D . 对废旧的该电池进行“放电处理”,让Li+从石墨烯中脱出有利于回收
已知  为中学化学中一种常见的盐,
为中学化学中一种常见的盐, 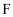 为淡黄色固体;
为淡黄色固体; 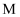 、
、 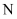 为常见的金属,
为常见的金属, 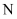 的氧化物可作耐火材料,可用它来制造耐火坩埚和耐高温试验仪器;
的氧化物可作耐火材料,可用它来制造耐火坩埚和耐高温试验仪器; 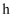 为气体单质,
为气体单质, 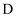 为无色气体,
为无色气体, 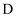 在空气中会出现红棕色,各物质的转化关系如下图(部分反应产物已略去)。
在空气中会出现红棕色,各物质的转化关系如下图(部分反应产物已略去)。
 为中学化学中一种常见的盐,
为中学化学中一种常见的盐, 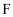 为淡黄色固体;
为淡黄色固体; 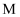 、
、 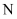 为常见的金属,
为常见的金属, 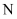 的氧化物可作耐火材料,可用它来制造耐火坩埚和耐高温试验仪器;
的氧化物可作耐火材料,可用它来制造耐火坩埚和耐高温试验仪器; 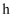 为气体单质,
为气体单质,  为无色气体,
为无色气体,  在空气中会出现红棕色,各物质的转化关系如下图(部分反应产物已略去)。
在空气中会出现红棕色,各物质的转化关系如下图(部分反应产物已略去)。 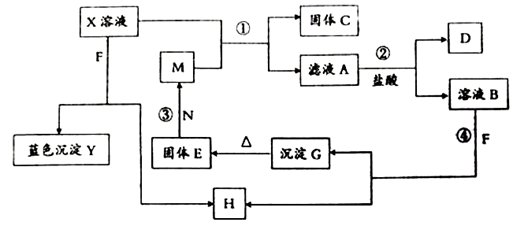
请回答下列问题;
-
(1)
 氧化物的化学式为,
氧化物的化学式为, 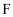 的电子式为。
的电子式为。
-
(2) 反应③的化学方程式为。
-
(3) 在反应①②③④中不属于置换反应的是(填序号)。
-
(4) 写出
 与
与 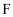 以等物质的量进行反应的离子方程式。
以等物质的量进行反应的离子方程式。
-
(5)
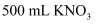 和
和 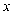 的混合溶液,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到
的混合溶液,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到 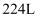 气体(标准状况下),假定电解后溶液体积仍为
气体(标准状况下),假定电解后溶液体积仍为 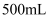 。
。 ①写出电解时阳极的电极反应式;
②电解后溶液中
 为
为 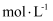
CO2与人类息息相关。近年来,CO2的资源化利用是化学研究热点之一。
-
(1) 已知:①2NaOH(s)+CO2(g)=Na2CO3(s)+H2O(g) ∆H1=-127.4kJ/mol
②NaOH(s)+CO2(g)=NaHCO3(s) ∆H2=-131.5kJ/mol
则:反应2NaHCO3(s)=Na2CO3(s)+H2O(g)+CO2(g) ∆H=kJ/mol。
-
(2) 25℃时,H2CO3的K1=4×10-7;K2=5×10-11。0.1mol/L的NaHCO3溶液中相关微粒的物质的量浓度关系为:c(H2CO3)c(
 )(填“>”、“<”或“=”)。
)(填“>”、“<”或“=”)。
-
(3) 人体血液中存在平衡CO2+H2O⇌H2CO3⇌H++
 ,当人呼吸过快或过深,体内失去二氧化碳太多,引发呼吸性碱中毒,导致手脚发麻、头晕。适用平衡移动原理解释上述现象:。
,当人呼吸过快或过深,体内失去二氧化碳太多,引发呼吸性碱中毒,导致手脚发麻、头晕。适用平衡移动原理解释上述现象:。
-
(4) 科学家利用电化学装置实现CH4和CO2的耦合转化,原理如图:
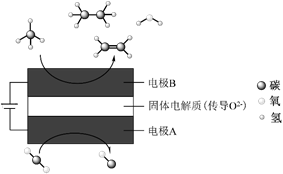
①电极A的电极反应式为。
②固体电解质中O2-传导方向是向极(填“A”或“B”)移动。
③若生成的乙烯和乙烷的物质的量之比为3:1,则消耗的CH4和CO2的物质的量之比为 。
④电催化CO2被还原为CO的具体应用价值是。
用如图所示的装置进行电解,A中盛有NaCl溶液,B中盛有饱和Na2SO4溶液,通电一会儿,发现湿润的淀粉KI试纸的D端变为蓝色。回答下列问题:
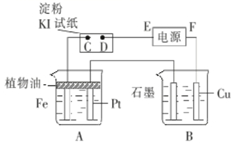
-
(1) 电源的F端为(填“正”或“负”)极。
-
(2) A中发生反应的总化学方程式为。
-
(3) B中石墨电极上的电极反应式为;Cu电极观察到的现象是;一段时间后,B中溶液pH(填“升高”、“降低”或“不变”)。
-
(4) 去掉该装置中的电源,改用导线连接,为使湿润的淀粉KI试纸的D端变为蓝色,可将(填“A”或“B”)中的溶液换成(填“稀硫酸”或“浓硝酸”)。
直接  燃料电池(
燃料电池( 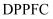 )是一种新型液态电池,其工作原理如图所示。下列说法错误的是( )
)是一种新型液态电池,其工作原理如图所示。下列说法错误的是( )
 燃料电池(
燃料电池( 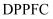 )是一种新型液态电池,其工作原理如图所示。下列说法错误的是( )
)是一种新型液态电池,其工作原理如图所示。下列说法错误的是( ) 
A . “气体c”为  B . 负极区溶液
B . 负极区溶液  增大
C . “电极b”的反应式为
增大
C . “电极b”的反应式为 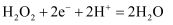 D . 当电路中转移
D . 当电路中转移 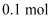 电子时,通过阴离子交换膜的
电子时,通过阴离子交换膜的  为4.8g
为4.8g
 B . 负极区溶液
B . 负极区溶液  增大
C . “电极b”的反应式为
增大
C . “电极b”的反应式为 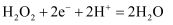 D . 当电路中转移
D . 当电路中转移 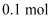 电子时,通过阴离子交换膜的
电子时,通过阴离子交换膜的  为4.8g
为4.8g
如图,甲、乙是两个完全相同的光伏并网发电模拟装置,利用它们对煤浆进行脱硫处理。下列叙述中错误的是( )
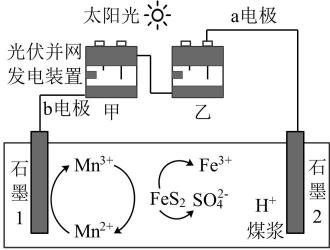
A . 光伏并网发电装置中b为正极
B . 石墨1电极上消耗1molMn2+ , 甲、乙中各转移0.5mol电子
C . 脱硫反应原理为:15Mn3++FeS2+8H2O=15Mn2++Fe3++2SO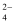 +16H+
D . 处理60gFeS2 , 石墨2电极上消耗7.5molH+
+16H+
D . 处理60gFeS2 , 石墨2电极上消耗7.5molH+
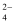 +16H+
D . 处理60gFeS2 , 石墨2电极上消耗7.5molH+
+16H+
D . 处理60gFeS2 , 石墨2电极上消耗7.5molH+
科学家利用多晶铜高效催化电解CO2制乙烯,原理如图所示。已知:电解前后电解液浓度几乎不变。下列说法错误的是( )
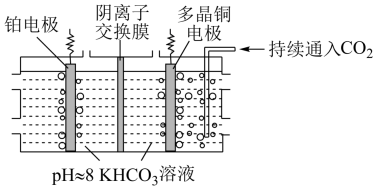
A . 铂电极产生的气体是O2和CO2
B . 铜电极的电极反应式为2CO2+12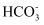 +12e-=C2H4+12
+12e-=C2H4+12 +4H2O
C . 通电过程中,溶液中
+4H2O
C . 通电过程中,溶液中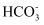 通过阴离子交换膜向右槽移动
D . 当电路中通过0.6mol电子时,理论上能产生标况下C2H41.12L
通过阴离子交换膜向右槽移动
D . 当电路中通过0.6mol电子时,理论上能产生标况下C2H41.12L
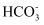 +12e-=C2H4+12
+12e-=C2H4+12 +4H2O
C . 通电过程中,溶液中
+4H2O
C . 通电过程中,溶液中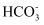 通过阴离子交换膜向右槽移动
D . 当电路中通过0.6mol电子时,理论上能产生标况下C2H41.12L
通过阴离子交换膜向右槽移动
D . 当电路中通过0.6mol电子时,理论上能产生标况下C2H41.12L
近日,我国科研团队设计了一种表面锂掺杂的锡纳米粒子催化剂s-SnLi可提高电催化制甲酸盐的产率,同时释放电能,实验原理如图所示。下列说法错误的是( )
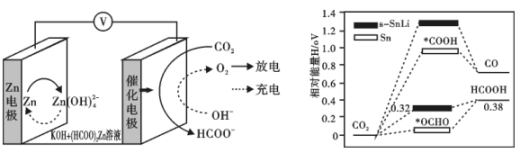
A . 使用催化剂能有效减少副产物CO的生成;使用s-SnLi催化剂,中间产物更不稳定
B . 充电时,阳极电极周围pH降低
C . 放电时,每生成1 mol HCOO- , 转移1 mol电子
D . 放电时,负极电极反应式为Zn+4OH--2e-=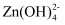
最近更新
- 八年级学生去距学校10千米的博物馆参观,一部分学生骑自行车先走,过了20分件后,其余学生乘汽车出发,结果他们同时到达.己
- 2010年8月15日,国务院法制办公室将《中华人民共和国社会救助法(征求意见稿)》全文公布,征求社会各界意见。这样做是因
- 硫隔绝空气加热后的蒸气中有一种物质的化学式为S8,关于S8的叙述正确的有() A.它是一种新型的化合物 B.相对分子质量
- 以下生物,除哪一种外都是由细胞构成的? A.草履虫 B.海带
- When milk arrived on the doorstep When I was a boy growing u
- 下列有关物质性质的描述中,属于化学性质的是 A.干冰易升华 B.酒精能燃
- ;
- U常见化合价有+4和+6,硝酸铀酰[UO2(NO3)2]加热可发生如下分解。UO2(NO3)2――UxOy+NO2↑+O
- 10.默写 (1)她静默的远了,远了, ,走尽这雨巷。(《雨巷》) (2)
- 面对CPI不断走高,我国政府可能采取的措施有 ①采取行政手段调控商品价格 ②上调存款准备金率,持续小幅加息③大量发行长期
- The teacher ______ have thought Johnson was worth it or she
- 人们的消费受相关商品价格变动的影响,如果A商品和B商品的关系如下表,则B商品中①②的需求量应分别是_____、_____
- The dance performed by the disabled actors is really a hit,
- 团购日益成为人们喜爱的购物方式,团购的商品从数码产品到服装美食……内容极其丰富,而最让人动心的是实惠的团购价。在这里,团
- ________ this is not the right way to the station, what shal
- 与《中国人民政治协商会议共同纲领》相比,1954年《中华人民共和国宪法》的新特点是 A.规定国家的权力属于人民
- 2009年6月5日,中央纪委、监察部召开的反腐倡廉工作座谈会强调,要以更坚定的态度、更有力的措施、更务实的作风加快推进重
- ⑴古诗默写。(必须默写)_______________,春与秋其代序。 ,恐美人之迟暮。 (
- 核糖与核酸都不含有的元素是 () A.N B.O C.P
- 12、孔子和苏格拉底是公元前5世纪的东西方思想巨人,两者思想的不同之处是 A.重视道德的意义 B.肯定人的



