第二节 化学电源 知识点题库
高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压。高铁电池的总反应为:3Zn+2K2FeO4+8H2O 3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述不正确的是
3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述不正确的是
A . 放电时负极反应为:Zn-2e-+2OH-==Zn(OH)2
B . 充电时阳极反应为:Fe(OH)3-3e-+5OH-==FeO42-+4H2O
C . 放电时每转移3mol电子,正极有1molK2FeO4被氧化
D . 放电时正极附近溶液的碱性增强
铅蓄电池是典型的二次电池,它的正、负极格板是惰性材料,电池总反应式为:Pb+PbO2+4H++2SO42﹣⇌2PbSO4+2H2O,请回答下列问题:
放电时:正极的电极反应式是 ;电解质溶液中H2SO4的浓度将变 (填“变大”、“变小”或“不变”);当外电路通过1mol电子时,理论上负极板的质量增加 g.
氢氧燃料电池是一种高效、环境友好的发电装置,它是以铂作电极,KOH溶液作电解液,总反应为:2H2+O2═2H2O,正极反应为:O2+2H2O+4e﹣═4OH﹣ , 下列叙述不正确的是( )
A . H2通入负极区
B . O2通入正极区
C . 负极反应为2H2+4OH﹣﹣4e﹣═4H2O
D . 正极发生氧化反应
下列用来表示物质变化的化学用语中,正确的是( )
A . 用惰性电极电解饱和食盐水时,阳极的电极反应式为2Cl﹣﹣2e﹣=Cl2↑
B . 在碱性介质中,氢氧燃料电池的负极反应式为O2+2H2O+4e﹣=4OH﹣
C . 粗铜精炼时,与电源正极相连的是纯铜,电极反应式为Cu﹣2e﹣=Cu2+
D . 钢铁发生电化学腐蚀的正极反应式为Fe﹣2e﹣=Fe2+
生物燃料电池是以有机物为燃料,直接或间接利用酶作为催化剂的一类特殊的燃料电池,其能量转化率高,是一种真正意义上的绿色电池,其工作原理如图所示.已知C1极的电极反应为C2H5OH+3H2O﹣12e﹣═2CO2+12H+ . 下列说法中不正确的是( )
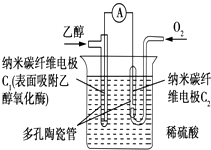
A . C1极为电池负极,C2极为电池正极
B . 溶液中的H+向C1电极移动
C . 该生物燃料电池的总反应方程式为C2H5OH+3O2═2CO2+3H2O
D . 电流由C2极经外电路流向C1极
用镁一次氯酸钠燃料电池作电源模拟消除工业酸性废水中的Cr2O72-的过程(将“Cr2O72-”还原为“Cr3+”),装置如图所示。下列说法中错误的是( )
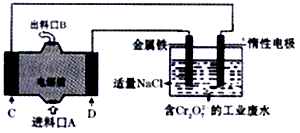
A . 金属铁电极的反应为:Fe-2e-=Fe2+
B . 装置中电子的流动路线是: C电极→惰性电极→金属铁电极→D电极
C . 装置工作过程中消耗14.4gMg,理论上可消除Cr2O72-0.1mol
D . 将Cr2O72-处理后的废水比原工业废水的pH增大
如图是一种可充电的锂离子电池充放电的工作示意图。放电时该电池的电极反应式为:
负极:LixC6-xe-=C6+xLi+(LixC6表示锂原子嵌入石墨形成的复合材料)
正极:Li1-xMnO2+xLi++xe-=LiMnO2(LiMnO2表示含锂原子的二氧化锰)
下列有关说法错误的是 ( )
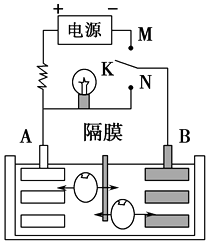
A . 该电池的反应式为Li1-xMnO2+LixC6=LiMnO2+C6
B . K与M相接时,A是阳极,发生氧化反应
C . K与N相接时,Li+由A极区迁移到B极区
D . 在整个充、放电过程中至少存在3种形式的能量转化
控制适当的条件,将反应2Fe3++2I-  2Fe2++I2设计成如图所示的原电池。下列判断错误的是( )
2Fe2++I2设计成如图所示的原电池。下列判断错误的是( )
 2Fe2++I2设计成如图所示的原电池。下列判断错误的是( )
2Fe2++I2设计成如图所示的原电池。下列判断错误的是( ) 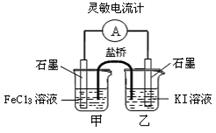
A . 反应开始时,乙中电极反应为2I--2e-= I2
B . 反应开始时,甲中石墨电极上Fe3+被还原
C . 电流计读数为零时,反应达到化学平衡状态
D . 平衡时甲中溶入FeCl2固体后,电流计读数为零
通过膜电池可除去废水中的乙酸钠和对氯苯酚( 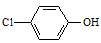 ),其原理如图所示,下列说法错误的是( )
),其原理如图所示,下列说法错误的是( )
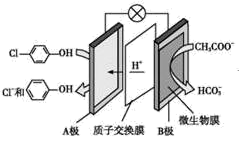
A . 该方法能够提供电能
B . B极上的电势比A极上的电势低
C . A极的电极反应为 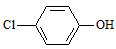 +H++2e-→Cl-+
+H++2e-→Cl-+ 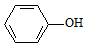 D . 电池工作时H+通过质子交换膜由正极区向负极区移动
D . 电池工作时H+通过质子交换膜由正极区向负极区移动
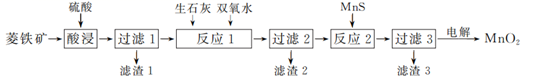
二氧化锰在工业上具有重要的作用,工业上可利用菱锰矿(主要成分为MnCO3、SiO2、FeCO3以及少量CuO)制取。制备流程如图所示:
-
(1) 酸浸过程中,MnCO3溶解的离子方程式为,选择用硫酸而不选择盐酸溶解,除了盐酸挥发造成设备腐蚀以外,另一个原因是。
-
(2) 滤渣3的主要成分是,除铁的过程中,应该先加(填“生石灰”或“双氧水”),原因是。
-
(3) 用惰性电极对过滤3得到的滤液进行电解,得到MnO2 , 写出电解过程中阳极电极反应式:。
据报道,我国氢氧燃料电池车在奥运会期间为运动员提供了可靠安全的服务。某种氢氧燃料电池的电解液为KOH溶液。下列有关电池的叙述错误的是( )
A . 正极反应式为:O2+2H2O+4e-=4OH-
B . 用该电池电解CuCl2溶液,产生2.24LCl2(标准状况)时,有0.1mol电子转移
C . 该燃料电池的总反应方程式为:2H2+O2=2H2O
D . 工作一段时间后,电解液中的KOH的物质的量不变
如图所示,其中甲池的总反应式为2CH3OH+3O2+4KOH=2K2CO3+6H2O,下列说法正确的是( )
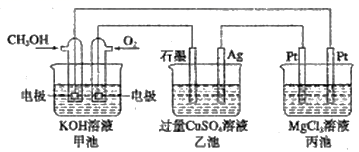
A . 甲池是电能转化为化学能的装置,乙、丙池是化学能转化电能的装置
B . 甲池通入CH3OH的电极反应式为CH3OH-6e-+2H2O=CO32-+8H+
C . 反应一段时间后,向乙池中加入一定量Cu(OH)2固体能使CuSO4溶液恢复到原浓度
D . 甲池中消耗280mL(标准状况下)O2 , 此时丙池中理论上最多产生1.45g固体
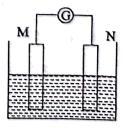
如图为原电池装置示意图:
-
(1) 若M为铜片,N为碳棒,电解质溶液为FeCl3溶液,则铜片为极(填“正”或“负”),写出正极反应式。
-
(2) 若M为Pb,N为PbO2 , 电解质为H2SO4溶液,工作时的总反应式为Pb+PbO2+2H2SO4=2PbSO4+2H2O。写出M电极反应式:;该电池工作时,M电极的质量将(填“增加”、“减小”或“不变”)。若该电池反应消耗了0.2 mol H2SO4 , 则转移电子的数目为。
-
(3) 若M、N均为铂片,电解质为KOH溶液,分别从M.、N两极通入CH4和O2 , 该电池为甲烷燃料电池,写出M电极反应式:。该电池工作一段时间后,溶液的碱性将(填“增强”、“减弱”或“不变”)。
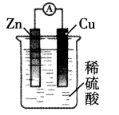
将锌片和铜片用导线连接后插入稀硫酸中,并在中间串联一个电流表,装置如图所示。
-
(1) 该装置可以将能转化为能。
-
(2) 装置中的负极材料是。
-
(3) 铜片上的电极反应式是,该电极上发生了(填“氧化”或“还原”)反应。
-
(4) 稀硫酸中的SO
 向(填“锌”或“铜”)片移动。
向(填“锌”或“铜”)片移动。
我国科学家发明了高温电解甲烷生产  的方法,原理如图所示。下列说法正确的是( )
的方法,原理如图所示。下列说法正确的是( )
 的方法,原理如图所示。下列说法正确的是( )
的方法,原理如图所示。下列说法正确的是( )
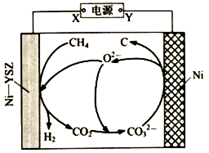
A . X为电源的负极
B . Ni电极上发生的电极反应方程式为 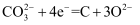 C . 电解一段时间后熔融碳酸盐中
C . 电解一段时间后熔融碳酸盐中  的物质的量增多
D . 该条件下,每产生1mol
的物质的量增多
D . 该条件下,每产生1mol  ,则生成12gC
,则生成12gC
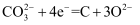 C . 电解一段时间后熔融碳酸盐中
C . 电解一段时间后熔融碳酸盐中  的物质的量增多
D . 该条件下,每产生1mol
的物质的量增多
D . 该条件下,每产生1mol  ,则生成12gC
,则生成12gC
氮氧化物(NOx)是有毒的大气污染物,研究发现,可以采用如图装置有效去除氮的氧化物,下列说法正确的是( )
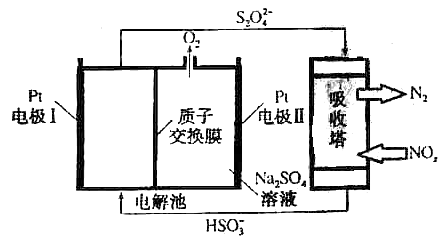
A . 电解过程中,Pt电极I上发生氧化反应
B . 电解过程中,Pt电极II上发生反应:4OH--4e-=2H2O+O2↑
C . 电解过程中,左极室pH会逐渐减小,
D . 若NOx为NO,转移1mol电子时吸收塔中消耗0.5molS2O42-
某电动汽车的锂离子电池的工作原理如图所示。下列叙述正确的是( )
A . 放电时,Li+从正极脱嵌,经过电解质溶液和离子交换膜嵌入负极
B . 放电时,正极反应式为LixC6-xe-=C6+xLi+
C . 充电时,阳极发生还原反应:  D . 电池工作时,负极材料减少a g,转移电子
D . 电池工作时,负极材料减少a g,转移电子 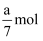
 D . 电池工作时,负极材料减少a g,转移电子
D . 电池工作时,负极材料减少a g,转移电子 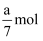
一种新型无隔膜可充电电池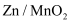 , 水系电池以锌箔、石墨毡为集流体,
, 水系电池以锌箔、石墨毡为集流体,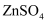 和
和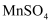 的混合液作电解质溶液,工作原理如图所示。
的混合液作电解质溶液,工作原理如图所示。
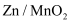 , 水系电池以锌箔、石墨毡为集流体,
, 水系电池以锌箔、石墨毡为集流体,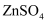 和
和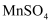 的混合液作电解质溶液,工作原理如图所示。
的混合液作电解质溶液,工作原理如图所示。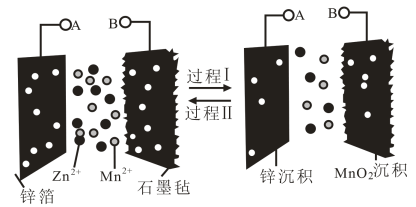
下列说法正确的是( )
A . 过程I为充电过程,a接电源的正极
B . 为增强电池效率,可向电解液中加入硫酸以增强溶液的导电性
C . 过程II为放电过程,石墨毡极的电极反应式为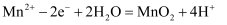 D . 放电时,当外电路转移2mol
D . 放电时,当外电路转移2mol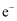 时,两电极质量变化的差值为22g
时,两电极质量变化的差值为22g
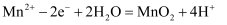 D . 放电时,当外电路转移2mol
D . 放电时,当外电路转移2mol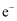 时,两电极质量变化的差值为22g
时,两电极质量变化的差值为22g
能量问题
-
(1) 火箭发射常以液态肼(N2H4)为燃料,液态过氧化氢为助燃剂。
已知:N2H4(l)+O2(g)=N2(g)+2H2O(g) ΔH=−534 kJ∙mol−1
H2O2(l)=H2O(l)+
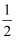 O2(g) ΔH=−98 kJ∙mol−1
O2(g) ΔH=−98 kJ∙mol−1H2O(l)=H2O(g) ΔH=44 kJ∙mol−1
试写出N2H4和液态H2O2反应生成气态水的热化学方程式:。
-
(2) 反应的自发性由焓变和熵变两个因素决定。N2(g)+O2(g)=2NO(g),已知N≡N的键能为946 kJ∙mol−1 , O=O键的键能为498 kJ∙mol−1 , N≡O的键能为630 kJ∙mol−1;该反应的ΔH=,其反应自发的原因是。
-
(3) 电动汽车的电源常以乙醇(CH3CH2OH)为燃料的固体燃料电池,以熔融的氧化物为电解质,其高温下能传导O2− , 写出负极的电极反应式。
-
(4) 以纯铜作阴极,以石墨作阳极,电解某浓度的硫酸铜溶液,阴极产物均附在电极上,通电一段时间后,关闭电源,迅速撤去电极(设阴极产物没有损耗),若在电解后的溶液中加入16.0gCuO固体,则恰好能使溶液恢复到原浓度,则整个电解过程中,所产生的气体体积为(标准状况)L。
我国科研团队成功研究出高比能量、低成本的钠离子二次电池,其工作原理如图所示。已知电池反应:Na1-xMnO2 + NaxCn NaMnO2 + nC。下列说法错误的是( )
NaMnO2 + nC。下列说法错误的是( )
 NaMnO2 + nC。下列说法错误的是( )
NaMnO2 + nC。下列说法错误的是( )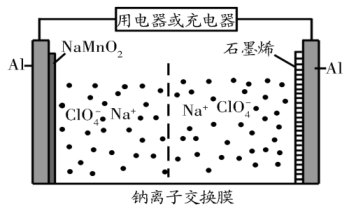
A . 电池放电过程中,NaMnO2/Al上的电势高于石墨烯/Al上的电势
B . 电池放电时,正极发生反应Na1-xMnO2 + xNa+ + xe- = NaMnO2
C . 电池充电时,外接电源的负极连接NaMnO2/Al电极
D . 电池充电时,Na+由NaMnO2/Al电极移向石墨烯/Al电极
最近更新
- 东南亚流经国家最多的河流是 ( ) A
- 下列各句中的破折号,和文中破折号作用相同的一项是( )水彩画作为舶来品,传入中国至今已有近300年历史。而水彩画真正在中
- ----Now that you like the computer so much. Why not buy it?-
- 在“研究平抛物体的运动”实验中,某同学记录了A、B、C三点,取A点为坐标原点,建立了如图所示的坐标系。平抛轨迹上的这三点
- The place _______interested me most was theChildren's Palac
- 右图是硝酸钾和氯化钠的溶解度曲线图,请根据图示信息回答: ①在 ℃时,氯化钠与硝酸钾的溶解度相等。②在t
- 我国降水量最多的地区是 ,夏季气温最高的地区是 。
- I’ll be late home because something has just at work
- 已知椭圆的离心率为,且过点. (1)求椭圆的标准方程; (2)四边形ABCD的顶点在椭圆上,且对角线AC、BD过原点O,
- 3.下列各句中,划横线的词语使用恰当的一句是( ) A.2013年,广州恒大足球队问鼎亚冠联赛,结束了中国俱乐部足球
- 81.The bridge is not open to the traffic,because it
- 如图是某一几何体的三视图,则这个几何体的体积是 ▲ .
- My bestwish is that every family _______ a large house with
- 加点字注音全对的一组是 ( ) A.哺(bǔ)育 跃(yuè)进 因为(wéi)
- 党始终代表中国先进文化的前进方向,当前我国发展先进文化的根本目标是( ) A.培育“四有”公民 B.以马克思列宁主
- Linda doesn't swim as ________as Ken.A.quickB.quickerC.quick
- 材料一:《中共中央关于推进农村改革发展若干重大问题的决定》指出:加强土地承包经营权流转管理和服务,建立健全土地承包经营权
- 下列对自然界物质的利用过程中只发生物理变化的是A.蒸发海水得到食盐 B.高温煅烧石灰石得到生石灰 C.冶炼铁
- 若=6,则=________.
- 英国人呤唎在其著作中记载:“1862年9月21日,这个美国兵痞,头一个为清军服务的美国人华尔,在率军攻打……慈溪的时候,



