第二章 化学反应速率和化学平衡 知识点题库
①反应混合物的密度不再改变 ②混合气体的平均相对分子质量不再改变
③C和D的物质的量之比为1:2 ④体系压强不再改变
⑤C的质量分数不再改变 ⑥v(A):v(C)=1:1.
 2C(g)+2D(g),在四种不同情况下的反应速率分别如下,其中反应速率最慢的是( )
2C(g)+2D(g),在四种不同情况下的反应速率分别如下,其中反应速率最慢的是( )
 2N2(g)+O2(g),其他条件不变时,容器I、Ⅱ、Ⅲ中N2O的平衡转化率随温度的变化如图所示。
2N2(g)+O2(g),其他条件不变时,容器I、Ⅱ、Ⅲ中N2O的平衡转化率随温度的变化如图所示。 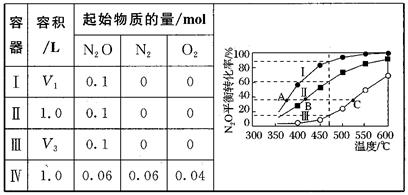
下列说法正确的是( )
-
(1) Ⅰ.脱硝:
已知:H2的燃烧热为285.8kJ/mol
N2(g)+2O2(g)=2NO2(g)△H=+133kJ/mol
H2O(g)=H2O(l)△H=-44kJ/mol
催化剂存在下,H2还原NO2生成水蒸气和其它无毒物质的热化学方程式为。
-
(2) Ⅱ.脱碳:
向2L密闭容器中加入2molCO2、6molH2 , 在适当的催化剂作用下,发生反应:CO2(g)+3H2(g)
 CH3OH(l)+H2O(l)。
CH3OH(l)+H2O(l)。下列叙述能说明此反应达到平衡状态的是__________。
A . 混合气体的平均式量保持不变 B . CO2和H2的体积分数保持不变; C . CO2和H2的转化率相等 D . 混合气体的密度保持不变 E . 1molCO2生成的同时有3molH—H键断裂 -
(3) 在T1℃时,体积为2L的恒容容器中充入物质的量之和为3mol的H2和CO,发生反应CO(g)+2H2(g)
 CH3OH(g)反应达到平衡时CH3OH的体积分数(V%)与n(H2)/n(CO)的关系如图1所示。
CH3OH(g)反应达到平衡时CH3OH的体积分数(V%)与n(H2)/n(CO)的关系如图1所示。 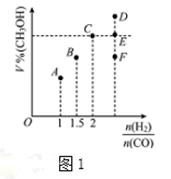
①当起始n(H2)/n(CO)=2,经过5min达到平衡,CO的转化率为0.4,则0~5min内平均反应速率V(H2)=。若此时再向容器中加入CO(g)和CH3OH(g)各0.4mol,达新平衡时H2的转化率将(选填“增大”、“减小”或“不变”);
②当起始n(H2)/n(CO)=3.5时,达到平衡状态后,CH3OH的体积分数可能是图1中的点(选填“D”、“E”或“F”)
 CH4(g)+H2O(g)。起始以物质的量之比为1∶1充入反应物,不同压强条件下,H2的平衡转化率随温度的变化情况如图所示(M、N点标记为▲)。下列有关说法正确的是( )
CH4(g)+H2O(g)。起始以物质的量之比为1∶1充入反应物,不同压强条件下,H2的平衡转化率随温度的变化情况如图所示(M、N点标记为▲)。下列有关说法正确的是( ) 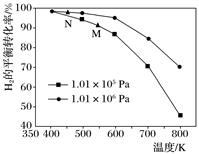
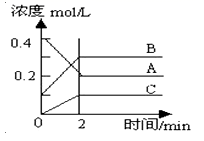
-
(1) 已知:N2O4(g)
 2NO2(g) ΔH>0 将一定量N2O4气体充入恒容的密闭容器中,控制反应温度为T1。
2NO2(g) ΔH>0 将一定量N2O4气体充入恒容的密闭容器中,控制反应温度为T1。
①下列可以作为反应达到平衡的判据是。
A.气体的压强不变 B.v正(N2O4)=2v逆(NO2) C.K不变 D.容器内气体的密度不变 E.容器内颜色不变
②t1时刻反应达到平衡,混合气体平衡总压强为p,N2O4气体的平衡转化率为75%,则反应N2O4(g)
 2NO2(g)的平衡常数Kp=(对于气相反应,用某组分B的平衡压强p(B)代替物质的量浓度c(B)也可表示平衡常数,记作Kp , 如p(B)=p·x(B),p为平衡总压强,x(B)为平衡系统中B的物质的量分数)。
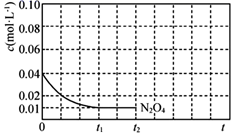
2NO2(g)的平衡常数Kp=(对于气相反应,用某组分B的平衡压强p(B)代替物质的量浓度c(B)也可表示平衡常数,记作Kp , 如p(B)=p·x(B),p为平衡总压强,x(B)为平衡系统中B的物质的量分数)。③反应温度T1时,c(N2O4)随t(时间)变化曲线如图,画出0~t2时段,c(NO2)随t变化曲线。保持其它条件不变,改变反应温度为T2(T2>T1),再次画出0~t2时段,c(NO2)随t变化趋势的曲线。
-
(2) NO氧化反应:2NO(g)+O2(g)=2NO2(g)分两步进行,其反应过程能量变化示意图如图。
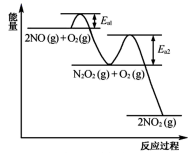
Ⅰ 2NO(g)=N2O2(g) ΔH1
Ⅱ N2O2(g)+O2(g)→2NO2(g) ΔH2
①决定NO氧化反应速率的步骤是(填“Ⅰ”或“Ⅱ”)。
②在恒容的密闭容器中充入一定量的NO和O2气体,保持其它条件不变,控制反应温度分别为T3和T4(T4>T3),测得c(NO)随t(时间)的变化曲线如图。转化相同量的NO,在温度(填“T3”或“T4”)下消耗的时间较长,试结合反应过程能量图分析其原因。
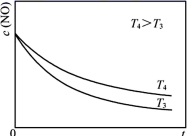
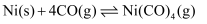 。
。 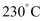 时,该反应的平衡常数
时,该反应的平衡常数 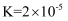 。
。 已知: 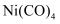 的沸点为
的沸点为  ,固体杂质不参与反应。
,固体杂质不参与反应。
第一阶段:将粗镍与  反应转化成气态
反应转化成气态 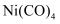 ;
;
第二阶段:将第一阶段反应后的气体分离出来,加热至 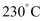 制得高纯镍。
制得高纯镍。
下列判断正确的是( )
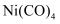 是离子化合物
B . 第一阶段,反应体系的温度应控制在
是离子化合物
B . 第一阶段,反应体系的温度应控制在 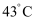 以上,以达到气化分离的目的
C . 反应达到平衡状态以后,保持体积不变通入
以上,以达到气化分离的目的
C . 反应达到平衡状态以后,保持体积不变通入  ,平衡正向移动,反应的平衡常数增大
D . 第二阶段,可以通过增大压强来提高
,平衡正向移动,反应的平衡常数增大
D . 第二阶段,可以通过增大压强来提高 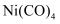 分解率
分解率
-
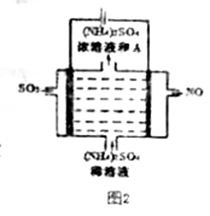
(1) 用过量的烧碱溶液吸收SO2 , 发生反应
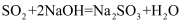 ,若向所得的
,若向所得的  溶液滴入过氧化氢溶液,则溶液的pH(填“增大”、“减小”或“不变”),发生反应的离子方程式为。
溶液滴入过氧化氢溶液,则溶液的pH(填“增大”、“减小”或“不变”),发生反应的离子方程式为。
-
(2) 研究发现,
 溶液也可以用来处理废气中的SO2 , 发生反应
溶液也可以用来处理废气中的SO2 , 发生反应  ,查阅资料可知,常温下,
,查阅资料可知,常温下, 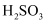 电离平衡常数:
电离平衡常数: 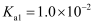 ,
, 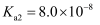 。
。 ①写出
 发生水解反应的离子方程式:;常温下,该反应的
发生水解反应的离子方程式:;常温下,该反应的  。
。②
 溶液中
溶液中  (填“>”、“<”或“=”)
(填“>”、“<”或“=”)  。
。 -
(3) 若向
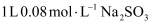 溶液中缓慢通入0.08mol Cl2 , 整个过程无气体逸出,忽略溶液体积的变化,测得溶液的pH与通入Cl2物质的量之间的变化曲线如图所示:
溶液中缓慢通入0.08mol Cl2 , 整个过程无气体逸出,忽略溶液体积的变化,测得溶液的pH与通入Cl2物质的量之间的变化曲线如图所示: 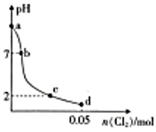
①a点pH=(填具体的数字)。
②下列说法错误的是(填标号)。
A.b点溶液中滴入紫色石蕊试液,此时原溶液不变色
B.c点溶液中存在
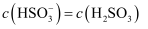
C.d点溶液中溶质只有
 、
、  和
和 
D.a点溶液中存在
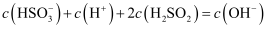
-
(4) 还可以采用多步法来处理废气中的SO2:
第1步:用过理的浓氨水吸收SO2 , 并在空气中氧化;
第2步:加入石灰水,发生反应
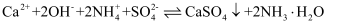 K,则K=[已知:
K,则K=[已知:  ,
,  ]。
]。
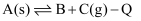 (
( 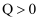 ),达到平衡。以下分析正确的是( )
),达到平衡。以下分析正确的是( )
 C . 若开始时向容器中加入1
C . 若开始时向容器中加入1 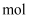 A,达到平衡时吸收热量Q
D . 缩小容器体积,重新达到平衡时,
A,达到平衡时吸收热量Q
D . 缩小容器体积,重新达到平衡时, 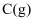 的浓度与原平衡浓度相等
的浓度与原平衡浓度相等
-
(1) 已知氮氧化物转化过程中的能量变化如图(图中表示生成2molNO2的能量变化)。1molNO氧化为NO2的焓变∆HkJ/mol。
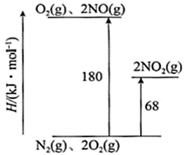
-
(2) 一定温度下,向2L恒容密闭容器中充入0.40molN2O4 , 发生反应N2O4(g)⇌2NO2(g)∆H=+Q kJ/mol,一段时间后达到平衡,测得数据如下:
时间
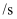
20
40
60
80
100
c(NO2)/(mol•L-1)
0.12
0.20
0.26
0.30
0.30
①
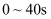 内,
内,  。
。②达平衡时,反应体系吸收的热量为
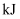 (用Q表示)。
(用Q表示)。③该温度下反应2NO2(g)⇌N2O4(g)的化学平衡常数K=。
-
(3) 近年来,地下水中的氮污染已成为一个世界性的环境问题。在金属Pt、Cu和铱(Ir)的催化作用下,密闭容器中的H2可高效转化酸性溶液中的硝态氮(
 ),其工作原理如图所示。
),其工作原理如图所示。 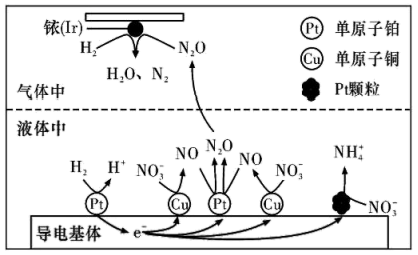
①Ir表面发生反应的方程式为。
②若导电基体上的Pt颗粒增多,造成的结果是。
①4NH3(g)+3O2(g)  2N2(g)+6H2O(g)△H1=-1266.8kJ•mol-1 K1
2N2(g)+6H2O(g)△H1=-1266.8kJ•mol-1 K1
②N2(g)+O2(g)  2NO(g)△H2=180.5kJ•mol-1 K2
2NO(g)△H2=180.5kJ•mol-1 K2
③4NH3(g)+5O2(g)═4NO(g)+6H2O(g)△H3 K3
则△H3=,K3=(用K1、K2表示)。
-
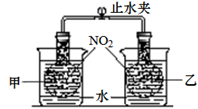
(1) 向左侧烧杯中加入NH4NO3晶体,观察甲瓶红棕色变浅,向右侧烧杯中加入CaO固体,乙瓶的红棕色变深。则该反应2NO2(g)⇌N2O4(g) ΔH0(填“>”“=”或“<”)。
-
(2) 关闭止水夹,维持温度不变,用注射器向甲瓶中充入一定量NO2 , 则此时反应2NO2(g)⇌N2O4(g)浓度熵QK(填“>”、“=”或“<”),平衡将(填“正向”“逆向”或“不”)移动,颜色比原来(填“深”“浅”或“不变”),再次达平衡时,NO2的转化率将(填“增大”“减小”或“不变”)。
-
(3) 查阅资料可知,F. Daniels等曾利用测压法在刚性反应器中研究了25℃时N2O5(g)分解反应:
Ⅰ.2N2O5(g)→4NO2(g)+O2(g) [t=∞时,N2O5(g)完全分解]
Ⅱ.2NO2(g)⇌N2O4(g)
反应体系的总压强p随时间t的变化如图所示:
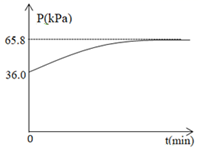
①研究表明,N2O5(g)分解的反应速率
 。则此时v(N2O5)=kPa·min−1。
。则此时v(N2O5)=kPa·min−1。②若提高反应温度至35℃,则N2O5(g)完全分解后体系压强p∞(35℃)65.8 kPa (填“大于”“等于”或“小于”),原因是。
③25℃时N2O4(g)⇌2NO2(g)反应的平衡常数Kp=kPa(Kp为以分压表示的平衡常数,计算结果保留1位小数)。
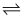 pC(g)的速率和平衡的影响,图象如下,下列判断正确的是( )
pC(g)的速率和平衡的影响,图象如下,下列判断正确的是( )
①2NO2(g)+NaCl(s)  NaNO3(s)+ClNO(g)
NaNO3(s)+ClNO(g)  H1<0平衡常数 K1
H1<0平衡常数 K1
②2NO(g)+Cl2(g)  2ClNO(g)
2ClNO(g)  H2<0平衡常数 K2
H2<0平衡常数 K2
10 分钟时反应达到平衡,测得容器内体系的压强减少 20%,10 分钟内用ClNO(g)表示 的平均反应速率v(ClNO)=7.5×10-3mol/(L·min)。下列说法正确的是( )
 2NaNO3(s)+2NO(g)+Cl2 (g)的平衡常数为K22-K1
2NaNO3(s)+2NO(g)+Cl2 (g)的平衡常数为K22-K1
 CH3COO-+H+ , 要使溶液中
CH3COO-+H+ , 要使溶液中  增大,可以采取的措施是( )
增大,可以采取的措施是( ) ①加少量烧碱固体 ②升高温度 ③加少量冰醋酸 ④加水 ⑤加少量醋酸钠固体
 )随时间(
)随时间( )变化有关实验数据见表。下列说法不正确的是( )
)变化有关实验数据见表。下列说法不正确的是( )时间 水样 | 0 | 5 | 10 | 15 | 20 | 25 |
Ⅰ( | 0.40 | 0.28 | 0.19 | 0.13 | 0.10 | 0.09 |
Ⅱ( | 0.40 | 0.31 | 0.24 | 0.20 | 0.18 | 0.16 |
Ⅲ( | 0.20 | 0.15 | 0.12 | 0.09 | 0.07 | 0.05 |
Ⅳ( | 0.20 | 0.09 | 0.05 | 0.03 | 0.01 | 0 |
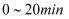 内,Ⅰ中M的平均分解速率为
内,Ⅰ中M的平均分解速率为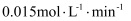 B . 其它条件相同时,水样酸性越强,M的分解速率越快
C . 在
B . 其它条件相同时,水样酸性越强,M的分解速率越快
C . 在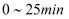 内,Ⅲ中M的分解百分率比Ⅱ大
D . 对比I、Ⅳ可知,
内,Ⅲ中M的分解百分率比Ⅱ大
D . 对比I、Ⅳ可知, 的存在可加快M的分解速率
的存在可加快M的分解速率
 2Z(g) ,一定条件下,将1 mol X和3 mol Y通入2L的恒容密闭容器中,10min后达到化学平衡,测得Y的物质的量为2.4 mol。下列说法正确的是( )
2Z(g) ,一定条件下,将1 mol X和3 mol Y通入2L的恒容密闭容器中,10min后达到化学平衡,测得Y的物质的量为2.4 mol。下列说法正确的是( )
-
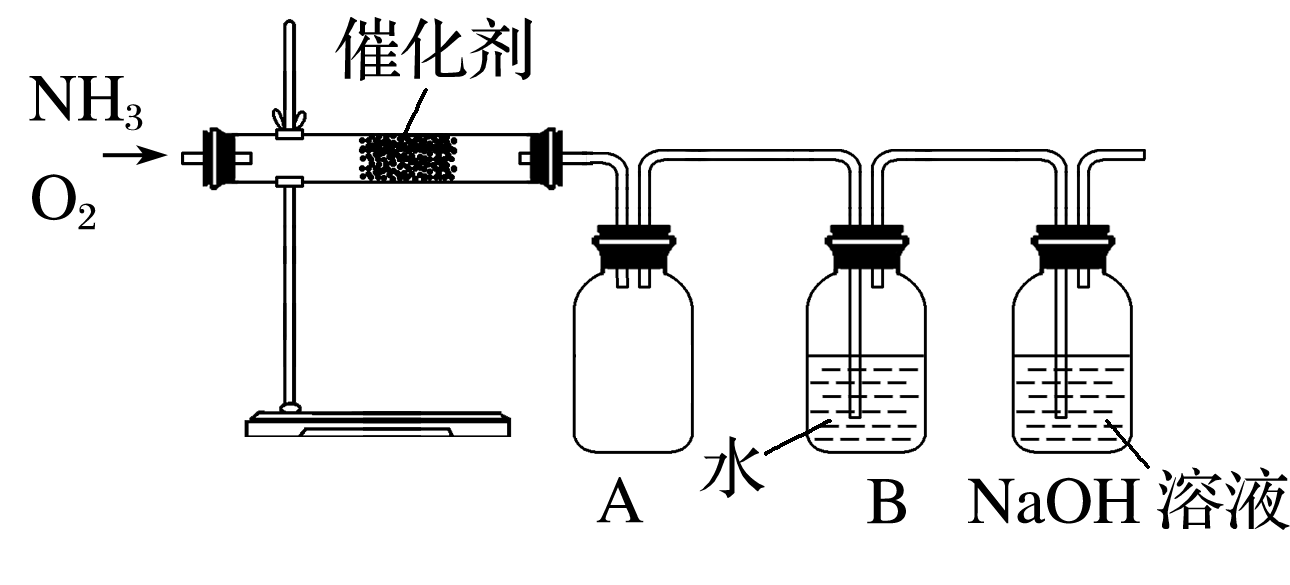
(1) 实验时先用酒精喷灯加热催化剂,然后通入反应气体,当催化剂红热后撤离酒精喷灯,催化剂始终保持红热,温度可达到700℃以上。下列图示中,能够正确表示该反应过程能量变化的是____(填字母)。A .
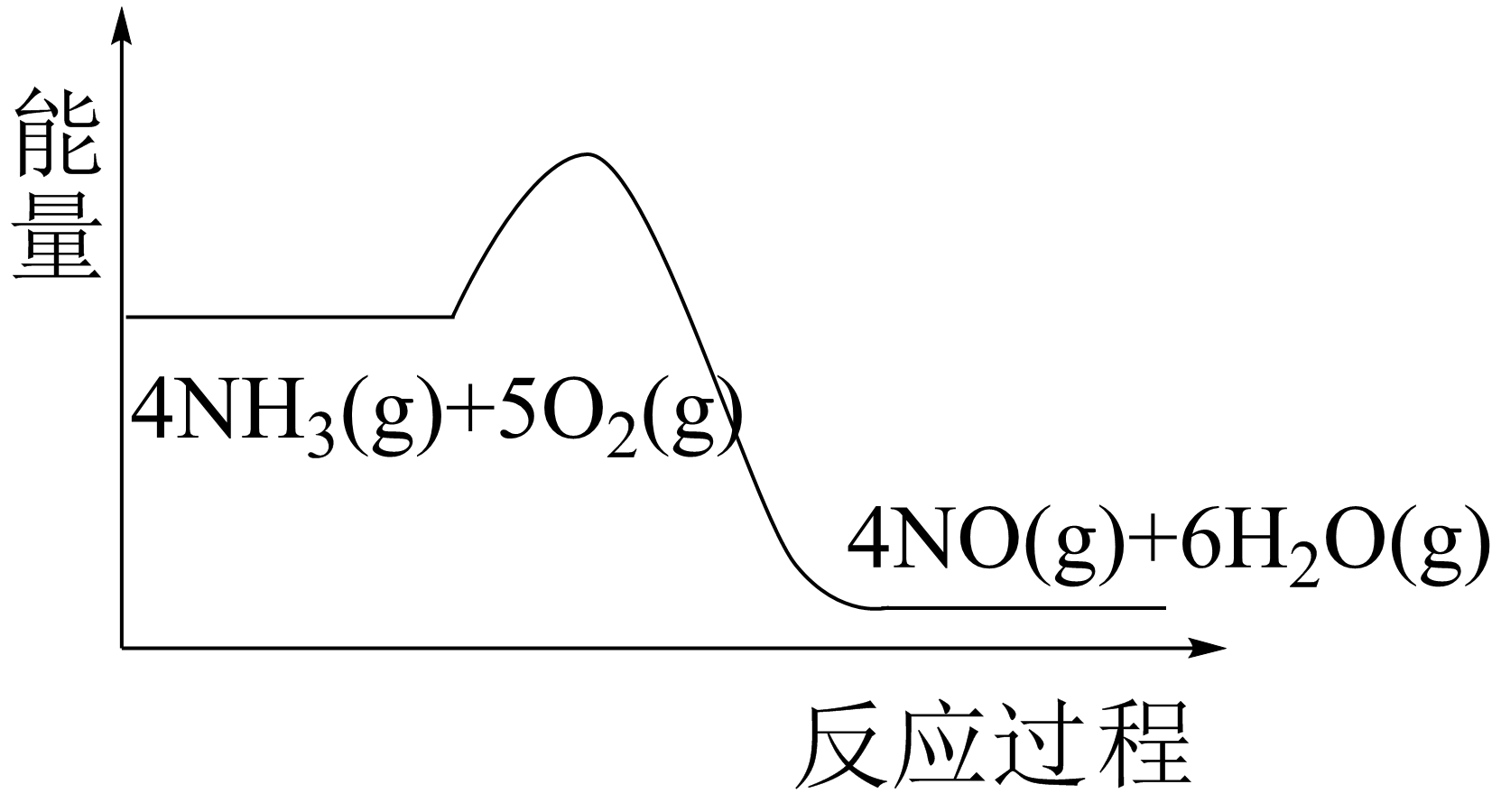 B .
B . 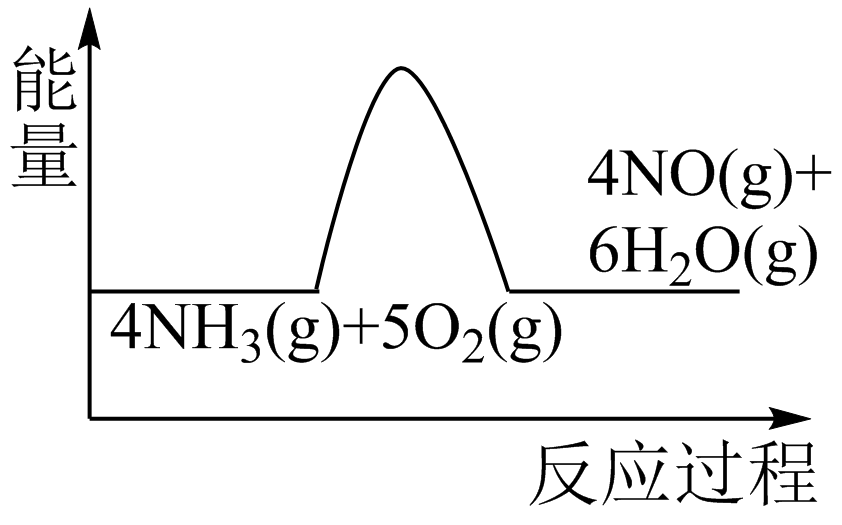 C .
C . 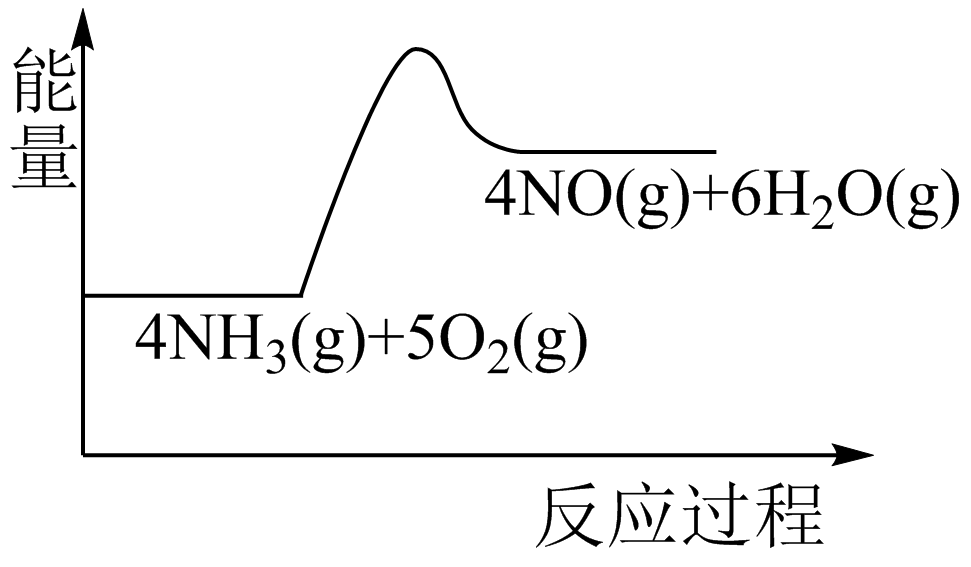
-
(2) 高温时,
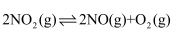 , 因此氨气与氧气反应难以生成
, 因此氨气与氧气反应难以生成 。根据下列1mol物质断键时的能量数据计算,当
。根据下列1mol物质断键时的能量数据计算,当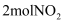 完全分解时,反应会(填“吸收”或“放出”)kJ能量。
完全分解时,反应会(填“吸收”或“放出”)kJ能量。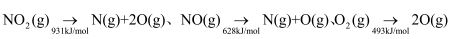
-
(3) 在2L的恒温密闭容器中,发生反应
 , 通入等物质的量的NO和
, 通入等物质的量的NO和 气体,n(NO)随时间的变化如下表:
气体,n(NO)随时间的变化如下表:t/s
0
1
2
3
4
5
n(NO)/mol
0.020
0.012
0.008
0.005
0.004
0.004
①某同学由数据推测,反应在第4s时恰好到达平衡状态。该推测(填“正确”或“错误”)
②在第5s时,
 的转化率为。
的转化率为。③容器中混合气体压强与反应开始时的压强比值为。
- 某溶液中含有HCO、SO、CO、CH3COO- 4种阴离子.若向其中加入足量的Na2O2后,溶液中离子浓度基本保持不变的
- 为学习《政治生活》 中“政治权利和义务”这一节课,小东在网上搜索到以下素材:①某中学生通过网站向本地政府的环保工作提出建
- 老师今年用7200元买一台笔记本。电子技术的飞速发展,计算机成本不断降低,每隔一年计算机的价格降低三分之一。三年后老师这
- 等比数列{an}中各项均为正数,Sn是其前n项和,且满足2S3=8a1+3a2,a4=16,则S4=() A.9
- 已知点G是△ABC的外心,是三个单位向量,且满足2,||=||.如图所示,△ABC的顶点B、C分别在x轴和y轴的非负半轴
- 个案监督即人大根据宪法原则,对人民群众反映强烈、社会影响较大的司法不公案件进行监督,是多年来地方人大及常委会在实践中探索
- 去年4月,我市开展了“北海历史文化进课堂”的活动,北海某校政教处就同学们对北海历史文化的了解程度进行随机抽样调查,并绘制
- 某学生设计了下图所示的四套装置来制取CO2,其中在制取时不能使反应随时发生或停止的装置为
- 下列有关科学研究、实验方法和实验原理的叙述,正确的是A.观察根尖分生组织细胞的有丝分裂时,解离液的作用是为了让细胞分散开
- 如图,小正方形方格的边长为1cm,则的长为___________cm.
- 甲、乙、丙三个物体用不可伸长的轻线通过轻滑轮连接,甲与地面用轻弹簧连接,如图所示。物体乙与物块丙之间的距离和物体丙到地面
- 地球上所有的生物共有一个家——生物圈,它的范围包括( ) A.大气圈、水圈和岩石圈 B.大气圈底部、水圈和岩石圈 C
- 下列气体中,本身无色但与空气接触能变成红棕色气体的是 A. CO2 B. NO C.
- What is eco-fashion? Eco-fashion is a complex phenomenon
- 求求你们,别开玩笑 [西班牙]卡何·塞拉 就像平常强盗行劫时一样,卡洛·帕里亚克诺蒙着脸,提一挺机关枪,冲进一家饭馆。饭
- 当人吃了过咸的食物时,机体细胞外液渗透压的调节过程有如下几个步骤,其正确顺序是() ①下丘脑渗透压感受器兴奋 ②大脑皮层
- 2009年8月,总书记在新疆考察时指出“民族团结是新疆各族人民的生命线,是做好新疆一切工作的重要保证。”强调民族团结是因
- 黑火药发生爆炸的反应中:S+2KNO3+3C=K2S+N2↑+3CO2↑被还原的元素是( ) A.只有N
- 阅读下面的新闻,概括优秀中学生应具备的素质。 《江南晚报》11月24日 (记者赵晖) 无锡市唯一的“校
- Many teenagers(青少年) feel that the most important people in t
 )
) )
)


