课题3 纯碱的生产 知识点题库
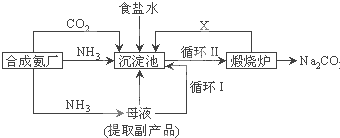
(1)上述生产纯碱的方法称 ,副产品的一种用途为 .
(2)沉淀池中发生的化学反应方程式是 .
(3)写出上述流程中X物质的分子式 .
(4)使原料氯化钠的利用率从70%提高到90%以上,主要是设计了 (填上述流程中的编号)的循环.从沉淀池中取出沉淀的操作是 .
(5)为检验产品碳酸钠中是否含有氯化钠,可取少量试样溶于水后,再滴加 .
-
(1) 纯碱是一种重要的化工原料.目前制碱工业主要有“氨碱法”和“联合制碱法”两种工艺.
①“氨碱法”产生大量CaCl2副产品,该工艺中生成CaCl2的化学反应方程式为
②“联合制碱法”中相关的化学反应方程式为
③C02是制碱工业的重要原料,请阐述“联合制碱法”与“氨碱法”中C02的来源有何不同
-
(2) 铀(U)是核反应最重要的燃料,在核反应中有重要的应用.目前已经研制成功一种螫合型离子交换树脂,它专门吸附海水中的U4+ , 而不吸附其他元素,其反应原理为 (用离子方程式表示,树脂用HR代替,下同),发生离子交换后的离子交换膜用酸处理还可再生,并得到含铀的溶液,其反应原理为
-
(3) 钢铁工业对促进经济和社会发展起了重要作用.
①不锈钢中含有的铬元素是在炼钢过程的氧吹 (填“前”或“后”)加入.
②炼钢时,加入硅、锰和铝的目的是 .
③炼铁和炼钢生产中,尾气均含有的主要污染物是 ;从环保和经济角度考虑,上述尾气经处理可用作
-
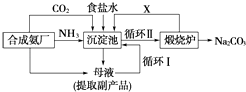
(1) 上述生产纯碱的方法称,副产品的一种用途为.
-
(2) 沉淀池中发生反应的化学方程式是.
-
(3) 写出上述流程中X物质的分子式为.
-
(4) 从沉淀池中取出沉淀的操作叫.
-
(5) 为检验产品碳酸钠中是否含有氯化钠,可取少量试样溶于水后,再滴加.
-
(6) 向母液中通氨气,加入细小食盐颗粒,冷却析出副产品,通氨气的作用有.
a.增大NH4+的浓度,使NH4Cl更多地析出
b.使NaHCO3更多地析出
c.使NaHCO3转化为Na2CO3 , 提高析出NH4Cl的纯度.
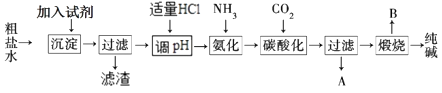
I.工业生产纯碱的工艺流程示意图如下:
-
(1) 为除去粗盐水中的Mg2+、Ca2+、SO42-等杂质离子,加入试剂顺序合理的是________。A . 碳酸钠、氢氧化钠、氯化钡 B . 碳酸钠、氯化钡、氢氧化钠 C . 氢氧化钠、碳酸钠、氯化钡 D . 氯化钡、氢氧化钠、碳酸钠
-
(2) 工业生产纯碱工艺流程中,碳酸化时产生的现象是。
-
(3) 碳酸化后过滤,滤液A最主要的成分是(填写化学式),检验这一成分的阴离子的具体方法是:。
-
(4) 煅烧制取Na2CO3在(填字母序号)中进行。
a.瓷坩埚 b.蒸发皿 c.铁坩埚 d.氧化铝坩埚
-
(5) II.纯碱在生产生活中有广泛的用途。
工业上,可能用纯碱代替烧碱生产某些化工产品。如用饱和纯碱溶液与氯气反应可制得有效成分为次氯酸钠的消毒液,其反应的离子方程式为。
-
(6) 纯碱可制备重铬酸钠(Na2Cr2O7),铬铁矿中的1molCr2O3反应时需要通入标准状况下O2的体积为。
 B . 制取碳酸氢钠
B . 制取碳酸氢钠 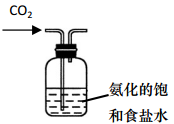 C . 分离碳酸氢钠
C . 分离碳酸氢钠 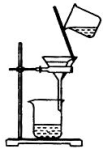 D . 干燥碳酸氢钠
D . 干燥碳酸氢钠 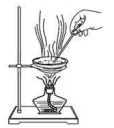
①Al2O3  NaAlO2(aq)
NaAlO2(aq)  Al(OH)3
Al(OH)3
②S  SO3
SO3  H2SO4
H2SO4
③饱和NaCl(aq) 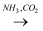 NaHCO3
NaHCO3  Na2CO3
Na2CO3
④Fe2O3 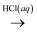 FeCl3(aq)
FeCl3(aq)  无水FeCl3
无水FeCl3
⑤MgCl2(aq) 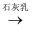 Mg(OH)2
Mg(OH)2  MgO
MgO
①NH3 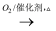 NO
NO 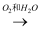 HNO3 ②浓盐酸
HNO3 ②浓盐酸  Cl2
Cl2  漂白粉
漂白粉
③MgCl2  无水MgCl2
无水MgCl2  Mg ④饱和NaCl
Mg ④饱和NaCl  NaHCO3
NaHCO3  Na2CO3
Na2CO3
⑤铝土矿  NaAlO2溶液
NaAlO2溶液  Al(OH)3
Al(OH)3  Al2O3
Al2O3  Al
Al
-
(1) (一)以一氯代乙酸钠(CH2ClCOONa)水溶液为原料,通过电解法可以制备1,2-二氯乙烷(CH2ClCH2Cl),装置如图1所示。
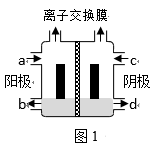
所用的离子交换膜是(填“阳”或“阴”)离子交换膜。
-
(2) 写出电解池总反应。
-
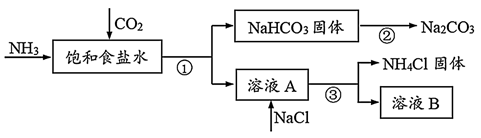
(3) (二)1940年,我国著名化工专家侯德榜先生成功冲破了“索尔维”法的技术封锁,并加以改进,用NaCl固体代替生石灰,加入母液,并联合合成氨厂一起生产出纯碱和氯化铵。这便是举世闻名的“侯氏联合制碱法”,工艺流程如图2。
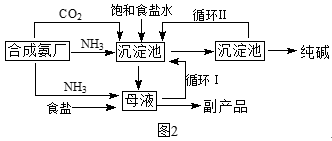
请回答:
关于合成氨反应,下列说法合理的是___。
A . 反应体系中一般用V2O5作催化剂 B . 因为该反应ΔS小于零,所以反应的ΔH一定也小于零 C . 因为该反应的ΔS小于零,所以反应的压强控制越高越好 D . 该反应往往控制在500℃左右,是因为该温度下反应物转化率最高 -
(4) 一定温度下合成氨反应的平衡常数K=48。若在该温度下,在9L的恒容容器中投入1mol氮气和3mol氢气进行反应,则氨气的平衡产率y=;若氮气和氢气的物质的量之比为n∶1,相应平衡体系中氨气的物质的量分数为x,请在图3中绘制x随n变化的示意图(计算时不计副反应)。
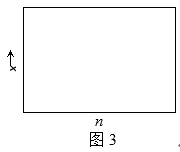
-
(5) 侯氏制碱法最大的优点是使原料氯化钠的利用率从70%提高到90%以上,主要是设计了(填上述编号)的循环。
-
(6) 关于侯氏联合制碱法,下列说法合理的是_____。A . 往沉淀池中先通入CO2再通入氨气的目的是提高NaHCO3的产量 B . 往母液中加入食盐的目的是使NaHCO3更多地析出 C . 从母液中经过循环Ⅰ进入沉淀池的主要是Na2CO3、NH4Cl和氨水 D . 往母液中通氨气目的仅仅是增大NH4+的浓度,使NH4Cl更多地析出
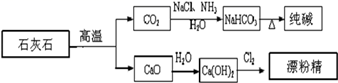
下列说法正确的是( )
| 氨碱法 | 联合制碱法 | ||
| A | 原料 | 食盐、氨气、生石灰 | 食盐、氨气、二氧化碳 |
| B | 副产物 | 氯化钙 | 氯化铵 |
| C | 循环物质 | 氨气、二氧化碳 | 氯化钠 |
| D | 评价 | 原料易得、设备简单、能耗低 | 原料利用率高、废弃物少 |
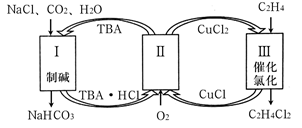
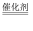 C2H4Cl2+2CuCl
C2H4Cl2+2CuCl

已知:NH3极易溶于水生成NH3•H2O,NH3•H2O可电离产生NH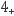 和OH-。下列说法不正确的是( )
和OH-。下列说法不正确的是( )
-
(1) Ⅰ.NaHCO3 的制备
实验流程及实验装置图如下:
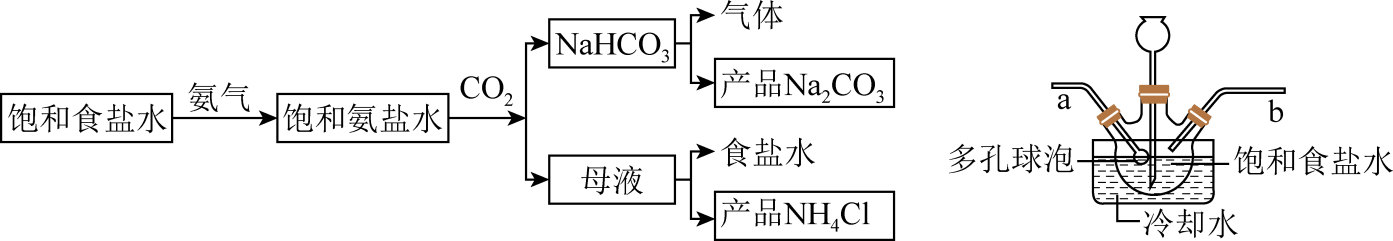
回答下列问题:
a导管末端多孔球泡的作用。
-
(2) b中通入的气体是, 写出实验室制取该气体的化学方程式。
-
(3) 生成NaHCO3的总反应的化学方程式为。
-
(4) Ⅱ.Na2CO3中NaHCO3含量测定
i.称取产品2.500g,用蒸馏水溶解,定容于250mL容量瓶中:
ii.移取25.00mL上述溶液于锥形瓶,加入2滴指示剂M,用0.1000mol·L-1盐酸标准溶液滴定至溶液由浅红色变无色(第一滴定终点), 消耗盐酸V1mL;
iii.在上述锥形瓶中再加入2滴指示剂N,继续用0.1000mol·L-1盐酸标准溶液滴定至终点(第二滴定终点),又消耗盐酸V2mL;
iv.平行测定三次,V1 平均值为22.25,V2平均值为23.51。
回答下列问题:
指示剂N为, 第二滴定终点的现象是。
-
(5) Na2CO3中NaHCO3的质量分数为 ( 保留三位有效数字)。
-
(6) 第一滴定终点时,某同学仰视读数,其他操作均正确,则NaHCO3质量分数的计算结果(填“偏大”“偏小”或“无影响”)。
已知:NaCl、NH4HCO3、NaHCO3、NH4Cl四种盐在不同温度下的溶解度如下表所示:
温度溶解度(g) 物质 | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | 60℃ | 70℃ |
NaCl | 35.8 | 36.0 | 36.3. | 36.6 | 37.0 | 37.3 | 37.8 |
NH4HCO3 | 15.8. | 21.0 | 27.0 | 一 | 一 | — | — |
NaHCO3 | 8.15 | 9.6 | 11.1 | 12.7 | 14.45 | 。16.4 | 一 |
NH4Cl | 33.3 | 37.2 | 41.1 | 45.8 | 50.4 | 55.2 | 60.2 |
回答下列问题:
-
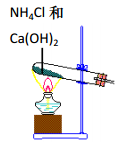
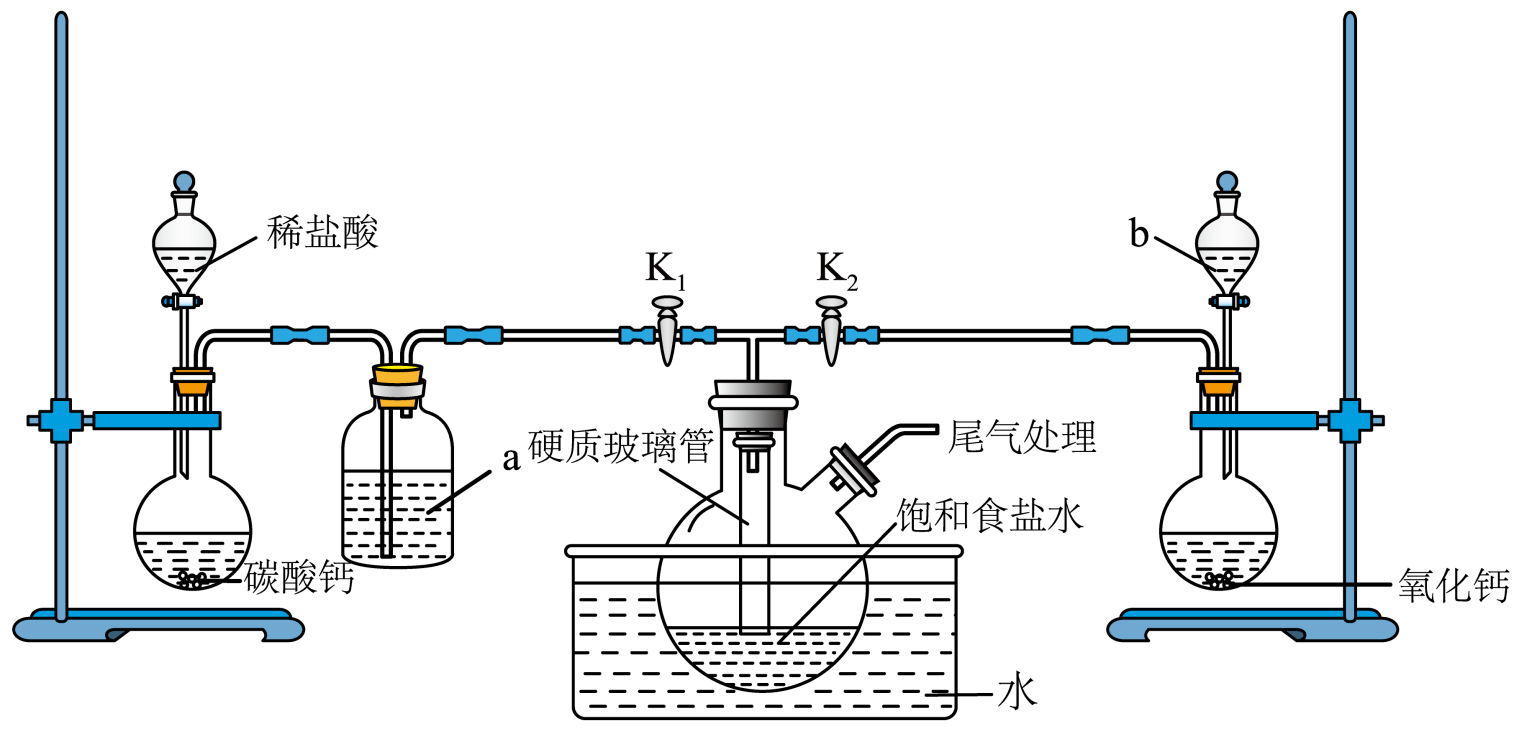
(1) 试剂b的名称是,试剂a的作用是。
-
(2) 实验时应先打开(填“K1”或“K2”)开关,持续通入气体一段时间后,关闭此开关,再打开另一开关。硬质玻璃管的作用是。
-
(3) 反应一段时间后,双颈烧瓶中观察到的实验现象为。该反应一般控制在30~35℃下进行,温度不宜过高的主要原因是(用化学方程式表示)。
-
(4) 实验结束后,过滤双颈烧瓶中的混合物,滤渣经灼烧得纯碱,并回收滤液中的NH4Cl。为促进滤液中NH4Cl析出,需向滤液中通入NH3并加入一定量NaCl固体,原因是。
-
(5) 制得的纯碱中混有NaHCO3和少量不与盐酸反应的杂质。该小组为测定其中NaHCO3的含量,取ag样品于试管中加水完全溶解,加入几滴酚酞溶液,用cmol·L-1的盐酸滴定至溶液由红色变为浅红色,消耗盐酸V1mL;再加1~2滴甲基橙指示剂,继续用盐酸滴定至溶液由黄色变为橙色,又消耗盐酸V2mL。则纯碱样品中NaHCO3质量分数为。
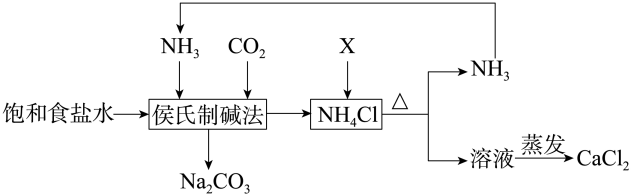
有关该制碱工艺描述错误的是( )
- 下面四个命题: ①若直线a,b异面,b,c异面,则a,c异面; ②若直线a,b相交,b,c相交,则a,c相交; ③若a∥
- 1872年日本政府发布告谕:“苟有国则有兵备,有兵备则人民不得不各就其役。”这最能说明 A.日本实行征兵制 B.日本以武
- 乌鸦喝水的故事大家都很熟悉。口渴的乌鸦将地上的小石块逐个投入瓶内,使水面不断上升,升到瓶口,乌鸦喝到了水。如图6所示,小
- 阅读下面的文字,完成下题。 国学大师汤一介 “当一个民族正处在伟大复兴的前夜时,它必须回顾自己的历史文化,从中吸取力量,
- 一个地区的自然增长率是由 决定的( ) A.出生率 B.死亡率 C.出生率和死亡
- 将酒精灯的灯芯拨得松散一些,可使燃烧更旺,其原因是A .减少酒精灯内酒精的挥发B .降低可燃物的着火点C .增大可燃物与
- 一个多边形的内角和等于一个三角形的外角和的2倍,则这个多边形的边数是 .
- 点在第三象限,则m ( )A. B. C. D.
- 下列反应不属于化合反应的是() A.铁+硫酸→硫酸亚铁+氢气 B.氧气+一氧化碳二氧化碳 C.氢气+氯气氯化氢 D.氧化
- 某自来水厂的蓄水池存有400吨水,水厂每小时可向蓄水池中注水60吨,同时蓄水池又向居民小区不间断供水,t小时内供水总量为
- 夏天到了,部分池塘、湖泊会出现腥味泡沫状漂浮物,这是由于( )的大量繁殖。 A.种子植物 B.蕨类植物
- 垒球运动的诞生完全是处于一种需要,由于恶劣的天气和拥挤的城市,第29届奥运会垒球比赛于2008年8月12日~21日在北京
- 阅读下文,回答5—8题。
- 下表为元素周期表的一部分,请参照元素①-⑧在表中的位置,用化学用语回答下列问题: 族 周期 IA 0 1 ①
- 下图表示细胞中蛋白质合成的部分过程,相关叙述不正确的是( ) A.甲分子上有个m密码子,乙分子上有个n密码子,若不
- 中学化学中几种常见物质的转化关系如下:将D溶液滴入沸水中可得到以F为分散质的红褐色液体。请回答下列问题:(1)写出D溶液
- I _________ singing to dancing. A.like B.enjoy
- 如图所示,带支架的平板小车沿水平面向左做直线运动,小球A用细线悬挂于支架前端,质量为m的物块B始终相对于小车静止地摆放在
- 探究创新,请你完成实验设计方案 某实验小组的同学要探究甲状腺激素对蝌蚪变态发育的影响,请你帮他们作出假设,并设计实验方案
- 曲线在点处的切线方程为 。



