第三节 化学反应的速率和限度 知识点题库
①C的生成速率与C的分解速率相等
②单位时间内生成amolA,同时生成3amolB
③A,B,C的浓度不再变化
④反应物的转化率不再变化
⑤混合气体的压强不再变化
⑥混合气体的物质的量不再变化
⑦混合气体的密度不再变化
⑧A,B,C,D的分子数之比为1:3:2:2.
①单位时间内生成n mol O2 , 同时生成2n mol NO2
②单位时间内生成n mol O2 , 同时生成2n mol NO
③用NO2、NO、O2的物质的量浓度变化表示的反应速率的比为2:2:1
④混合气体的压强不再改变
⑤混合气体的颜色不再改变 ⑥混合气体的平均摩尔质量不再改变.
图① 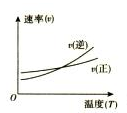 图②
图② 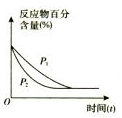 图③
图③ 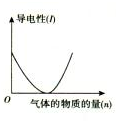 图④
图④ 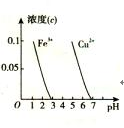
-
(1) 燃煤发电厂常利用反应2CaCO3(s)+2SO2(g)+O2(g)=2CaSO4(s)+2CO2(g);ΔH=-681.8kJ·mol−1对煤进行脱硫处理来减少SO2的排放。对于该反应,在T℃时,借助传感器测得反应在不同时间点上各物质的浓度如下:
时间/min
浓度/mol·L−1
0
10
20
30
40
50
O2
1.00
0.79
0.60
0.60
0.64
0.64
CO2
0
0.42
0.80
0.80
0.88
0.88
①0~10min内,平均反应速率v(O2)=;
②30min后,只改变某一条件,反应重新达到平衡。根据上表中的数据判断,改变的条件可能是(填字母)。
A.加入一定量的粉状碳酸钙 B.通入一定量的O2
C.适当缩小容器的体积 D.加入合适的催化剂
-
(2) NOx的排放主要来自于汽车尾气,有人利用反应C(s)+2NO(g)
 N2(g)+CO2(g) ΔH=-34.0kJ·mol−1 , 用活性炭对NO进行吸附。已知在密闭容器中加入足量的C和一定量的NO气体,保持恒压测得NO的转化率随温度的变化如图所示:
N2(g)+CO2(g) ΔH=-34.0kJ·mol−1 , 用活性炭对NO进行吸附。已知在密闭容器中加入足量的C和一定量的NO气体,保持恒压测得NO的转化率随温度的变化如图所示: 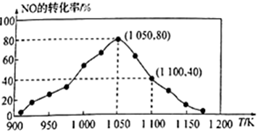
由图可知,1050K前反应中NO的转化率随温度升高而增大,其原因为,在1050K、1.1×106Pa时,该反应的化学平衡常数Kp=(已知:气体分压(P分)=气体总压(Pa)×体积分数)
-
(3) 为避免汽车尾气中的有害气体对大气的污染,需给汽车安装尾气净化装置。在净化装置中CO和NO发生反应2NO(g)+2CO(g)
 N2(g)+2CO2(g) ΔH=-746.8kJ·mol−1 , 生成无毒的N2和CO2。实验测得,v正=k正·c2(NO)·c2(CO),v逆=k逆·c(N2)·c2(CO2)(k正、k逆为速率常数,只与温度有关)。
N2(g)+2CO2(g) ΔH=-746.8kJ·mol−1 , 生成无毒的N2和CO2。实验测得,v正=k正·c2(NO)·c2(CO),v逆=k逆·c(N2)·c2(CO2)(k正、k逆为速率常数,只与温度有关)。 ①达到平衡后,仅升高温度,k正增大的倍数 (填“>”“<”或“=”)k逆增大的倍数。
②若在1L的密闭容器中充入1mol CO和1mol NO,在一定温度下达到平衡时,CO的转化率为40%,则
 = 。
= 。
|
物质 时间 |
X |
Y |
Z |
Q |
|
起始/mol |
0.7 |
1 |
||
|
2 min末/mol |
0.8 |
2.7 |
0.8 |
2.7 |
|
3 min末/mol |
0.8 |
已知2 min内v(Q)=0.075 mol·L-1·min-1 , v(Z) ∶v(Y) =1 ∶2 ,
-
(1) 试确定以下物质的物质的量:起始时n(Y)=,n(Q)=;
-
(2) 方程式中m=,n=,p=,q=;
-
(3) 用Z表示2 min内的反应速率;
-
(4) 2 min时,Z的转化率为。
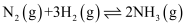 达到平衡状态的标志是( )
达到平衡状态的标志是( ) ① 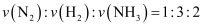 ②各组分的物质的量不变 ③体系的压强不再发生变化 ④混合气体的密度不变 ⑤体系的温度不再发生变化 ⑥
②各组分的物质的量不变 ③体系的压强不再发生变化 ④混合气体的密度不变 ⑤体系的温度不再发生变化 ⑥  ⑦3mol H-H键断裂的同时有2mol N-H键也断裂
⑦3mol H-H键断裂的同时有2mol N-H键也断裂
 4Fe (OH)3+8OH -+3O2↑。在 pH=4.7 的溶液中,配成 c (K2FeO4)=1.0×10-3mol·L-1 试样,分别置于 20-60℃的恒 温水浴中,测定 K2FeO4 总量的变化如图,纵坐标为试样的浓度, 则下列说法错误的是( )
4Fe (OH)3+8OH -+3O2↑。在 pH=4.7 的溶液中,配成 c (K2FeO4)=1.0×10-3mol·L-1 试样,分别置于 20-60℃的恒 温水浴中,测定 K2FeO4 总量的变化如图,纵坐标为试样的浓度, 则下列说法错误的是( ) 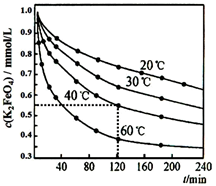
 2C(g),达到平衡状态的标志( )
2C(g),达到平衡状态的标志( )
| 选项 | 实验 | 现象 | 结论 |
| A | 向FeCl3溶液中通入足量的H2S | 生成两种沉淀 | Fe3+的氧化性强于S |
| B | 向浓度均为0.1 mol:L-1的CuSO4和MgSO4混合溶液中滴加少量NaOH溶液 | 先出现浅蓝色沉淀 | Cu(OH)2的溶度积比Mg(OH)2的小 |
| C | 向FeCl3溶液中滴入几滴30%的H2O2溶液 | 有气体产生,一段时间后,FeCl3溶液颜色加深 | Fe3+能催化H2O2 分解,且该分解反应为放热反应 |
| D | 铜粉加入稀硫酸中,加热;再加入少量硝酸钾固体 | 加热时无明显现象,加入硝酸钾后溶液变蓝 | 硝酸钾起催化作用 |

-
(1) 将NO、CO转化为2种无毒气体的化学方程式是。
-
(2) 反应开始至10 min,v(NO)=mol/(L•min),NO的转化率为,此温度下达到平衡常数为。
-
(3) 下列说法正确的是。
a.新型催化剂可以加快NO、CO的转化
b该反应进行到10 min时达到化学平衡状态
c.平衡时CO的浓度是0.4 mol/ L
①体系的温度不再改变; ②体系的压强不再改变;
③混合气体密度不再改变; ④混合气体的平均摩尔质量不再改变;
⑤N2和H2的浓度之比达到1:3; ⑥v(N2)正反应=3v(H2)逆反应;
⑦2v(H2)正反应=3v(NH3)逆反应; ⑧每有一根N≡N键断裂就有6根N-H键形成。
 BaS(s)+4CO(g),CO的平衡浓度(mol/L)的对数lgc(CO)与温度的倒数
BaS(s)+4CO(g),CO的平衡浓度(mol/L)的对数lgc(CO)与温度的倒数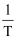 的关系如图所示,下列说法中正确的是( )
的关系如图所示,下列说法中正确的是( )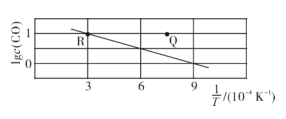
 K时,反应的平衡常数为1
D . 温度不变,将R点状态的容器体积扩大,重新达到平衡时,气体的压强减小
K时,反应的平衡常数为1
D . 温度不变,将R点状态的容器体积扩大,重新达到平衡时,气体的压强减小
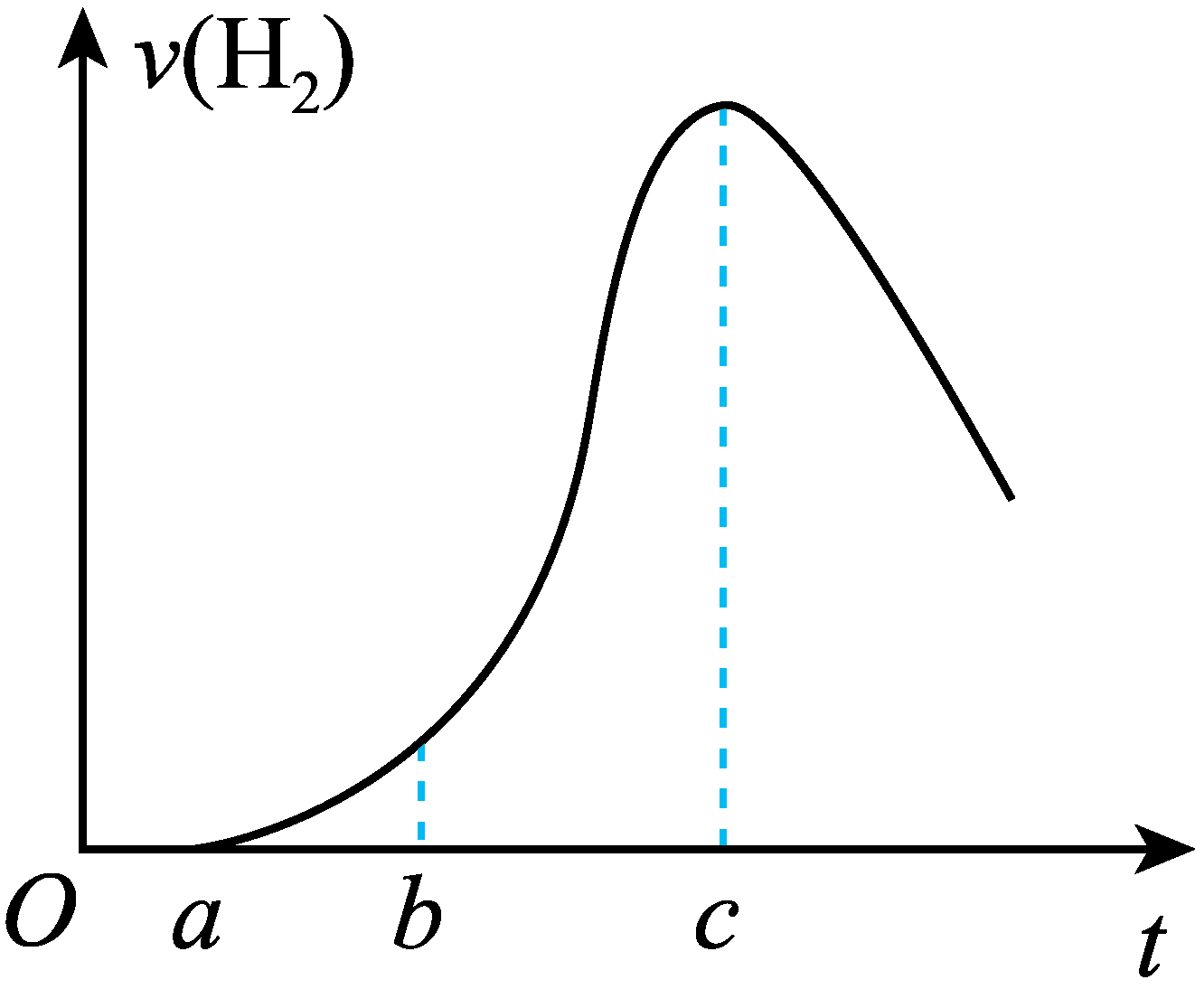
①有气体参加的化学反应,若增大压强(即缩小反应容器的体积),可增加活化分子数目,从而使反应速率增大
②其他条件不变,温度越高,化学反应速率越快
③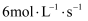 的反应速率一定比
的反应速率一定比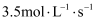 的反应速率大
的反应速率大
④其他条件不变,升高温度能增大反应物分子中活化分子的百分数
⑤恒温时,增大压强,化学反应速率一定加快
⑥增大反应物浓度,可增大活化分子的百分数,从而使单位时间内有效碰撞次数增多
⑦如果使用催化剂,可使反应物所有分子间的碰撞机会增多,则反应速率加快
⑧如果使反应物分子的能量增加,则活化分子百分数增大,有效碰撞次数增多
⑨如果活化分子百分数未变,但增加单位体积内活化分子数,可以使有效碰撞次数增多⑩如果使气体分子间距离减小,可以使所有的活化分子间的碰撞都成为有效碰撞
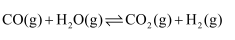 , 下列能判断该反应已达到化学平衡状态的标志是( )
, 下列能判断该反应已达到化学平衡状态的标志是( )
 和
和 的物质的量浓度之和不再变化
B . 混合气体的分子总数不再变化
C . 混合气体的密度不再变化
D .
的物质的量浓度之和不再变化
B . 混合气体的分子总数不再变化
C . 混合气体的密度不再变化
D .  和
和 的物质的量之比不再变化
的物质的量之比不再变化
- 阅读下面语段,按要求回答问题: 从古至今都没有长生不老的人,但每个人的寿命都极不相同,从生物学和医学上来看,人类的寿命应
- 海洋里由浅入深依次生长着绿藻、褐藻、红藻,影响植物这样分布的主要因素是( ) A.阳光 B
- 北京中关村的科技人员计划去印度参观、学习、交流经验,他们最好去的城市是A.新德里B.加尔各答C.孟买D.班加罗尔
- 是平面上不共线三点,向量,,设P为线段AB垂直平分线上任意一点,向量.若,,则的值是
- 如图,在宽为20m,长为30m的矩形地面上修建两条同样宽的道路,余下部分作为耕地.已知耕地的面积为551m2则道路的宽为
- X、Y两元素是同周期的主族非金属元素,如果X原子半径比Y大,下面说法正确的是() A.X的最高价氧化物对应的水化物的酸性
- —Do you go to work by bus? —________. A.Yes,but I did
- 两个分别带有电荷量﹣Q和+5Q的相同金属小球(均可视为点电荷),固定在相距为r的两处,它们间库仑力的大小为F,两小球相互
- A、B均为原子序数为1﹣20的元素,已知A的原子序数为n,A2+离子比B2﹣离子少8个电子,则B的原子序数是( )
- 下列与有机物的结构、性质有关的叙述正确的是 A.乙烯、氯乙烯、聚乙烯均可使酸性高锰酸钾溶液褪色 B.乙酸与乙醇可以发生酯
- 在图6“海水等温线示意”中,箭头表示洋流流向,正确的是 A.①是暖流,位于北半球 B.①是寒流,位于南半球 C.②是寒流
- 2008年9月27日,神舟七号航天员翟志刚完成中国历史上第一次太空行走,他相对地球行走了5 100 千米路程,用科学记数
- 将Ba(NO3)2、NaOH、H2SO4、K2CO3四种无色溶液编号甲、乙、丙、丁,并两两混合,现象如下表所示:下列选项
- 右图为我国某地5月5日前后几天的天气变化资料统计图,回答6~7题。6.这次降水的形成原因是( ) A
- 绿茶中的单宁酸具有抑制血压上升、清热解毒、抗癌等功效,其化学式为C76H52O46,下列说法不正确的是
- 使带电的金属小球靠近不带电的验电器,验电器的箔片张开.下列各图表示验电器上感应电荷的分布情况,正确的是
- 下列所述情景中手作为受力物体的是:A、手拍桌子,手感到疼 B、手将石块举高C、用手
- 关于经线和纬线的叙述正确的是( ) A.所有经线都与本初子午线平行 B.纬度越低,纬线越短 C.经线
- 15.补写出下列句子中的空缺部分。 (1)《荆轲刺秦王》中通过众宾客的神态表现出送行气氛的语句是:__ ___
- 下图是在显微镜下观察到的人血细胞图,请分析回答:(1)在显微镜下观察人血涂片时,视野中呈红色、数量最多的是[ ]



