第一节 金属的化学性质 知识点题库
把铝粉与Fe3O4的混合物,分为两等份。前一份在高温下恰好完全反应,之后将生成物与足量盐酸充分反应;后一份直接加入足量NaOH溶液充分反应。前后两种情况下生成的气体在同温同压下的体积比是( )
A . 4:3
B . 3:4
C . 9:8
D . 1:1
下列有关物质的性质或应用的说法中正确的是( )
A . 铝合金是一种混合物,它比纯铝的熔点高
B . 高炉中的主要反应是高温下焦炭和氧化铁直接作用炼出生铁
C . 铁钉放在浓硝酸中浸泡后,再用蒸馏水冲洗,然后放入CuSO4溶液中不反应,说明铁钉表面形成了一层致密稳定的氧化膜
D . 电解从海水中得到的氯化镁溶液可获得金属镁
下列关于金属的叙述中正确的是( )
A . 常温下所有的金属都是固态
B . 金属具有导电、导热和延展性
C . 金属元素的原子只有还原性,离子只有氧化性
D . 所有金属元素都以化合态存在于自然界
将一定质量的Al、Fe混合物加入到足量的盐酸中,充分反应后得到标准状况下的氢气8.96L;如果将等质量的该混合物加入到足量的NaOH溶液中,充分反应后得到标准状况下的氢气6.72L.
(1)写出与碱反应涉及的化学方程式: ;
(2)混合物中Al和Fe的质量分别为 和 ;
(3)当混合物与盐酸反应时,转移电子数为 mol;与NaOH溶液反应时转移电子数为 mol.
铁、铜混合粉末18.0g加入到100ml 5.0mol/LFeCl3溶液中,剩余固体质量为3.2g.下列说法正确的是( )
A . 剩余固体是铁、铜混合物
B . 原固体混合物中铜的质量是9.6g
C . 反应后溶液中n(Fe3+)=0.10 mol
D . 反应后溶液中n(Fe2+)+n(Cu2+)=0.75 mol
将Fe、Cu、Fe2+、Fe3+和Cu2+盛于同一容器中充分反应,反应后Fe有剩余,则容器中其它存在的单质或离子只能是( )
A . Cu、Fe3+
B . Fe2+、Fe3+
C . Cu、Cu2+
D . Cu、Fe2+
下列元素在自然界中仅以化合态存在的是( )
①Si ②Al ③Cl ④Fe ⑤Na.
A . ①②⑤
B . ①②
C . ①②③
D . ①②③④⑤
下列反应中,反应条件、加液顺序、反应物用量或浓度等改变时,反应产物均不发生变化的是( )
A . 钠与氧气反应
B . 盐酸和碳酸氢钠溶液
C . 铜与硝酸反应
D . 氯化铝溶液和氢氧化钠溶液反应
下列单质或化合物性质的描述正确的是( )
A . 食品包装中常放入有硅胶和铁粉的小袋,防止食物受潮和氧化变质
B . Na2O、Na2O2组成元素相同,与CO2反应产物也相同
C . SiO2与酸、碱均能反应,属于两性氧化物
D . 新制氯水显酸性,向其中滴加少量紫色石蕊试液,充分振荡后溶液呈红色
下列有关金属的说法中正确的是( )
A . 生铁比纯铁抗腐蚀能力更强
B . 青铜、不锈钢、硬铝都是合金
C . 性质越活泼的金属越早被人类冶炼和使用
D . 单质铝在空气中比较耐腐蚀,所以铝是不活泼金属
下列说法正确的是( )
A . 向Na2CO3溶液中加硫酸,有气泡产生,说明非金属性S>C
B . 酸性:HBr> HI,说明非金属性Br>I
C . 金属性Na>Cu,钠投入硫酸铜溶液会析出红色沉淀
D . 金属性Al>Cu,常温下,铝与同浓硫酸反应比铜更剧烈
某含有Na2O杂质的Na2O2试样,一个化学实验小组利用H2O与Na2O2的反应来测定该样品的纯度。可供选择的装置如下:
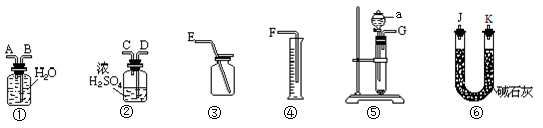
请回答下列问题:
-
(1) 用上述装置可以组装一套最简单的测定过氧化钠样品纯度的实验装置。所选用装置的连接顺序应是(填各接口的字母,连接胶管省略)。
-
(2) 写出实验中Na2O2发生反应的化学方程式并用双线桥表示电子转移数。将Na2O2投入滴有酚酞的水中现象是
-
(3) 用上述实验后所得溶液配制成浓度为1.0mol/L的溶液,回答下列问题。
①向400mL该溶液中通入0.3molCO2 , 则所得溶液中HC
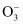 和
和  的物质的量浓度之比约为。
的物质的量浓度之比约为。A.1:3 B.1:2 C.2:1 D.3:1
②将上述溶液蒸发结晶得到Na2CO3和NaHCO3固体混合物,下列选项中不能准确测定混合物中Na2CO3质量分数的是。
a.取ag混合物充分加热,在干燥器中冷却至室温,减重bg
b.取ag混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得bg固体
c.取ag混合物与足量稀硫酸充分反应,逸出气体用碱石灰吸收,增重bg
d.取ag混合物与足量Ba(OH)2溶液充分反应,过滤、洗涤、烘干,得bg固体
将镁铝合金溶于 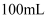 稀硝酸中,产生
稀硝酸中,产生 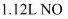 气体(标准状况),向反应后的溶液中加入
气体(标准状况),向反应后的溶液中加入  溶液,产生沉淀情况如图所示。
溶液,产生沉淀情况如图所示。
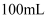 稀硝酸中,产生
稀硝酸中,产生 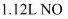 气体(标准状况),向反应后的溶液中加入
气体(标准状况),向反应后的溶液中加入  溶液,产生沉淀情况如图所示。
溶液,产生沉淀情况如图所示。 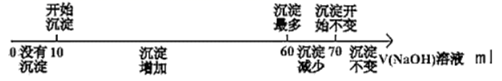
-
(1) 反应过程中转移电子物质的量为
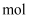 。
。
-
(2) 计算氢氧化钠溶液物质的量浓度(写出简要计算过程)
下列说法正确的是( )
A . Fe与水蒸气高温下反应生成Fe(OH)2和H2
B . 铜长期置于潮湿的空气中会与空气反应生成Cu2(OH)2CO3
C . Na可以从硫酸铜溶液中置换出铜单质
D . 侯氏制碱法原理是向氯化钠饱和溶液中先通CO2 , 再通NH3
探究Na2O2与水的反应,实验如图:
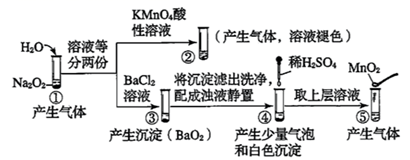
已知:H2O2⇌H++HO  、HO
、HO  ⇌H++O
⇌H++O 
下列分析错误的是( )
A . ①、⑤中产生的气体能使带火星的木条复燃
B . ①、④中均发生了氧化还原反应和复分解反应
C . ②、⑤中KMnO4与MnO2的作用不同,产生气体的量也不同
D . 沉淀经过滤、洗涤、干燥后称量:④中反应后的沉淀质量小于③中所得沉淀的质量
为探究钠的部分性质,设计实验操作如下:
①向如图所示的试管中加入苯(已知苯的密度为0.86 g·cm-3 , 苯不溶于水);②拔出大头 针,使Na(密度为0.97 g·cm-3)落入苯中(钠与苯不反应);③从长颈漏斗中加入MgCl2溶液(密度约为1 g·cm-3)。下列说法中正确的是( )
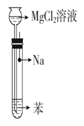
A . 把MgCl2溶液加入苯中,MgCl2溶液在上层
B . 钠一直停留在苯层不发生反应
C . Na在MgCl2溶液与苯的界面处反应,并上下跳动直至消失,下层有白色沉淀产生
D . Na在MgCl2溶液底部四处游动,MgCl2溶液中有白色沉淀产生
现有三种常见元素的性质或结构如下表:
|
X |
与Al同周期,金属性最强 |
|
Y |
与Al同周期,最外层电子数是最内层电子数的3倍 |
|
Z |
常温下单质为双原子分子,为黄绿色有毒气体 |
|
W |
单质紫黑色,遇淀粉溶液显蓝色 |
-
(1) X元素的名称是;Y的原子结构示意图是;W在元素周期表中的位置是;
-
(2) 请写出Z的单质与X元素最高价氧化物所对应水化物的溶液在常温下反应的离子方程式;
-
(3) 判断非金属性ZY(填“>”或“<”),请用离子方程式进行说明:。
铍镁都是IIA族元素,分别位于第2、3周期,下列有关说法正确的是( )
A . 原子半径铍比镁的大
B . 铍的最高化合价为+3价
C . 单质与水的反应镁比铍的剧烈
D . 最高价氧化物对应的水化物的碱性铍比镁的强
如图转化过程中错误的是( )
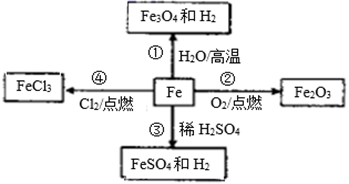
A . ①
B . ②
C . ③
D . ④
将等物质的量的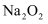 和
和 固体混合,在密闭容器中隔绝空气加热到质量不再变化时排出气体,所得残留物是( )
固体混合,在密闭容器中隔绝空气加热到质量不再变化时排出气体,所得残留物是( )
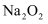 和
和 固体混合,在密闭容器中隔绝空气加热到质量不再变化时排出气体,所得残留物是( )
固体混合,在密闭容器中隔绝空气加热到质量不再变化时排出气体,所得残留物是( )
A . 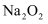 、NaOH
B .
、NaOH
B .  C .
C . 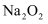 、
、 D . NaOH、
D . NaOH、
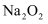 、NaOH
B .
、NaOH
B .  C .
C . 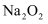 、
、 D . NaOH、
D . NaOH、
最近更新
- 答案:D
- 玲玲和爸爸准备暑假去新疆旅游.下面是妈妈的嘱咐,你认为妈妈说的不对的是( )A.“骑骆驼时,一定要注意安全.”
- 一定质量的理想气体,状态变化过程如P-T图上abcd图线所示,其中bc⊥ab,cd∥ab,由图线可知 A、ab过程,气体
- 计算:=
- 下图是三种微粒的结构示意图,有关它们的说法正确的是A.它们都是原子 B.它们的原子的核外电子
- 某生用小球做分离定律模拟实验:每次分别从Ⅰ、Ⅱ小桶中随机抓取一个小球并记录字母组合;再将抓取的小球分别放回原来小桶后重复
- 下列化学用语书写正确的是( ) A.两个氧分子:2O B.三个二氧化硫分子:3SO2 C.水中氧元素的化合价
- 已知等差数列的前n项和为Sn,且S10=12,S20=17,则S30为( ) A.15
- The regulations were made_____ children after the accidents
- 下列离子方程式正确的是 ( ) A.铝溶于烧碱溶液:Al+2OH-=AlO2-+H2↑B.用铜电极电解硫酸铜溶液
- 曲线在点处的切线方程为 .
- ______ man may usually be known by the books he reads as wel
- 参加过辛亥革命的吴玉章曾说过:“从前皇帝自称为天子,如果有人说皇帝是强盗,可以打倒,别人一定把他看作疯子。孙中山就曾经是
- 下列各表述与示意图一致的是A.图①表示25℃时,用0.1 mol·L-1盐酸滴定20 mL 0.1 mol·L-1 Na
- 下列标志图中,既是轴对称图形,又是中心对称图形的是 ( )
- 若单摆的摆长不变,摆球的质量增加为原来的4 倍,摆球经过平衡位置时的动能减为原来的1/2,则单摆振动的 (
- 22.在下面一段文字横线处补写恰当的语句,使整段文字语意完整连贯,内容贴切,逻辑严密。每处不超过16个字。 睡眠是生命的
- 下表为四个国家在同一年度中的粮食作物生产的统计表。读表回答9~10题。 粮食作物生产统计 甲 乙 丙 丁 每公顷肥料施用
- 某思想家说:“我之出而仕也,为天下,……为万民,非为一姓也。”他所反对的是 ( ) A.民主共和制 B.中央集
- 人口的可持续发展应该( ) A.文化教育的发展相适应 B.住房、交通建设情况相适应 C.城市人口比例、人口年龄



