4.3 质量守恒定律 知识点题库
目前制备高纯硅最广泛采用的方法为三氯硅烷还原法,其化学反应原理为:①SiO2+2C ![]() Si+2X ②Si+3HCl
Si+2X ②Si+3HCl ![]() HSiCl+H ③HSiCl+H═Si+3HCl
HSiCl+H ③HSiCl+H═Si+3HCl
-
(1) 反应①中X的化学式为.
-
(2) 三氯硅烷(HSiCl3)中硅元素的化合价为.
物质 | a | b | c | d |
反应前质量/g | 6.4 | 3.2 | 4.0 | 0.5 |
反应后质量/g | 待测 | 2.56 | 7.2 | 0.5 |
①a和b是反应物,d一定是催化剂
②反应后a物质的质量是3.84g
③c物质中元素的种类,一定是a、b两种物质中元素的种类之和
④若a与b的相对分子质量之比是2:1,则反应中a与b的化学计量数之比是1:1.

-
(1) 甲同学取一支蜡烛粘在玻璃片上,将玻璃片和蜡烛一起放在天平上称量.天平平衡,如图所示点燃蜡烛,过一会观察到天平指针(向左偏、向右偏)因此他得出结论:蜡烛燃烧不符合质量守恒定律.
-
(2) 乙同学对甲同学的实验思考后,进行了改进,他将蜡烛放于一 密闭、干燥、透明的玻璃容器中,放于天平上调节平衡,并设法点燃蜡烛,过一会可观察到蜡烛,天平仍然平衡,他得出结论,蜡烛燃烧符合质量守恒定律.
-
(3) 甲同学得出不符合质量守恒定律的原因是.乙同学从实验上证实蜡烛燃烧符合质量守恒定律.并且还从微观角度进行了解释,他的解释是:.由此可得出结论:用实验研究化学反应前后反应物与生成物之间的质量关系,并有气体参与时,必需在容器中进行.
-
(4) 乙同学通过仔细观察.还观察到了一个明显的现象,他根据该现象得出蜡烛的组成中含有氢元素;该同学又进行了进一步的实验,最后还得出蜡烛的组成中还一定含碳元素.他进行的实验是.他得出蜡烛的组成中一定含碳、氢元素结论的化学原理是.
-
(1) 在炼铁工业中,常用石灰石将铁矿石中的杂质二氧化硅转化为炉渣除去,发生反应的化学方程式为:CaCO3+SiO2
 X+CO2↑,其中X的化学式是 。
A . CaSiO4 B . Ca2SiO3 C . CaSi2O3 D . CaSiO3
X+CO2↑,其中X的化学式是 。
A . CaSiO4 B . Ca2SiO3 C . CaSi2O3 D . CaSiO3 -
(2) 恩施被誉为世界硒都,具有丰富的硒资源.硒(Se)是人生命中必需的微量元素,在周期表中与硫同族、化学性质相似.A、B、C、D表示4种物质,它们的微观示意图如图:
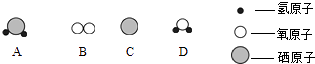
物质A和B在点燃条件下反应生成C和D两种物质,反应的化学方程式是,其基本反应类型是.有机化学中的最简式﹣用元素符号表示化合物分子中各元素的原子个数最简比的式子.某有机物中C、H、O元素的质量比为6:1:8,则该有机物的最简式为(按C、H、O顺序).
物质质量 /g 反应时间/min | 活性炭 | NO | 甲 | 乙 |
0 | 28.72 | 5.00 | 0 | 0 |
4 | 28.00 | 1.40 | x | 2.64 |
下列说法正确的是()
A.生成甲、乙的分子数之比为1:1
B.反应消耗的C与NO的质量之比为2:5
C. x的值为26.76
D.
 CO
B . 2CuO + C
CO
B . 2CuO + C  2Cu + CO2↑
C . CaCO3
2Cu + CO2↑
C . CaCO3  CaO + CO2
D . Na2CO3 + 2HCl= 2NaCl + H2CO3
CaO + CO2
D . Na2CO3 + 2HCl= 2NaCl + H2CO3
 中,根据质量守恒定律判断X的化学式为()
中,根据质量守恒定律判断X的化学式为()
(提出问题)化学反应前后各物质的质量总和是否相等。
(猜想假设)猜想1:不相等;猜想2:。
(实验探究)甲、乙两组同学用托盘天平分别称量反应前后物质的质量。
|
甲组 |
乙组 |
|
|
实验装置(如图) |
| |
| 实验现象 | ①有气泡产生,天平指针 (填“向左”、“向右”或不”,下同)偏转 | ②铁钉表面有红色物质析出,溶液颜色发生改变天平指针偏转。 |
| 实验结论 | 猜想1正确 | ③猜想2正确,发生反应的化学方程式为。 |
(反思评价)通过讨论同学们认为甲组实验方案不合理。
(得到启示)在探究化学反应前后各物质的质量总和是否相等时,凡有气体生成或参加的反应一定要在容器中进行。
(优化装置)同学们对甲组左盘中的反应装置进行了改进(如图),待完全反应后,将装置置于天平上称量,所得质量较反应前的小。若整个操作过程无差错,则造成上述实验误差的原因可能是(填字母)。

A.该反应前后原子的种类、数目、质量变少
B.该反应生成物的总质量小于反应物的总质量
C.气球膨胀产生的浮力干扰了实验结果
(得出结论)改进装置后同学们再次进行探究,均得出猜想2正确。
(拓展应用)硝酸铵(NH4NO3)固体在不同温度下发生不同的分解反应,则下列各物质中不可能是该反应产物的是(填序号)。
A.NH3 B.H2O C.SO2 D.N2

-
(1) 明矾可用于净水,是因为明矾溶于水生成的胶状物可以悬浮于水中的杂质,使之从水中沉降出来,日常生活中常用的方法降低水的硬度。
-
(2) 某学校食堂的早餐提供:鸡蛋、小米粥、鲜肉包、馒头及面条,请你从均衡营养的角度建议食堂增加含的食物(填字母)。
A 蛋白质 B 油脂 C 糖类 D 维生素
-
(3) 硝酸铵又称“硝铵”,是一种常用氮肥。向硝酸铵溶液中加入紫色石蕊溶液,溶液变红色,说明硝酸铵溶液显(填“酸性”、“碱性”或“中性”)。
-
(4) 甲醛(CH3OH)有毒,误饮可使眼镜失明,甚至死亡,最新研究证明,用氨气(NH3)处理含有甲醛的工业废水,可使其转变成无毒的物质,有关反应的化学方程式为
 ,则X的化学式为。
,则X的化学式为。
-
(1) 二氧化锰在反应中起催化作用,反应后它的质量为g;
-
(2) 计算过氧化氢溶液中H2O2的质量。

-
(1) 图中仪器a的名称是,b的名称是。
-
(2) 写出乙炔的物理性质之一:。
-
(3) 从图中选择实验室制备乙炔所用仪器的最佳组合是(填序号)。
-
(4) 碳化钙(CaC2)与水反应的化学方程式为CaC2+2H2O=X+C2H2↑,X是一种碱,则X的化学式为。
 B . 探究硝酸钾溶解度与温度的关系
B . 探究硝酸钾溶解度与温度的关系  C . 探究水的组成元素
C . 探究水的组成元素  D . 验证质量守恒定律
D . 验证质量守恒定律 
| 物质 | 苯 | 氧气 | 二氧化碳 | 水 | X |
| 反应前质量/g | 3.9 | 9.6 | 0 | 0 | 0 |
| 反应中质量/g | 2.6 | 6.4 | 2.2 | 0.9 | m |
| 反应后质量/g | a | b | c | 2.7 | n |
下列判断正确的是( )
|
碳酸氢钠片的质量/g |
足量稀盐酸的质量/g |
反应前总质量/g |
反应后总质量/g |
m(CO2)/g |
|
3.0g |
193.8g |
192.7g |
求该碳酸氢钠片样品中碳酸氢钠的含量。

-
(1) 生成CO2的质量是g。
-
(2) 通过计算判断该品牌纯碱中碳酸钠的含量是否与包装说明相符?(结果精确到0.1%)。
- 仿照下面画线的句子,自选喻体,另写两个句子。要求所写句子的句式和画线句相同,并能够形成排比。 我是一只蜜蜂, 在祖国的大
- 豌豆花的颜色受两对等位基因E/e与F/f所控制,只有当E、F同时存在时才开紫花,否则开白花。下列选项中都符合以上条件的亲
- 阅读下面一首宋诗,然后回答问题。碧湘门①陶 弼 城中烟树绿波漫,几万楼台树影间。 天阔鸟行②疑没草,地卑江势
- 函数的图像是由函数的图像向左平移个单位而得到的,则函数的图像与直线轴围成的封闭图形的面积为A.
- E When the six very best students from different cities in G
- Gibbons failed to see the ______ (商业的) value of his discover
- 高致病性禽流感病毒H5N1侵入人体后可发生如图所示的免疫反应(A、B为有关的物质),下列各种分析正确的是( )A.效应
- Scientists have many theories about how the universe
- 据了解,野生扬子鳄种群的雌雄比例一般稳定在5︰1左右,这样的性别比是由孵化时的温度所决定的;繁殖季节雄性扬子鳄发出“轰
- 电暖器接入电路时与其他家用电器的连接方式是 ▲ (选填“串联”或“并联”).某家庭电路中电能表的示数为,若一个“22
- Recently, one of my best friends, whom I've shared just abou
- 一横波在某一时刻的图象如图所示,其波速为5m/s,其上有一质点A,下列说法正确的是 A.此波的频率为5Hz
- 如图,AB是⊙O的直径,AC是弦,D是AC的中点,若OD=4,则BC=_______.
- 工业上可以利用氟硅酸、碳酸氢铵制备冰晶石(Na3AlF6),其工艺如下: 请回答下列问题: (1)反应
- 下列实验操作正确的是
- 10.Here _____ a new pair of shoes for you. A. is
- —Sorry, I made a mistake again. — Practice more a
- 人的胰岛素和胰蛋白酶的主要成分都是蛋白质,但合成这两种蛋白质的细胞的功能却完全不同,其根本原因是( ) A.不同细
- 如图所示的电路,L是小灯泡,C是极板水平放置的平行板电容器。有一带电油滴悬浮在两极板间静止不动。若滑动变阻器的滑片向下滑
- 下列离子方程式正确的是 A.把少量SO2通入Ca(ClO)2溶液中:SO2 + H2O + Ca2++ 2ClO- =





