3.3 溶液的酸碱性 知识点题库
下列有关物质性质与应用的叙述不正确的是( )
A . 醋酸显酸性,可洗涤水垢
B . 甲醛能改变蛋白质的结构,可保鲜食品
C . 钛合金与人体具有很好的“相溶性”,可制造人造骨
D . 某些植物花瓣浸出液在pH不同的溶液中显示不同颜色,可作酸碱指示剂
下列各组离子能在pH=12的水溶液中大量共存的是( )
A . Fe3+、Ca2+、CO32﹣
B . Na+、SO42﹣、Cl﹣
C . Ba2+、H+、Cl﹣
D . Ag+、NH4+、NO3﹣
某初中化学实验报告中有如下记录,其中实验数据不合理的是( )
A . 用10mL量筒准确量取5.2mL稀硫酸
B . 用托盘天平称取11.7gCuO粉末
C . 用pH试纸测得溶液的pH为3.5
D . 温度计上显示室温读数为25.6℃
下列实验记录合理的是( )
A . 用托盘天平称取10.15gNaCl
B . 用100mL烧杯量取75mL蒸馏水
C . 用pH试纸测出某碱溶液的pH为12
D . 用pH试纸测得某酸溶液的pH为8.1
下列实验操作中正确的是( )
A . 滴瓶上的滴管用完后要用水清洗后放回滴瓶中
B . 药品用量没有说明,液体取1~2mL,固体1~2g
C . 实验室用高锰酸钾加热制取氧气时,试管口略向下倾斜
D . 测溶液的pH,先用水湿润pH试纸再测
某pH=13的溶液中可能含有Cu2+、Na+、SO42﹣、CO32﹣、NO3﹣等离子中的一种或几种,为了检验该溶液中含有的离子,进行如下实验并分析:
-
(1) 该溶液pH=13,证明不存在的离子是.
-
(2) 取少量该溶液于试管中,滴加适最BaCl2溶液,产生白色沉淀,再加入过量的稀盐酸,沉淀部分溶解.写出沉淀溶解的化学方程式:.
-
(3) 该溶液中一定存在的离子是,可能存在的离子是.
铅蓄电池在生产、生活中使用广泛.其构造示意图如图,回答下列问题:

①铅蓄电池充电时是将电能转化为能
②铅蓄电池放电过程中,反应的化学方程式为 Pb+PbO2+2H2SO4═2PbSO4+2H2O,据此可知,铅蓄电池在放电时,溶液的pH不断(填“增大”、“减小”或“不变”)
③从材料分类角度看,塑料是一类材料. (填“合成”或“复合”)
④废硫酸直接排放会污染环境,可以用熟石灰中和硫酸,写出该反应的化学方程式.
室温下,在pH=1的溶液中可能大量共存的是( )
A . K+、Cl﹣、SO42﹣、OH﹣
B . Na+、SO42﹣、NO3﹣、CO32﹣
C . NH4+、Cl﹣、NO3﹣、SO42﹣
D . Ba2+、NO3﹣、Cl﹣、SO42﹣
某同学对CaH2的制备和性质进行探究。
【阅读资料】①用H2与钙加热制得CaH2
②钙遇水立即发生剧烈反应生成一种碱和一种气体
③CaH2要密封保存,遇水反应也生成一种碱和一种气体
【CaH2的制备】设计的制取装置如图所示.

【阅读资料】①用H2与钙加热制得CaH2
②钙遇水立即发生剧烈反应生成一种碱和一种气体
③CaH2要密封保存,遇水反应也生成一种碱和一种气体
【CaH2的制备】设计的制取装置如图所示.

-
(1) 装置B的作用是;
-
(2) 制备CaH2实验结束后,取少量产物,小心加入水中,观察有气泡产生,在溶液中滴入石蕊试液后显色。该同学据此判断:实验中确有氢化钙生成,其他同学提出结论不一定符合题意,原因是。
-
(3) 【CaH2的性质探究】
取少量上述制得的CaH2 样品加入到足量的碳酸钠溶液中,产生大量气泡,过滤,得到滤渣和滤液。经检验滤渣的成分是碳酸钙。该同学进行了如下的探究。
点燃产生的气体,火焰淡蓝色;将燃烧产物通入澄清石灰水中,无现象。则该气体为 (写化学式)。
-
(4) 对滤液中溶质的成分做出如下猜测并进行实验:
猜想一:NaOH 猜想二:NaOH、Ca(OH)2
猜想三:NaOH、Na2CO3 猜想四:NaOH、Na2CO3、Ca(OH)2
经过讨论,大家一致认为猜想四不合理,请用化学方程式说明原因
-
(5) 【实验验证】
实验
现象
结论
实验一:取滤液,向其中滴入少量 Na2CO3溶液
猜想二不成立
实验二:另取滤液,向其中加入足量稀盐酸
猜想三成立
-
(6) 【定量分析】
取制得的CaH2样品1g(杂质为未反应完的Ca)加入到足量的Na2CO3溶液中,充分反应后,过滤、洗涤、干燥称得CaCO3质量为2.4g,则该样品中CaH2的质量分数为
-
(1) 随着人类对能源的需求量日益增长,化石燃料等不可再生能源面临枯竭的危险,在汽油中加入适量乙醇(C2H5OH)作为汽车燃料可适当节省石油资源。乙醇属于(填“有机化合物”或“无机化合物”),写出乙醇燃烧的化学方程式。请再写出一例可节省石油资源的方法。
-
(2) “酸”一词从有酸味的酒而来。常温下酸溶液的pH7(填“>”、“<”或“=”),硫酸是用途广泛的酸,实验室稀释浓硫酸的正确方法是。
如图所示的四个图象分别对应四种过程,其中正确的是()
A . 将NaOH溶液逐滴滴加到盛有稀 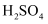 的烧杯中
的烧杯中  B . 分别向等质量且足量的Mg和Zn中加入等质量,等浓度的稀硫酸
B . 分别向等质量且足量的Mg和Zn中加入等质量,等浓度的稀硫酸  C . 室温时,向一定量的饱和石灰水中加入少量氧化钙
C . 室温时,向一定量的饱和石灰水中加入少量氧化钙  D . 向
D . 向  溶液中逐滴加入稀硫酸
溶液中逐滴加入稀硫酸 
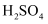 的烧杯中
的烧杯中  B . 分别向等质量且足量的Mg和Zn中加入等质量,等浓度的稀硫酸
B . 分别向等质量且足量的Mg和Zn中加入等质量,等浓度的稀硫酸  C . 室温时,向一定量的饱和石灰水中加入少量氧化钙
C . 室温时,向一定量的饱和石灰水中加入少量氧化钙  D . 向
D . 向  溶液中逐滴加入稀硫酸
溶液中逐滴加入稀硫酸 
下列实验操作中,正确的是()
A . 取用液体  B . 加热液体
B . 加热液体  C . 检查气密性
C . 检查气密性  D . 测定溶液pH值
D . 测定溶液pH值 
 B . 加热液体
B . 加热液体  C . 检查气密性
C . 检查气密性  D . 测定溶液pH值
D . 测定溶液pH值 
一些食物的近似pH如下:牛奶6.3~6.6;鸡蛋清7.6~8.0;柠檬2.2~2.4;番茄4.0-4.4。其中碱性最强的是( )
A . 牛奶
B . 柠檬
C . 鸡蛋清
D . 番茄
盐酸是一种重要的化工原料,也是实验室中重要的化学试剂,初中化学中许多实验都用到了盐酸。
-
(1) 打开浓盐酸的试剂瓶,观察到瓶口有产生。下列实验中一定不会用到盐酸的是(填序号)。
A.除去熟石灰中的石灰石 B.鉴别氯化钠和碳酸钠
C.实验室制取二氧化碳 D.除去铁钉上的锈迹
-
(2) 用盐酸按照下图的方式进行中和反应实验,其化学反应方程式是,向烧杯中逐滴滴入盐酸至过量的过程中,能够说明盐酸与氢氧化钠发生了化学反应的实验现象是。以下证明盐酸过量的操作及实验现象的叙述正确的是(填序号)。

A.滴加石蕊溶液,搅拌后溶液变蓝
B.另滴加氢氧化钠溶液,搅拌后溶液颜色不变
C.加入蒸馏水,搅拌后溶液颜色不变
D.加入金属Cu片,产生气泡
如图所示的图象能反映相对应实验的是( )

A . ①高温煅烧一定质量的石灰石
B . ②用相同质量、相同溶质质量分数的过氧化氢溶液分别制取氧气
C . ③向一定体积的稀盐酸中逐滴加入氢氧化钠溶液
D . ④某温度下,向一定量饱和硝酸钾溶液中加入硝酸钾晶体
下列稀溶液,仅用酚酞及同组物质之间反应就能鉴别出来的一组是 ( )
A . NaOH、H2SO4 、HNO3
B . KOH 、HCl 、Ba(OH)2
C . NaOH、NaCl、Na2CO3
D . NaOH、NaCl、HCl
下列图像能正确反映其对应关系的是( )
A .  电解水生成氢气和氧气的质量与反应时间的关系
B .
电解水生成氢气和氧气的质量与反应时间的关系
B .  加热一定量高锰酸钾固体制氧气,剩余固体中锰元素的质量分数与反应时间的关系
C .
加热一定量高锰酸钾固体制氧气,剩余固体中锰元素的质量分数与反应时间的关系
C .  向氢氧化钠溶液中不断加水,溶液pH与加入水的质量关系
D .
向氢氧化钠溶液中不断加水,溶液pH与加入水的质量关系
D .  相同质量的Mg、Fe分别与足量的稀盐酸反应,产生氢气的质量与反应时间的关系
相同质量的Mg、Fe分别与足量的稀盐酸反应,产生氢气的质量与反应时间的关系
 电解水生成氢气和氧气的质量与反应时间的关系
B .
电解水生成氢气和氧气的质量与反应时间的关系
B .  加热一定量高锰酸钾固体制氧气,剩余固体中锰元素的质量分数与反应时间的关系
C .
加热一定量高锰酸钾固体制氧气,剩余固体中锰元素的质量分数与反应时间的关系
C .  向氢氧化钠溶液中不断加水,溶液pH与加入水的质量关系
D .
向氢氧化钠溶液中不断加水,溶液pH与加入水的质量关系
D .  相同质量的Mg、Fe分别与足量的稀盐酸反应,产生氢气的质量与反应时间的关系
相同质量的Mg、Fe分别与足量的稀盐酸反应,产生氢气的质量与反应时间的关系
规范实验操作是保证安全和实验成败的关键,下列实验操作正确的是( )
A . 稀释浓硫酸  B . 称量氢氧化钠
B . 称量氢氧化钠 C . 吸取药液
C . 吸取药液 D . 测定溶液pH
D . 测定溶液pH
 B . 称量氢氧化钠
B . 称量氢氧化钠 C . 吸取药液
C . 吸取药液 D . 测定溶液pH
D . 测定溶液pH
下表是人体内部分体液的pH,相关说法不正确的是( )
体液 | 尿液 | 胃液 | 血液 | 汗液 |
pH | 4.7~8.4 | 0.9~1.5 | 7.35~7.45 | 5.5~6.6 |
A . 利用pH试纸可测定出上述体液中的pH
B . 胃液的酸性最强,是由胃酸中的盐酸导致的
C . 若血液的pH偏酸性,可能是溶解了二氧化碳
D . 尿液的pH小于4.7,会影响人体健康
下列是一些常见食品的pH,其中,碱性最强的是( )
选项 | A | B | C | D |
食品 | 菠菜 | 香蕉 | 土豆 | 蛋清 |
pH | 14.6 | 8.3 | 5.4 | 3.2 |
A . A
B . B
C . C
D . D
最近更新
- .复数的虚部是 (
- _____ how to express the idea in English, he turned to the d
- NPR has ended its contract with Juan Williams, one of its se
- 已知直角坐标平面上点Q(2,0)和圆C:x2+y2=1,动点M到圆C的切线长与|MQ|的比等于常数λ(λ>0),求
- 化学在生活中无处不在,其中不科学的是( )A.含食品添加剂的食品都不属于绿色食品 B.维生素C具有还原性,在人体内
- 如图,四边形OABC是边长为1的正方形,OC与x轴正半轴的夹角为15°,点B在抛物线的图像上,则的值为
- 老舍的著名话剧《茶馆》中一位秦二爷,他在19世纪末致力于投资近代工业,他的理想是要“顶大顶大的工厂!那才救得了穷人,那才
- 往平底烧瓶中放入氢氧化钡晶体和氯化铵晶体,塞紧瓶塞。在木板上滴少量水,如图所示,一会儿就会发现瓶内固态物质变成液体,瓶壁
- 古诗文默写。(共8分) (1)亲贤臣,远小人, ;亲小人,远贤臣,
- 为了应对互联网的迅速发展,针对第一代互联网数据包传送格式设计时的局限性,世界互联网工程组织设计并正式发布了面向下一代互联
- 下列疾病中属于传染病的一组是 ①流行性感冒;②先天性愚型;③艾滋病;④红绿色盲; ⑤病毒性肝
- A_____girl named Dong Xinyi looked after her disabled fathe
- 填入下文横线处的句子,与上文衔接最恰当的一句是( ) 从古至今,法国人都视花为生活中不可缺少的一部分,____。 A.他
- 某瓷器收藏家的藏品有珐琅彩瓷瓶、五彩镂空云凤纹瓶、青花花卉纹执壶。该收藏家 的生活年代不早于
- It’s raining heavily. Who’s _____ my umbrella?A. brought
- “直到1500'年以前,大西洋一直是一道栅栏,一个终点。到1500年左右,它一变而为一座桥梁,一个起程点了。”导致这一变
- 下列动物中分别属于腔肠动物和棘皮动物的是:A .拂子介和海鳃 B .海鸡冠和海羊齿 C .拂子介和海羊齿 D
- 用绳系一个小球,使它在光滑水平面上做匀速圆周运动,小球受几个力的作用分析正确的是 ( )A.重力,桌面的支持
- 运行以下程序时,循环体内语句执行的次数是( )i=1;while i<10 i=i+1; i=i
- 为了除去粗盐中的Ca2+,Mg2+,SO42﹣及泥沙,得到纯净的NaCl,可将粗盐溶于水,然后在下列操作中选取必要的步骤



