课题3 溶液的浓度 知识点题库
某化学小组初步探究“氢氧化钠溶液与盐酸发生中和反应时溶液温度的变化情况”.

实验用品:37%的浓盐酸(密度为1.18g/mL)、10%的氢氧化钠溶液、蒸馏水、量筒、温度计
-
(1) 实验一:配制100mL 10%的盐酸(密度为1.05g/mL)
实验步骤
(1)计算:需要37%的浓盐酸的体积为 mL(精确到0.01mL,下同);需要蒸馏水的体积为 mL(水的密度为1.0g/mL)
(2)量取浓盐酸和蒸馏水.
(3)混合配制.
-
(2) 实验二:在一定体积的10%的氢氧化钠溶液中滴加10%的盐酸(室温下),反应中溶液温度的变化如下:
加入盐酸的体积(V)/mL
0
2
4
6
8
10
12
14
16
18
20
溶液温度变化(△t)/℃
△t1
5.2
9.6
12.0
16.0
18.2
16.7
15.7
14.7
13.7
12.9
(1)表中△t1的值为 .
(2)试绘出溶液温度变化与加入盐酸体积之间的关系图 .
(3)根据所绘曲线分析,加入盐酸的体积在0~10mL时,溶液温度变化的趋势及其原因是 .
(4)其他条件不变,若改用20%的盐酸进行滴加,结合对上述曲线的分析,大胆猜想新曲线最高点的位置(不考虑溶液密度和比热容的变化及热量散失等影响因素).
横坐标及猜想理由: ;
纵坐标及猜想理由: .
现有一种Na2CO3和NaHCO3的混合物,某同学为测定其含量,取一定量的该样品溶于水,逐滴加入稀盐酸并不断振荡,首先发生反应:Na2CO3 + HCl = NaHCO3 + NaCl,然后才发生反应:NaHCO3+ HCl = NaCl + CO2↑+ H2O。
已知:该温度下CO2密度为1.98g/L,实验测得产生的CO2的与加入稀盐酸的数据如上图。
-
(1) 当加入 g盐酸时,才开始产生CO2;图中V= mL
-
(2) ①所加入盐酸中HCl的质量分数为多少?
②原样品中Na2CO3和NaHCO3的质量各是多少?(百分数精确到0.1%,质量精确到0.01g)
现有FeCl3和CuCl2的混合溶液195.2g,向其中加入铁粉,反应的先后顺序为:2FeCl3+Fe═3FeCl2CuCl2+Fe═FeCl2+Cu.加入铁粉质量与反应就溶液中剩余固体质量的关系如图所示.

-
(1) m(剩余固体)>6.4g时,剩余固体的成分是(填化学式),此剩余固体加入盐酸,发生反应的化学方程式为.
-
(2) 原FeCl3和CuCl2的混合溶液中FeCl3的质量为g.
-
(3) 求当加入11.2g铁粉时,反应后所得溶液中FeCl2的质量分数(写出计算过程)

-
(1) 样品中碳酸钙的质量分数是多少?
-
(2) 所用稀盐酸溶质的质量分数是多少?
-
(3) 加入150g稀盐酸反应后,所得溶液的溶质质量分数是多少?(保留到0.1%)

|
|
|
|
20℃时,向一定量接近饱和的硝酸钾溶液中加入硝酸钾固体 | 加热一定量的高锰酸钾固体 | 向一定量的二氧化锰中加入过氧化氢溶液 | 向两份完全相同的稀盐酸中分别加入锌粉、镁粉至过量 |
 如图向等质量、等质量分数的稀硫酸中分别加入铁和锌
B .
如图向等质量、等质量分数的稀硫酸中分别加入铁和锌
B .  如图向一含有盐酸的氯化铁溶液中边震荡边加入氢氧化钠溶液
C .
如图向一含有盐酸的氯化铁溶液中边震荡边加入氢氧化钠溶液
C .  如图高温煅烧石灰石
D .
如图高温煅烧石灰石
D .  如图等温条件下往接近饱和的硝酸钾溶液中不断加入硝酸钾固体
如图等温条件下往接近饱和的硝酸钾溶液中不断加入硝酸钾固体

-
(1) 共制取氢气 g;
-
(2) 稀硫酸中溶质的质量分数.

-
(1) 实验中发生反应的化学方程式为。
-
(2) 求解混合物中发生反应物质的质量(x)的比例式为。
-
(3) 混合物中氯化钠和碳酸钠质量的最简整数比为。
-
(4) 蒸发后所得溶液的溶质质量分数为。
-
(5) 若用36.5%的浓盐酸配制实验所用的稀盐酸,需加水的质量。
-
(6) 上述稀释操作中,需要用到的实验仪器有量筒、烧杯、。


-
(1) ①中溶质与溶剂的质量比为。
-
(2) 固体甲的溶解度曲线可用右图中的表示。(填a或b)
-
(3) 以上溶液中一定为饱和溶液的是;(填①、②或③)
-
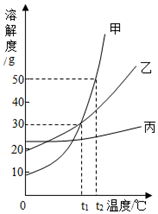
(1) t1℃时,甲、乙两种物质的溶解度为。
-
(2) t2℃时,1吨甲物质的饱和溶液中溶质与溶液的质量比为(填最简整数比)。
-
(3) 现有t1℃时质量相同的甲、乙、丙三种物质的溶液,将这三种溶液分别升温到t2℃,所得溶液中溶质质量分数大小关系是______(填序号)。A . 甲>乙>丙 B . 甲=乙<丙 C . 甲=乙>丙 D . 无法判断
-
(4) 若用已配好的50g溶质质量分数为6%的氯化钠溶液配制溶质质量分数为3%的氯化钠溶液,需要加水的质量为g。
|
实验序号 |
1 |
2 |
3 |
4 |
5 |
|
加入CaCl2溶液质量/g |
15 |
15 |
15 |
15 |
15 |
|
生成沉淀的总质量/g |
3 |
| 9 | 10 | 10 |
求:
-
(1) 表格中
 的数值是。
的数值是。
-
(2) 固体混合物中Na2CO3的质量分数。(写出计算过程,下同,精确到0.1%)
-
(3) 通过计算确定图中a点的坐标。

-
(1) 生活中常用的方法降低水的硬度,并能起到消毒杀菌的作用。
-
(2) 在农业生产中,常用溶质质量分数为3%的KNO3溶液作无土栽培的营养液,配制100kg该营养液需要水的质量是kg。
-
(3) 水是常见的溶剂,如图是a、b、c三种固体物质在水中的溶解度曲线,回答下列问题:

①t1℃时,a的溶解度c的溶解度(填“<”“>”“=”)。
②t2℃时,将30g a物质放入50g水中充分溶解,所得溶液中溶质与溶剂质量比是。
③保持t2℃不变,要使接近饱和的b溶液变为饱和溶液,你采取的方法是。

| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 90 | 100 |
| 溶解度/g | 13.3 | 31.6 | 63.9 | 110 | 169 | X | 246 |
-
(1) 溶解度表中X值的范围为 。
-
(2) a点对应的溶液质量为。
-
(3) b点对应的溶液的溶质质量分数为(列式即可)。
-
(4) 使d点对应的溶液变成饱和溶液,至少需要加入硝酸钾的质量为。
-
(5) 溶液温度从60℃升温至80℃时,溶液中溶质的质量分数(填“变大”“不变”或“变小”)。
- 拟除虫菊酯是一类高效、低毒,对昆虫具有强烈触杀作用的杀虫剂,其中对光稳定的溴氰酯的结构简式如下:下列对该化合物叙述正确的
- 如图2所示,有关电与磁实验的装置图,其中用来研究磁场对电流作用的是:
- 某国2009年生产甲商品50亿件,价格总额450亿元。如果2010年生产甲商品的社会劳动生产率提高50%,其他条件不变,
- 在“验证动量守恒定律”时:(1)需要的实验器材有:斜槽轨道、大小相等质量不等的小钢球两个、重垂线一条、白纸、刻度尺,还需
- 就业是民生之本,为了稳定就业,企业可采用的措施是 A.应建立健全与社会主义市场经济相适应的社会保障制度 B.完善失业保险
- 将下列各组物质放入烧杯中,加入适量水搅拌,待充分反应后过滤,在滤纸上留下两种金属的是() A.Zn、NaCl、CuCl2
- 新华社迎接十七大特稿《在历史关节点上——中国八十六年回眸》一文中用“日出东方、星火燎原、力挽狂澜、灯塔指引、进京赶考”这
- 图是小明设计的测量一个小灯泡额定功率的电路图。已知定值电阻R0=15Ω,滑动变阻器R(20Ω 1A),电源电压为18
- 阅读下面语段,按要求回答问题: 以气节来评价人是残酷的,在局外站着说话的人,用完美道德的_____来要求别人当贞洁烈妇
- (2012·衡阳模拟)如图所示为杂技“顶竿”表演,一人站在地上,肩上扛一质量为M的竖直竹竿,当竿上一质量为m的人以加速
- 下列各句中与例句句式特点相同的一项是( ) 例:然而不王者,未之有也。 A.养生丧死无憾,王道之始也。 B.不拘
- 如图所示的工件的主视图是( )A. B.C. D.
- When a giraffe has ______ drink, it has to stand with its fr
- 在平面直角坐标中,已知点A(2,3)、B(4,7),直线与线段AB有交点,则k的取值范围为 .
- Black Eyed Peas: The E.N.D THE Black Eyed Peas’ fifth albu
- 2011年11月3日凌晨,我国自主设计的“神舟八号”飞船与“天宫一号”成功实现安全对接,携手遨游太空。如图所示,对接后,
- 下列符合既能表示一种元素,还能表示一个原子,又能表示一种物质的是() A.O B.N C.C D.H
- 一个矩形线圈在匀强磁场中转动产生的电动势e=200sin100πt(V),那么()A.该交变电流的频率是100 HzB.
- 读漫画《子孙与资源》,对漫画认识正确的有①人口过多会影响社会的持续发展 ②人口众多给资源带来了巨大压力 ③我国人口与就业
- “又出新车啦!”“又有车降价啦!”这是人们在媒体上见得最多的一类消息。最近有超过10款的轿车宣布降价,另外有北京现代索纳







