第3节 化学方程式 知识点题库
化学方程式:用 来表示化学反应的式子。化学方程式书写原则:A、以为依据;B、符合定律。书写步骤:(1)写出反应物和生成物的正确。(2)化学方程式。(3)注明反应 及生成物的 。
化学方程式的意义:(1)表示反应在什么下进行。(2)表示什么物质,结果生成了什么物质。(3).表示各物质间微粒(原子与分子)的 。(4).表示反应物、生成物各物质间的 。
用化学方程式表示以石灰石.纯碱.水为原料来制取烧碱的过程:
.
《奔跑吧 兄弟》是一档热播的娱乐节目,其中蕴含着许多化学知识。
-
(1) 节目最刺激的游戏是“撕名牌”。“名牌”是贴在队员衣服后面,标有自己姓名的标牌,制作材料有棉布、塑料等。塑料属于(填“有机化合物”或“无机化合物”);鉴别棉布和涤纶布的方法是;
-
(2) 其中一期节目,队员用水枪将酚酞溶液喷射到对方的“名牌”上,立即变红色。事先浸泡“名牌”的溶液可能是___________;A . 白酒 B . 柠檬酸 C . 食盐溶液 D . 纯碱溶液
-
(3)
另一期节目,蓝色的“污水”中注入“神秘水”后立即变得澄清透明。“污水”是单宁酸和硫酸亚铁溶液混合后发生一系列化学反应形成的,加入无色的“神秘水”草酸后,污水变澄清。其中的一个反应为2C76H49O46Fe+H2C2O4
 2C76H50O46Fe+2X,则X的化学式为;草酸(H2C2O4)中碳元素的化合价为。
2C76H50O46Fe+2X,则X的化学式为;草酸(H2C2O4)中碳元素的化合价为。
某同学查阅资料得知:①Cu与稀硫酸不反应,但Cu可与浓硫酸在加热的条件下反应,化学方程式为:Cu+2H2SO4(浓) 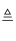 CuSO4+SO2↑+2R;②有元素化合价升降的反应是氧化还原反应.下列说法中不正确的是( )
CuSO4+SO2↑+2R;②有元素化合价升降的反应是氧化还原反应.下列说法中不正确的是( )
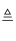 CuSO4+SO2↑+2R;②有元素化合价升降的反应是氧化还原反应.下列说法中不正确的是( )
CuSO4+SO2↑+2R;②有元素化合价升降的反应是氧化还原反应.下列说法中不正确的是( )
A . 该反应属于氧化还原反应
B . R为相对分子质量最小的氧化物
C . 硫酸铜是由铜离子和硫酸根离子构成的化合物
D . 反应中,SO2和R的质量比是32:9
实验室制取氧气时,在试管中加热一定量高锰酸钾固体,随着反应的发生,如图所示的纵坐标表示的是( )

A . 固体物质的质量
B . 高锰酸钾的质量
C . 氧气的质量
D . 固体中锰元素的质量分数
某化学兴趣小组为测定某有机物(含C、H、O三种元素)中各元素的质量比,用下图实验装置(部分夹持装置略去)进行探究。

提示:装置C中发生的反应为2Na2O2+2CO2=2Na2CO3+O2
实验数据:(下表)
读数 | 反应前质量/g | 反应后质量/g |
电子天平a | 217.0 | 222.4 |
电子天平b | 150.0 | 158.4 |
请计算该有机物中各元素的质量比(写出计算过程)。
氨水(NH3·H2O)也是常见的碱,是由NH3溶于水形成的溶液。氨水很不稳定,容易放出有刺激性气味的NH3。根据所学知识回答:
-
(1) NH3·H2O在水溶液中解离出来的离子有。
-
(2) 打开装有氨水的试剂瓶后闻到刺激性气味,说明分子。
-
(3) 写出NH3·H2O与稀H2SO4反应的化学方程式。
-
(4) 将一片有酚酞的干燥纸条和一片有酚酞的湿润纸条分别放入两瓶干燥的NH3中,现象是:。
-
(5) NH3在一定的条件下能跟O2反应,反应过程可用下列示意图表示(注:
 表示氮原子,
表示氮原子,  表示氧原子,
表示氧原子,  表示氢原子;各物质未配平)。请分析在该反应中参加反应的NH3与O2的分子个数之比为。
表示氢原子;各物质未配平)。请分析在该反应中参加反应的NH3与O2的分子个数之比为。
某海洋化工厂集团氨碱法生产的纯碱产品中含有少量氯化钠杂质,为测定该产品中碳酸钠的质量分数,他们进行了以下实验;取12.0g该纯碱样品于烧杯中,称得烧杯及所盛纯碱样品的总质量为158.0g,再把100g稀盐酸平均分成四份依次加入样品中,每次均充分反应,实验数据如表:
|
所加盐酸的次数 |
第一次 |
第二次 |
第三次 |
第四次 |
|
所加盐酸的质量/g |
25 |
25 |
25 |
25 |
|
烧杯及所盛物质的总质量/g |
181.2 |
204.4 |
228.6 |
253.6 |
请你据此分析计算:
-
(1) 第一次加入稀盐酸充分反应后,生成二氧化碳的质量是克。
-
(2) 第四次稀盐酸加入后,烧杯中所得溶液的溶质质量分数是多少?(请写出计算过程,结果精确到0.1%)
18世纪末,法国科学家拉瓦锡曾经做了这样—个实验:让水蒸气通过一根烧红的枪管,生成了一种气体。某校科学兴趣小组的同学对这个实验很感兴趣:难道红热的铁能与水蒸气反应?带着疑问,他们设计了如图所示的装置进行探究。

-
(1) 已知试管内湿棉花不参加化学反应,它的作用是;
-
(2) 若干燥从a导管出来的气体,应从右边装置中(选填“b”或“c”)端管口通入;
-
(3) 其实红热的铁遇到水蒸气,反应后生成氢气和黑色固体四氧化三铁,它属于反应(填基本反应类型),其化学方程式。
普通黄铜仅由铜和锌组成,广泛用于制造板材、管材等,也用于铸造机械零件。现有一块50.00g黄铜样品,某同学利用一种未知浓度的稀盐酸来测定样品中Cu的质量分数。有关数据如下图:

求:
-
(1) 黄铜中Cu的质量分数。
-
(2) 样品完全反应产生的H2的质量。
-
(3) 稀盐酸的溶质质量分数。
m克20%的氢氧化钠溶液与n克20%的盐酸恰好完全反应,如果将m克20%的氢氧化钠溶液改为m克20% 的氢氧化钾溶液,充分反应后所得溶液的pH( )
A . pH<7
B . pH=7
C . pH>7
D . 无法判断
向100克的Na2CO3、Na2SO4混合溶液中先后滴加BaCl2、HCl溶液,反应过程中加入溶液的质量与产生沉淀或气体的质量关系如图所示。下列说法错误的是( )

A . 0-a段发生的反应属于复分解反应
B . m的值为2.33克
C . 该混合溶液中Na2CO3的质量分数是2.12%
D . 取c点对应的溶液,滴加硝酸银溶液,有白色沉淀,说明加入的盐酸已过量
如图所示,AOB
为一杠杆(质量忽略不计),A端悬挂一铜块,并浸没在饱和的硝酸银溶液中,B端用一弹簧测力计竖直向下拉,使杠杆始终处于水平位置平衡。(金属块体积变化忽略不计)

-
(1) 写出烧杯中发生变化的化学方程式;
-
(2) 该过程中整个装置的实验现象是;
-
(3) 铜离子、银离子进入人体会造成重金属中毒,各地医院为及时救治中毒病人,常采用静脉注射EDTA钙钠(C10Hl2CaN2Na2O8),以促进这些金属的排出。通过静脉注射的EDTA钙钠通过血液循环进入心脏四个腔室的顺序是。
我国科学家创造性地构建了“单中心铁催化剂”,在甲烷高效转化研究中获得重大突破,其成果在最近的美国《科学》杂志发表。该转化的微观示意图如图所示,有关转化的说法正确的是( )

A . 催化剂只能是加快反应速率
B . 保持氢气化学性质的最小粒子是H
C . 该反应的化学方程式是:2CH4═C2H4+2H2
D . 反应前后分子的种类发生了改变,是分解反应
如图所示,某矿石含六种元素。则该矿石中不可能存在的物质是( )

A . Al2O3
B . CaCO3
C . SiO2
D . Cu2(OH)2CO3
某溶液中可能含有盐酸、硫酸、硝酸钠、氯化铜中的一种或几种,为了探究其组成,取一定质量的该溶液,向其中逐滴加入氢氧化钡溶液,生成沉淀的质量与所加氢氧化钡溶液的质量之间的关系如图所示。请回答下列问题:

-
(1) 该溶液中一定含有的溶质是(填化学式)。
-
(2) 请写出O~a过程中发生反应的化学方程式:。
随机取一定量的镁粉和铜粉的混合物于烧杯中,再向其中分次加入同一稀硫酸。实验过程中有关物质的用量及质量测定并记录如下表,请回答问题:
|
实验次序 |
第一次 |
第二次 |
第三次 |
第四次 |
|
加入稀硫酸的质量(克) |
35 |
35 |
35 |
35 |
|
剩余固体的质量(克) |
8.6 |
7.4 |
6.2 |
5.2 |
-
(1) 随机所取镁粉和铜粉混合物的质量为 克;
-
(2) 第四次实验操作结束后的溶液中溶质的化学式为 ;
-
(3) 所用稀硫酸中溶质的质量分数为多少?
某同学为了测定一瓶过氧化氢溶液中溶质的质量分数,取该溶液20 g,加入二氧化锰0.5 g,完全反应后,称得烧杯内剩余物质的总质量为19.7 g。
请回答下列问题:
-
(1) 二氧化锰在反应中的作用是 。
-
(2) 计算该过氧化氢溶液中溶质的质量分数。(写出计算过程)
-
(3) 现要配制100g溶质的质量分数为3%的过氧化氢消毒液,需10%过氧化氢溶液的质量为g。
听说墨鱼骨能治疗胃酸过多,好学的小科和小妍想探个究竟。查阅资料,墨鱼骨含碳酸钙70%~85%以上,还含有多种氨基酸(有机物在高温条件下易分解)。为了测定墨鱼骨中碳酸钙的含量,他们先将墨鱼骨洗净晒干,并按各自设计实验方法进行研究。

-
(1) 小科称取10克洗净晒干的墨鱼骨,高温灼烧至质量不变,冷却后称得剩余固体质量为5.4克,处理如下:
CO2 质量=10克-5.4克=4.6克
设碳酸钙质量为M
CaCO3

CO2↑+CaO
100
44
M
4.6g

所以M=10.5克
CaCO3% =10.5克÷10克×100%=105%
小科的计算结果与事实不符,产生错误的原因是:。
-
(2) 小研用如图所示的实验装置进行实验,其中浓硫酸的作用是。
-
(3) 小妍将30mL稀盐酸分3次加入到5克样品中,每次加入盐酸后充分反应,待量筒内的水的体积不再变化时,读出水的体积,结果见下表。已知本实验条件下CO2的密度为2.0克/升,求:该墨鱼骨粉样品中CaCO3的质量分数。
第一次
第二次
第三次
加入稀盐酸的体积(毫升)
10
10
10
进入量筒内水的体积(毫升)
330
660
880
某兴趣小组的同学设计了如图甲、乙、丙所示的三个实验(天平略)来验证质量守恒定律。

-
(1) 小组同学讨论后认为,上述甲、乙、丙三个实验装置中,只有实验(填装置序号)能直接用于验证质量守恒定律。
-
(2) 将图丙改进为图丁的目的是。
最近更新
- After_________walk,they all felt tired. A.three hours
- 某有机物蒸气完全燃烧需三倍于其体积的氧气,产生于二倍于其体积的二氧化碳(体积均在相同状况下测定),该有机物可能是() A
- 下列过程通电后才能进行的是() ①电离 ②电解 ③电镀 ④电化学腐蚀 A.①②③
- 如图甲所示,静止在水平地面上的物块M.在t=0时刻起受到拉力F的作用.F﹣t关系如图乙所示.设物块与地面间的最大静摩擦力
- 在圆轨道上运动的国际空间站里,一宇航员A静止(相对空间舱)“站”于舱内朝向地球一侧的“地面”B上,如图所示,下列说法正确
- 实验室用加热氯酸钾的方法制取氧气并用排水法收集,下列仪器在组装时的前后顺序正确的是 A.②①④③ B.①②④
- 读图,回答1~2题。1.生态农业将物质和能量多层次循环利用,图中①②③分别表示() A.畜牧场、沼气池、耕作业 B.耕作
- 第二卷(共35分) 第四部分:写作(共两节,满分35分) 第一节 短文改错(共10小题;每小题1分,满分10分) 此题
- “纳米材料”是粒子直径为几纳米至几十纳米的材料,纳米碳就是其中一种。若将纳米碳均匀地分散到蒸馏水中,所形成的物质
- a=-1是直线ax+(2a-1)y+1=0和直线3x+ay+3=0垂直的( ) A.充分而不必要条件
- 下图中,AC线地跨三个国家,读后回答8-11题。8.A地气候特征是 ( ) A.最冷月均温小于0℃ B
- 阅读下面的人物访谈,完成下面试题。卖猪肉也要卖出北大水平今年7月,北大前任校长许智宏来深圳,点名约见两位在“
- (8分)一物块从斜面长s、倾角为的斜面的顶端由静止开始下滑,物块与斜面的滑动摩擦系数为,求物块滑到斜面底端所需的时间。
- 是某公司生产的一种新型除草剂,比原有除草剂大大提高了除草效率,关于这种物质的叙述中正确的是( )A.该物质的分子式
- I don’t remember the book yesterday. A. where I p
- 根据你的经验,下列家庭小实验能成功的是 A.用加热的方法修补电木等热固性塑料 B.用食盐水除去
- ,朝露待日晞。
- 下列关于生物基本特征的叙述,正确的是
- 在过去20多年间,中美贸易年均增长18%以上,2002年上半年即达到419.7亿美元。美国是中国第二大贸易伙伴,中国则是
- 假设你是李华,校学生会主席。你将为来曲沃中学访问的外宾对学校作一个介绍。内容要点如下: 1. 介绍学校历史文化(顾炎武《



