高考二轮复习知识点:离子浓度大小的比较5
高考二轮复习知识点:离子浓度大小的比较5
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 多选题 | 详细信息 |
|
下列有关物质浓度关系的描述中,正确的是( )
A . 25℃时,NaB溶液的pH=8,c(Na+)﹣c(B﹣)=9.9×10﹣7mol•L﹣1
B . 25℃时,向0.1mol•L﹣1NH4HSO4溶液中滴加NaOH溶液至中性:c(Na+)>c(NH4+)>c(SO42﹣)>c(OH﹣)=c(H+)
C . 0.1mol•L﹣1的NaHCO3溶液中:c(OH﹣)+2c(CO32﹣)=c(H+)+c(H2CO3)
D . 同温下,pH相同时,溶液物质的量浓度:c(CH3COONa)>c(NaHCO3)>c(C6H5ONa)>c(Na2CO3)
|
|
| 2. 多选题 | 详细信息 |
|
25℃时,下列溶液中微粒的物质的量浓度关系正确的是( )
A . 0.1mol•L﹣lNaHC2O4溶液(pH=5.5):c(Na+)>c( HC2O4﹣)>c(H2C2O4)>c(C2O42﹣ )
B . 0.1mol•L﹣1NaHS 溶液:C(OH﹣)+c(S2﹣)=c( H+)+c(H2S)
C . 0.1mol•L﹣1CH3COOH 溶液和 0.1mol•L﹣1CH3COONa 溶液等体积混合:c(Na+)>c(CH3COOH)>c(CH3COO﹣)>c(H+)>c( OH﹣)
D . 0.1mol•L﹣lNH4HSO4 溶液中滴加 0.1mol•L﹣1NaOH 溶液至中性:c(Na+ )>c(SO42﹣ )>c(NH4+ )>c(OH﹣)=c(H+)
|
|
| 3. 多选题 | 详细信息 |
|
25℃时,下列指定溶液中微粒的物质的量浓度关系正确的是( )
A . 0.1mol·L-1Na2S溶液中:c(OH-)= c(H2S) + c(HS-)
B . 0.1mol·L-1 CH3COONH4溶液中:c(NH4+)+ c(NH3·H2O)=c(CH3COO-) +c(CH3COOH)
C . 0.1mol·L-1pH=6的NaHSO3溶液中:c(Na+) >c(HSO
 ) >c(SO ) >c(SO 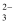 )>c(H2SO3)
D . 0.1mol·L-1Na2CO3溶液与0.1mol·L-1NaHCO3溶液等体积混合所得溶液中:c(CO )>c(H2SO3)
D . 0.1mol·L-1Na2CO3溶液与0.1mol·L-1NaHCO3溶液等体积混合所得溶液中:c(CO 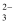 ) >c(HCO3-) >c(OH-) >c(H2CO3) ) >c(HCO3-) >c(OH-) >c(H2CO3)
|
|
| 4. 多选题 | 详细信息 |
|
已知常温下,向20mL0.1mol·L-1的HA溶液中,滴入0.1mol·L-1的NaOH溶液,所得滴定曲线如下图所示,下列说法错误的是( )
A . 若A点的pH=3,则HA为一元弱酸,其电离平衡常数的数量级为10-5
B . B点各微粒物质的量浓度的关系是:2c(H+)+c(A-)=2c(OH-)+c(HA)
C . C点存在关系式:c(A-)=c(Na+)
D . 若D点的pH=8.4,则水电离出的c(H+)=10-8.4mol·L-1
|
|
| 5. 单选题 | 详细信息 |
|
实验测得10 mL 0.50 mol·L-1NH4Cl溶液、10 mL 0.50mol·L-1CH3COONa溶液的pH分别随温度与稀释加水量的变化如图所示。已知25 ℃时CH3COOH和NH3·H2O的电离常数均为1.8×10-5.下列说法错误的是( )
A . 图中实线表示pH随加水量的变化,虚线表示pH随温度的变化'
B . 将NH4Cl溶液加水稀释至浓度
 mol·L-1 , 溶液pH变化值小于lgx
C . 随温度升高,Kw增大,CH3COONa溶液中c(OH- )减小,c(H+)增大,pH减小
D . 25 ℃时稀释相同倍数的NH4Cl溶液与CH3COONa溶液中:c(Na+ )-c(CH3COO- )=c(Cl-)-c(NH mol·L-1 , 溶液pH变化值小于lgx
C . 随温度升高,Kw增大,CH3COONa溶液中c(OH- )减小,c(H+)增大,pH减小
D . 25 ℃时稀释相同倍数的NH4Cl溶液与CH3COONa溶液中:c(Na+ )-c(CH3COO- )=c(Cl-)-c(NH  ) )
|
|
| 6. 单选题 | 详细信息 |
|
HA是一元弱酸,难溶盐MA的饱和溶液中
 而变化, 而变化,  不发生水解。实验发现,298K时 不发生水解。实验发现,298K时  ,如下图中实线所示。 ,如下图中实线所示。 下列叙述错误的是( )
A . 溶液pH = 4 时.
 B . MA 的溶度积
B . MA 的溶度积  C . 溶液 pH = 7 时,
C . 溶液 pH = 7 时,  D . HA 的电离常数
D . HA 的电离常数 
|
|
| 7. 单选题 | 详细信息 |
|
常温下,用
 的盐酸分别滴定20.00mL浓度均为 的盐酸分别滴定20.00mL浓度均为  三种一元弱酸的钠盐 三种一元弱酸的钠盐  溶液,滴定曲线如图所示。下列判断错误的是( ) 溶液,滴定曲线如图所示。下列判断错误的是( )
A . 该
 溶液中: 溶液中:  B . 三种一元弱酸的电离常数:
B . 三种一元弱酸的电离常数:  C . 当
C . 当  时,三种溶液中: 时,三种溶液中:  D . 分别滴加20.00mL盐酸后,再将三种溶液混合:
D . 分别滴加20.00mL盐酸后,再将三种溶液混合: 
|
|
| 8. 单选题 | 详细信息 |
|
鸟嘌呤(
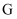 )是一种有机弱碱,可与盐酸反应生成盐酸盐(用 )是一种有机弱碱,可与盐酸反应生成盐酸盐(用  表示)。已知 表示)。已知  水溶液呈酸性,下列叙述正确的是( ) 水溶液呈酸性,下列叙述正确的是( )
A .
 水溶液的 水溶液的  B .
B .  水溶液加水稀释, 水溶液加水稀释,  升高
C . 升高
C .  在水中的电离方程式为: 在水中的电离方程式为:  D .
D .  水溶液中: 水溶液中: 
|
|
| 9. 单选题 | 详细信息 |
|
取两份
  的 的  溶液,一份滴加 溶液,一份滴加  的盐酸,另一份滴加 的盐酸,另一份滴加  溶液,溶液的pH随加入酸(或碱)体积的变化如图。 溶液,溶液的pH随加入酸(或碱)体积的变化如图。 下列说法不正确的是( )
A . 由a点可知:
 溶液中 溶液中  的水解程度大于电离程度
B . 的水解程度大于电离程度
B .  过程中: 过程中:  逐渐减小
C . 逐渐减小
C .  过程中: 过程中:  D . 令c点的
D . 令c点的  ,e点的 ,e点的  ,则 ,则 
|
|
| 10. 多选题 | 详细信息 |
|
室温下,向10mL0.10mol·L-1的HA(Ka=1.0×10-3)中逐滴加入0.10mol·L-1NaOH溶液,溶液pH随加入NaOH溶液体积的变化关系如图所示。若溶液混合引起的体积变化可忽略,下列说法正确的是( )
A . a点时,c(Na+)-c(HA)=c(OH-)-c(H+)
B . 由a→b,溶液中n(A-)持续增大
C . b点时,c(Na+)=c(HA)+c(A-)+c(OH-)
D . V=10mL时,c(HA)+c(A-)+c(Na+)=0.20mol·L-1
|
|
高中化学 试卷推荐
- 河南省豫北名校大联考2021-2022学年高二下学期期中考试化学试题
- 上海市徐汇区2022届高三二模化学试题
- 江苏省启东市2020-2021学年高二上学期化学期中考试试卷
- 安徽省马鞍山市2021年高考化学一模试卷
- 黑龙江省八校2021-2022学年高二上学期期中联合考试化学试题
- 河南省洛阳市豫西名校2021-2022学年高二上学期化学第一次月考试卷
- 安徽省黄山市2020-2021学年高二上学期期末考试化学试题
- 山西省大同、阳泉市2022届高三第二次模拟考试理科综合化学试题
- 浙江省淳安县汾口中学2020-2021学年高一下学期化学开学考试试卷
- 浙江省衢州市2021-2022学年高一上学期期末教学质量检测化学试题
- 湖南省娄底市2020-2021学年高二上学期化学期中考试试卷
- 四川省遂宁市2021年高考化学三模试卷
最近更新
- 南宋初期,古徽州(今皖、浙、赣三省交界)是古代徽商的发源地。当地居民充分利用本地资源优势,与区外发展商品贸易,徽
- A、B之间有6条网线路并联,它们通过的最大信息量分别为1,1,2,2,3,4,现从中任取三条网线,且使三这三条网线通过的
- 下列应用或事实与胶体的性质无关的是( )。A.用明矾净化饮用水 B.用石膏或盐卤点
- 如图所示是一定质量的理想气体由a状态变化到b状态。则a→b过程中 A.气体的温度升高B.气体内每个分子的动能都增大C.气
- ----Hello! My name isAnn.-----_________. A. Yes, you are.
- “我们亚洲,山是高昂的头;我们亚洲,河像热血流……”听到这首《亚洲雄风》歌曲,我们的脑海中会涌现出一幅壮丽山河的画卷。
- 下面句子是对黄河壶口瀑布的描写,适当调整画线部分的语序,把它改写成格式协调一致、匀整对称的排比句。(可以根据题目要求改变
- B.假设 2007 年 1 单位 M 国货币/1 单位 N 国货币为 1: 5.5。 2008 年,M国的通货膨胀率为
- 下列对汉朝选官察举制度的叙述,不正确的是:( ) A.是为适应专制主义中央集权封建国家统治而建立的选官制度 B
- (本小题满分12分) 在棱长为1的正方体中,为上的点,且满足,为上的点,且满足。 (1)求异面直线与AC所成的角的大小;
- 生物体中细胞内的葡萄糖,细胞膜外的富氧液体及细胞膜可构成微型生物原电池,下列有关判断正确的是 ()
- 分解因式: .
- “大力推进生态文明建设,努力建设美丽中国”是今年全国两会的主题之一。以下行为不利于环境保护的是( ) A.
- 有两根木条,一根AB长为80㎝,另一根CD长为130㎝,在它们的中点处各有一个小圆孔M、N(圆孔直径忽略不计,M、N抽象
- 在建筑装修中,工人用质量为m的磨石对斜壁进行打磨,当对磨石加竖直向上推力F时,磨石恰好沿斜壁向上做匀加速直线运动,已知磨
- 能被肾小管全部重吸收回到血液的物质是 A、水 B、无机盐 C、葡萄糖 D、尿素
- 下列事例中中属于动能转化为重力势能的是 A.小刚用弹弓上形变的橡皮条将“子弹”弹射出去 B.小明脚踩滑板从高
- 如图,抛物线y=x2+bx+c与x轴交于A、B两点,B点坐标为(3,0),与y轴交于点C(0,3). (1)求抛物线的解
- 为了减少大气污染,许多城市推广汽车使用清洁燃料。目前使用的清洁燃料主要有两类:一类是压缩天然气(CNG),另一类是液化石
- 老师讲了一个新的龟兔赛跑的故事,按照老师所讲的故事情节,乌龟和兔子的位移随时间的图象如图所示,则根据图象可知()A.发令









