高考二轮复习知识点:电解池工作原理及应用3
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | 详细信息 |
|
利用生物燃料电池原理研究室温下氨的合成,电池工作时MV2+/MV+在电极与酶之间传递电子,示意图如下所示。下列说法错误的是( )
A . 相比现有工业合成氨,该方法条件温和,同时还可提供电能
B . 阴极区,在氢化酶作用下发生反应H2+2MV2+=2H++2MV+
C . 正极区,固氮酶为催化剂,N2发生还原反应生成NH3
D . 电池工作时质子通过交换膜由负极区向正极区移动
|
|
| 2. 实验探究题 | 详细信息 |
|
近年来,随着聚酯工业的快速发展,氯气的需求量和氯化氢的产出量也随之迅速增长。因此,将氯化氢转化为氯气的技术成为科学研究的热点。回答下列问题:
|
|
| 3. 多选题 | 详细信息 |
|
我国科学家设计二氧化碳熔盐捕获及电化学转化装置,其示意图如图:下列说法不正确的是( )
A . b为电源的负极
B . ①②中,捕获CO2时碳元素的化合价发生了变化
C . a极的电极反应式为2C2O52﹣﹣4e﹣═ 4CO2 +O2
D . 上述装置存在反应:CO2
 C+O2 C+O2
|
|
| 4. 多选题 | 详细信息 |
|
利用电解法可将含有
 等杂质的粗铜提纯。下列叙述中正确的是( ) 等杂质的粗铜提纯。下列叙述中正确的是( )
A . 电解时精铜作阳极
B . 粗铜连接电源的负极
C . 电解时阴极上发生的电极反应为
 D . 电解后,电解槽底部会形成含有少量
D . 电解后,电解槽底部会形成含有少量  等金属的阳极泥 等金属的阳极泥
|
|
| 5. 多选题 | 详细信息 |
|
钠碱脱硫液(
 )吸收一定量 )吸收一定量  气体后,可通过以下装置实现再生。下列说法正确的是( ) 气体后,可通过以下装置实现再生。下列说法正确的是( )
A . 电极b应接电源的负极
B . m应为阳离子交换膜
C . 出液2的
 大于进液 大于进液 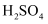 的 的  D . 出液1可使溴水褪色
D . 出液1可使溴水褪色
|
|
| 6. 多选题 | 详细信息 |
|
我国科研工作者提出通过电解原理联合制备环氧乙烷同时处理酸性含铬废水,其工作原理示意图如图所示。其中双极膜由阳离子交换膜和阴离子交换膜组成,工作时内层
 解离为 解离为 和 和 , 并分别向两极迁移。下列说法正确的是( ) , 并分别向两极迁移。下列说法正确的是( )
A . 电极a上的电势低于电极b上的电势
B . 膜q为双极膜中的阳离子交换膜
C . 工作时,NaOH溶液浓度保持不变
D . 每生成
 , 酸性废水质量理论上增加3g , 酸性废水质量理论上增加3g
|
|
| 7. 综合题 | 详细信息 | ||||||||||||||
|
“绿水青山就是金山银山”,研究消除氮氧化物污染对建设美丽家乡,打造宜居环境有重要意义。
|
|||||||||||||||
| 8. 综合题 | 详细信息 |
|
Mn及其化合物在工业生产中具有重要的用途。
|
|
| 9. 综合题 | 详细信息 | |||||||||
|
处理再利用H2S有多种方法。
|
||||||||||
| 10. 综合题 | 详细信息 | ||||||||||||||||||||
|
综合处理炼锌矿渣[主要含铁酸镓Ga2(Fe2O4)3、铁酸锌ZnFe2O4],实现变废为宝得到多种产品,进一步利用镓盐可制备具有优异光电性能的氮化镓GaN(Ga与Al同主族),部分工艺流程如图:
已知:①常温下,浸出液中各离子形成氢氧化物沉淀的pH和金属离子在工艺条件下的萃取率(进入有机层中金属离子的百分数)见表:
②当溶液中剩余离子的浓度小于10-5mol·L-1时,视为沉淀完全。 ③MOCVD:化学气相沉积,以合成的三甲基镓为原料,使其与NH3反应得到GaN。 请回答下列问题:
|
|||||||||||||||||||||
- 湖北省部分省重点中学2020-2021学年高二下学期化学3月月考试卷
- 江西省鹰潭市2022届高三第二次模拟考试理科综合化学试题
- 山东省日照市2021年高考化学三模试卷
- 广东省河源市河源高级中学2020-2021学年高一上学期化学期中考试试卷
- 福建省名校联盟2021-2022学年高二下学期期中考试化学试题.
- 福建省三明市三地三校2020-2021学年高一上学期化学期中考试试卷
- 广西来宾市2020-2021学年高一上学期期末教学质量检测化学试题
- 辽宁省沈阳市郊联体2021-2022学年高三上学期化学10月月考试卷
- 河南省新乡市2022届高三第三次模拟理科综合化学试题
- 安徽省马鞍山市和县2020-2021学年高一上学期化学期中考试试卷
- 湖北省蕲春县2020-2021学年高二下学期化学期中考试试卷
- 广东省广州市番禺区洛溪新城中学2020-2021学年高一下学期化学4月月考试卷
- 无论m为何实数,直线y=x+m与y=-x+4的交点不可能在第______象限.
- (三)文学类文本阅读(14分) 阅读下面的文字,完成7~9题。 朱先生退兵 陈忠实 那天清晨,朱先生正在
- 在已建立直角坐标系的4×4正方形方格纸中, △ABC是格点三角形(三角形的三个顶点都是小正方形的顶点),若以格点P,A,
- 根据对话内容,从方框中选择恰当的选项补全对话。 A: Would you like to have dinner wit
- 阅读下面的文言文,完成下面试题。 齐桓公求管仲 桓公自莒反于齐,使鲍叔为宰,辞曰:“臣,君之庸臣也。君加惠于臣,
- 下列说法正确的是A.H2O的摩尔质量是18g B. 1molCO2比1molCO多1个氧原子C
- 生物既能适应环境,也能影响环境。下列现象中,属于影响环境的是 A、根深叶茂 B、大雁南飞 C、大树底下好乘凉 D、秋风扫
- 已知在三棱锥S—ABC中(如下图),P、Q分别是△SAC和△SAB的重心,则BC与平面APQ的位置关系是________
- 图①为一种平板电脑保护套的支架效果图,AM固定于平板电脑背面, 与可活动的MB、CB部分组成支架.平板电脑的下端N保持在
- 1851年的伦敦博览会是英国展出最新工业成果的盛会,下列哪一工业成果可用于这一届博览会的展出A.第一架反射望远镜
- 关于的一元二次方程,其根的判别式的值为1,求m的值及该方程的根.
- The cookies _________ good.Could I have some more?A.tasteB.s
- 目前,我国汽车产业已经进入持续、稳定、快速的增长期,但市场竞争也越来越激烈。据此回答下题。 随着国内汽车消费日趋理性,消
- 若复数(-6+k2)-(k2-4)i(k∈R)所对应的点在第三象限,则k的取值范围是________.
- 在现行元素周期表中,所含元素种数最多的族和周期分别是( ) A. 第ⅠA族 第六周期 B. 第Ⅷ族 第六周期 C. 第Ⅲ
- 一根导体两端加电压2 V时,通过的电流正好是0.1 A,则导体的电阻是________ Ω。如果这根导体两端加的电压变为
- 乙烯与乙烷混合气体共a mol,与b mol的氧气共存于一密闭容器中,点燃后充分反应,乙烯和乙烷全部消耗完,得到CO到C
- A:What can I do for you? B:Yes, please. 1 .But what kind
- 如图6,一次函数的图象与轴,轴交于A,B两点,与反比例函数的图象相交于C,D两点,分别过C,D两点作轴,轴的垂线,垂足为
- 如图14-7-20所示,用伏安法测电阻Rx,电路电压恒定;当K接a时,电压表示数为10 V,电流表示数为0.2 A;当K


 Cl2(g) ΔH1=83 kJ·mol-1
Cl2(g) ΔH1=83 kJ·mol-1






 反应生成
反应生成 的热化学方程式。
的热化学方程式。 恒容密闭容器中,投入
恒容密闭容器中,投入 和
和 , 经过一段时间后达到平衡状态,测得
, 经过一段时间后达到平衡状态,测得 的转化率为
的转化率为 。该温度下,反应的平衡常数为。
。该温度下,反应的平衡常数为。
 的脱除。热解温度为
的脱除。热解温度为 得到的煤焦分别用
得到的煤焦分别用 表示,相关信息如下表:
表示,相关信息如下表:


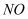 的脱除主要包含吸附和化学还原(
的脱除主要包含吸附和化学还原( )两个过程]
)两个过程]
 后,随着温度升高,单位时间内NO的脱除率增大的原因是。
后,随着温度升高,单位时间内NO的脱除率增大的原因是。

 +4H+=2CO2↑+Mn2++2H2O)
+4H+=2CO2↑+Mn2++2H2O) +16H+=2Mn2++10CO2↑+8H2O)
+16H+=2Mn2++10CO2↑+8H2O) S2(?)+2H2(g)。其他条件不变时,H2S的平衡转化率随温度和压强的变化如图。
S2(?)+2H2(g)。其他条件不变时,H2S的平衡转化率随温度和压强的变化如图。






