高中化学选择性必修1单元分层测试:第三章 水溶液中的离子反应与平衡 B卷
高中化学选择性必修1单元分层测试:第三章 水溶液中的离子反应与平衡 B卷
教材科目:化学
试卷分类:高二上学期
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
教材科目:化学
试卷分类:高二上学期
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | 详细信息 |
|
常温下,向20 mL 0.1mol·L-1的盐酸中逐滴加入0.1 mol·L-1的氨水,溶液pH的变化与加入氨水的体积关系如图所示。下列叙述错误的是( )
A . V>20 mL
B . ①、②、③点水的电离程度大小为:②>③>①
C . 在点②所示溶液中:c(Cl-)=c(NH3·H2O)+c(NH
 )
D . 在点②、③之间可能存在:c(NH )
D . 在点②、③之间可能存在:c(NH  )>c(Cl-)=c(OH-)>c(H+) )>c(Cl-)=c(OH-)>c(H+)
|
|
| 2. 多选题 | 详细信息 | ||||||||
|
部分弱酸的电离平衡常数如表所示:
下列说法错误的是( )
A .
 B .
B .  C . 中和等体积、等pH的
C . 中和等体积、等pH的  和 和  溶液,前者消耗 溶液,前者消耗  的量小于后者
D . 等体积、等浓度的 的量小于后者
D . 等体积、等浓度的  和 和  溶液中,前者所含离子总数小于后者 溶液中,前者所含离子总数小于后者
|
|||||||||
| 3. 多选题 | 详细信息 |
|
已知:常温下,
 。某温度下,饱和溶液中 。某温度下,饱和溶液中  与 与  、 、  的关系如图所示。 的关系如图所示。 下列说法正确的是( )
A . 曲线Ⅱ代表
 的沉淀溶解平衡曲线
B . 常温下, 的沉淀溶解平衡曲线
B . 常温下,  的 的  C . 常温下,当
C . 常温下,当  时,饱和溶液中 时,饱和溶液中  D . 加入
D . 加入 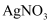 固体可使溶液由 固体可使溶液由 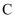 点沿直线变为 点沿直线变为 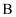 点 点
|
|
| 4. 多选题 | 详细信息 |
|
常温下,用
 盐酸滴定 盐酸滴定  某弱碱 某弱碱  溶液,所得溶液 溶液,所得溶液  、 、  和 和  的物质的量分数与滴加盐酸体积的关系如图所示。下列叙述错误的是( ) 的物质的量分数与滴加盐酸体积的关系如图所示。下列叙述错误的是( )
A . 曲线①代表
 ,曲线②代表 ,曲线②代表  B . b点溶液中存在
B . b点溶液中存在  C .
C .  的电离平衡常数为 的电离平衡常数为  D . a、b、c三点的溶液,水的电离程度
D . a、b、c三点的溶液,水的电离程度 
|
|
| 5. 多选题 | 详细信息 |
|
25℃时,向1L某缓冲溶液(含0.1mol·L-1CH3COOH、0.08mol·L-1CH3COONa)和1L0.1mol·L-1CH3COOH溶液中加入NaOH(s)或通入HCl(g),两种溶液的pH变化如图所示(不考虑溶液体积变化)。已知缓冲溶液pH=pKa-lg
 , 下列说法正确的是( ) , 下列说法正确的是( )
A . 曲线①对应的溶液是缓冲溶液
B . 25℃时醋酸的电离常数的数量级为10-5
C . a点溶液中离子浓度的大小关系为c(CH3COO-)=c(CH3COOH)>c(H+)>c(OH-)
D . b点溶液存在:4c(CH3COOH)+9c(H+)=9c(Cl-)+9c(OH-)+5c(CH3COO-)
|
|
| 6. 多选题 | 详细信息 |
|
向一定体积的
 的草酸溶液中滴加 的草酸溶液中滴加 的NaOH溶液,溶液中 的NaOH溶液,溶液中 、 、 、 、 的物质的量分数(δ)随pH变化的关系如图所示。下列说法错误的是( ) 的物质的量分数(δ)随pH变化的关系如图所示。下列说法错误的是( )
A . 水的电离程度:N>M>P
B .
 的水解平衡常数 的水解平衡常数 C . N点:
C . N点: D . 向
D . 向 的溶液中持续滴加NaOH溶液,水的电离程度持续变大 的溶液中持续滴加NaOH溶液,水的电离程度持续变大
|
|
| 7. 综合题 | 详细信息 |
下列物质中:①
|
|
| 8. 单选题 | 详细信息 |
常温下,向10mL0.10mol/LCuCl2溶液中滴加0.10mol/LNa2S溶液,滴加过程中-lgc(Cu2+)与Na2S溶液体积(V)的关系如图所示。下列说法不正确的是
A . Ksp(CuS)=10-35.4
B . a点溶液中:c(S2-)•c(Cu2+)=Ksp(CuS)
C . c点溶液中:c(Na+)>c(Cl-)>c(S2-)>c(OH-)>c(H+)
D . a、b、c三点溶液中,水的电离程度最大的是b点
|
|
| 9. 单选题 | 详细信息 |
常温时将
|
|
| 10. 单选题 | 详细信息 | ||||||||||||
下列实验或装置能达到实验目的的是
A . A
B . B
C . C
D . D
|
|||||||||||||
高中化学 试卷推荐
- 浙江省湖州市2020-2021学年高一下学期化学期末考试试卷
- 江苏省扬州市邗江区2020-2021学年高二上学期化学期中考试试卷(选修)
- 上海市青浦区2021-2022学年高三上学期期终调研测试化学试题
- 山东省日照市2022届高三第二次模拟考试化学试题
- 广西河池市2020-2021学年高一上学期期末教学质量检测化学试题
- 江苏省启东市2020-2021学年高一上学期化学期中考试试卷
- 北京市丰台区2021届高三上学期期末考试化学试题
- 辽宁省朝阳市建平县2021-2022学年高一上学期期末考试化学试题
- 广东省揭阳市第三中学2020-2021学年高二上学期化学期中考试试卷
- 安徽省合肥市2021年高考化学一模试卷
- 陕西省安康市2020-2021学年高二上学期期末化学试题
- 广西岑溪市2020-2021学年高二上学期化学期中考试试卷(文)
最近更新
- (本小题满分14分)平面直角坐标系中,平行四边形ABOC如图放置,点A、C的坐标分别为(0,3)、(,0),将此平行四边
- (09年湖北八校联考文)(14分)已知数列中,,,其前项和满足,令 (Ⅰ)求数列的通项公式; (Ⅱ)令,求证:
- 回答下列有关问题:①用量筒量取一定体积液体,倾倒于烧杯中,量筒内残留的液滴应怎样处理,否则会使配成的溶液浓度如何变化?②
- 非零向量(a+b),(2a-b)互相垂直;(a-2b)与(2a+b)互相垂直,求a与b的夹角.
- 果蝇是研究遗传学问题的良好材料,请回答: ⑴果蝇的体细胞中有4对染色体,在精子的形成过程中,会出现两次染色体排列在细胞中
- 在我国最早出现的近代企业是 A.洋务派创办的企业 B.民族资本主义企业 C.外商企业 D.官
- —Mom, my classmates are playing outside. Can I join them?
- 在研究电容器的电容与哪些因素有关的实验中,对电容器充电后与电源断开。现使两极板间的距离靠近一些,同时又在两极板间插入电介
- 一定温度下,对可逆反应 A(g)+ B(g)2C(g)的下列叙述中,能说明反应已达到平衡的是( )A.单位时间内消耗a
- 下列说法中不正确的是 ①将BaSO4放入水中不能导电,所以BaSO4是非电解质 ②氨溶于水得到的溶液氨水能导电,所以氨水
- 下列说法正确的是() A.使元素的化合态转化成游离态的过程就是还原的过程 B.高炉炼铁的原料有铁矿石、焦炭和空气。工业上
- 关于从集合A到集合B的映射,下面的说法错误的是( )A.A中的每一个元素在B中都有象B.A中的两个不同元素在B中的
- 下列选项中属于规律的一组是 ①月亮绕地球转 ②新
- 下列汽车标志中既是轴对称图形又是中心对称图形的是()
- 家用碱面的主要成分是Na2CO3。其物质类别属于( ) A.酸 B.盐
- 石蕊、硫酸、氢氧化钙、碳酸钠是常见的四种物质,它们的溶液之间的反应关系如上图所示,图中两圆相交部分(A、B、C、D)表示
- 心理学家研究发现,轻松和愉快会使T细胞提高对病毒、肿瘤的监控,间接引起抗体生成能力的升高。这表明不健康的心态会导致………
- 下列化学式只能表示一种物质的是A.C3H8 B.C4H10 C.C4H8
- 使有意义的的取值范围是 .
- 某昼夜温差大的地区,粮食作物的籽粒饱满,果树和瓜果类果实较甜,这是因为 ( ) A.光合作用旺盛,呼


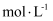 )(25℃)
)(25℃)







 ②
② ③
③ ④盐酸 ⑤
④盐酸 ⑤ ⑥
⑥
 。将上述六种物质分别配成
。将上述六种物质分别配成 的溶液,向稀氨水中分别滴加少量六种溶液,能使氨水的电离平衡逆向移动且
的溶液,向稀氨水中分别滴加少量六种溶液,能使氨水的电离平衡逆向移动且 增大的是(填序号),此时
增大的是(填序号),此时 (填“增大”“减小”或“不变”,下同),
(填“增大”“减小”或“不变”,下同), 。
。
 的
的 ”或“
”或“ 的电离平衡常数为
的电离平衡常数为 , 向
, 向 的
的 溶液中滴加少量硫酸,再加水稀释至
溶液中滴加少量硫酸,再加水稀释至 , 此时测得
, 此时测得 , 则溶液中
, 则溶液中
 。
。
 的电离平衡常数为
的电离平衡常数为 ;碳酸
;碳酸 的电离平衡常数为
的电离平衡常数为 ,
,  , 足量的
, 足量的 溶液和
溶液和
 的某酸
的某酸 与
与 的某碱
的某碱 等体积混合后,溶液的
等体积混合后,溶液的 。下列说法错误的是
。下列说法错误的是
 的水溶液一定显碱性
的水溶液一定显碱性







