高考二轮复习知识点:判断简单分子或离子的构型3
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 多选题 | 详细信息 |
|
下列描述中正确的是( )
A . CS2为空间构型为V形的极性分子
B . 双原子或多原子形成的气体单质中,一定有σ键,可能有π键
C . 氢原子电子云的一个小黑点表示一个电子
D . SiF4和SO32-的中心原子均为sp3杂化
|
|
| 2. 多选题 | 详细信息 |
|
硫代硫酸钠(Na2S2O3)可作定影剂,反应的化学方程式为AgBr+2Na2S2O3=Na3[Ag(S2O3)2]+NaBr,产物中的Na3[Ag(S2O3)2]常用于切花保鲜。下列说法错误的是( )
A . 基态Na+的核外电子存在10种运动状态
B . S2O
 的空间结构为四面体形,中心原子S的杂化方式为sp3
C . 欲测定切花保鲜液中Na3[Ag(S2O3)2]的浓度,可用NaCl标准溶液滴定Ag+
D . NaBr的晶体结构与NaCl晶体相似,每个Br-周围有8个Na+ 的空间结构为四面体形,中心原子S的杂化方式为sp3
C . 欲测定切花保鲜液中Na3[Ag(S2O3)2]的浓度,可用NaCl标准溶液滴定Ag+
D . NaBr的晶体结构与NaCl晶体相似,每个Br-周围有8个Na+
|
|
| 3. 综合题 | 详细信息 |
|
【物质结构与性质】
Cu(Inl-xGaxSe2)(简称CIGS)可作多晶膜太阳能电池材料,具有非常好的发展前景。 回答下列问题:
|
|
| 4. 综合题 | 详细信息 |
|
锂离子电池让电动汽车飞速发展,有利于实现节能减排。LiCoO2、LiFePO4、Li4TisO12常用作电池的电极材料,LiPF6、LiAsF6常用作锂离子聚合物电池的载体材料。
回答下列问题:
|
|
| 5. 综合题 | 详细信息 |
|
电动汽车电池材料的发展技术之一是使用三元材料镍锰钴酸锂。回答下列问题:
|
|
| 6. 综合题 | 详细信息 |
|
CdSnAs2是一种高迁移率的新型热电材料。回答下列问题:
|
|
| 7. 综合题 | 详细信息 |
|
半导体芯片的关键材料是我国优先发展的新材料。经过半个多世纪的发展,硅基材料的半导体器件性能已经接近其物理极限,以碳化硅、氮化镓等为代表的第二代半导体材料成为当今热点。回答如下问题:
|
|
| 8. 综合题 | 详细信息 |
|
硫及其化合物有许多用途,请回答下列问题。
|
|
| 9. 综合题 | 详细信息 |
|
氮化硼(BN)是一种重要的功能陶瓷材料.以天然硼砂(主要成分Na2B4O7)为起始物,经过一系列反应可以得到BN和火箭高能燃料及有机合成催化剂BF3的过程如下:
|
|
| 10. 综合题 | 详细信息 |
|
N、P、S、
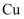 、 、  元素形成的化合物质性质丰富,研究较多。 元素形成的化合物质性质丰富,研究较多。
|
|
- 浙江省温州人文高级中学2019-2020学年高一下学期化学期中考试试卷
- 安徽省亳州市涡阳县育萃中学2019-2020学年高一上学期化学第二次月考试卷
- 2015-2016学年甘肃省平凉市庄浪县紫荆中学高二下学期期中化学试卷
- 北京市大兴区2017-2018学年高考理综-化学一模考试试卷
- 高中化学人教版 选修五 第三章 第四节 有机合成
- 上海市长宁区2017-2018学年高考化学二模考试试卷
- 高中化学鲁科版(2019)必修第二册 第1章第1节 原子结构与元素性质
- 高中化学人教版 选修四 第一章 化学反应与能量 第三节 化学反应热的计算 化学反应热的计算第二课时(反应热的计算)
- 高中化学人教版(2019)必修第二册 第八章第一节 自然资源的开发利用
- 2016-2017学年湖北省孝感市七校教学联盟高二下学期期中化学试卷
- 高中化学人教版(2019)必修第二册第六章 化学反应与能量 单元测试
- 高中化学人教版 选修五 第二章 第一节 烷烃和烯烃
- 细胞中水的存在形式有_____________和__________两种,_________与其他物质相结合,是细胞结构
- 向10mL2mol/L的氯化铝溶液中加入0.5mol/L的烧碱溶液,反应得到沉淀0.78g,则加入的烧碱溶液的体积为A.
- 如图所示:∠C=∠E=90°,AC=3,BC=4,AE=2,则AD=______.
- 能将乙烷、乙烯两种气体鉴别出来的试剂是 ( ) A.溴水 B.K
- 在我国的一本古代典籍中阐述了一项天文学方面的重要思考:“当日之冲(日冲:古代天文学概念,指的是太阳、地球与月亮等其他星体
- 下列关于化学反应的自发性叙述中正确的是 : ( )A.焓
- 下列关于对流层中热力环流的叙述,正确的是( ) A.气温越低的地方,气压越高 B.气温越高,大气密度越大 C.在同
- 函数在上有两个不同的零点,则实数的取值范围是 .
- 1933年罗斯福实行新政后,美国商品获得了更大的海外市场,国内商品价格也有一定提高,债务人特别是农民的债务负担减轻了将近
- 已知NH4CuSO3与足量的2mol/L硫酸溶液混合微热,产生下列现象: ①有红色金属生成 ②产生刺激性气味的
- 高一新教材中有一演示实验,用脱脂棉包住约0.2g过氧化钠粉末,置于石棉网上,往脱脂棉上滴水,观察到脱脂棉剧烈燃烧起来。(
- 下列有关细胞中“一定”的说法正确的是( ) ①光合作用一定在叶绿体中进行②有氧呼吸一定在线粒体中进行,有H2O生成一定
- 已知数列{an}满足a1=,an+1=an+.求证:(1)2<an<3;(2)an+1-2<(an-2);(3)an-2
- 自2011年1月起,我国在所有公共场所、室内工作场所、公共交通工具和其他可能的室内外公共场所完全禁止吸烟。目前这一目标还
- 假定你是中学生李华。高三将是辛苦忙碌的一年,不管自己还是父母都会很辛苦。每个家长都是望子成龙的,处在这一重要的学习阶段,
- 按每个小题后的要求做题,将答案写在题上。 1. A: He said, “She left 10 minutes ago
- 19.下面是“2012年中小学生上网调查”统计表,请阅读后回答问题。 学生上网普及率 小学87.5% 初中91.4% 高
- 十八大报告指出,全面准确贯彻“一国两制”、“港人治港”、“澳人治澳”、高度自治的方针,必须把坚持一国原则和尊重两制差异、
- The country life he was used to greatly since 1992. A、c
- 下列标题,不符合“大河流域——人类文明的摇篮”这一选题的是 A.金字塔的国度 B.奴隶

 的空间构型为。
的空间构型为。


 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为  ),则配体中NO
),则配体中NO  的大π键可表示为,空间构型为。
的大π键可表示为,空间构型为。


 形成配离子[Cd(NH3)4]2+中,中心离子的配位数为,画出配离子的结构式(不考虑立体构型)。
形成配离子[Cd(NH3)4]2+中,中心离子的配位数为,画出配离子的结构式(不考虑立体构型)。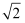 =1.414,
=1.414, 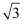 =1.732.则锡原子的半径为pm,锡的相对原子质量为(只需写出计算表达式)。
=1.732.则锡原子的半径为pm,锡的相对原子质量为(只需写出计算表达式)。 
 的空间构型是,其中Si的价层电子对数目为、杂化轨道类型为。
的空间构型是,其中Si的价层电子对数目为、杂化轨道类型为。



 )分子中氮、碳的杂化类型分别为、。
)分子中氮、碳的杂化类型分别为、。
 的大小关系为
的大小关系为 
 (填“>”“<”或“=”),原因是。
(填“>”“<”或“=”),原因是。
 不稳定遇到氧气被氧化成深蓝色的
不稳定遇到氧气被氧化成深蓝色的  ,试回答下列问题:
,试回答下列问题:  键的数目为个。
键的数目为个。 的空间结构为。
的空间结构为。 ,写出该反应的离子方程式。
,写出该反应的离子方程式。 属于立方晶体,如下图所示,
属于立方晶体,如下图所示, 
 ,阿伏加德罗常数为
,阿伏加德罗常数为 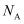 ,S原子填充在
,S原子填充在  构成的正四面体空隙中,则晶胞中正四面体的空隙填充率为,则
构成的正四面体空隙中,则晶胞中正四面体的空隙填充率为,则  (列出计算式)。
(列出计算式)。


