高考二轮复习知识点:浓硫酸的性质实验
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 实验探究题 | 详细信息 |
|
某兴趣小组在实验室用铜和硫酸为原料多种方法制取硫酸铜.制备方法如下:
Ⅰ.方法一:
|
|
| 2. 实验探究题 | 详细信息 | ||||||
|
某实验小组同学为了探究铜与浓硫酸的反应,进行了如下实验,实验装置如图所示.
实验步骤: ①先连接如图所示的装置,检查好气密性,再加入试剂; ②加热A试管,待B试管中品红溶液退色后,熄灭酒精灯; ③将Cu丝向上抽动离开液面. 请回答下列问题:
|
|||||||
| 3. 实验探究题 | 详细信息 |
|
为研究铜与浓硫酸的反应,某化学兴趣小组进行如下实验.
实验I:反应产物的定性探究,按如图装置(固定装置已略去)进行实验:
|
|
| 4. 实验探究题 | 详细信息 | ||||||||||||||||||||||||||||||||||||||||||||
|
中学教材显示“浓硫酸具有吸水性、脱水性、强氧化性,能使铁钝化”。某学习小组对“具有该四个特性的浓硫酸的浓度范围”进行了以下实验探究。
|
|||||||||||||||||||||||||||||||||||||||||||||
| 5. 实验探究题 | 详细信息 |
|
某化学小组欲进行如下实验探究金属与浓硫酸反应。试回答下列问题。
|
|
| 6. 单选题 | 详细信息 |
|
下列说法错误的是( )
A . 聚氯乙烯可以制食物保鲜膜
B . 铝热反应可用于焊接钢轨
C . 液氯可以保存在钢瓶中
D . 常温下可用铁槽车运输浓硫酸
|
|
| 7. 单选题 | 详细信息 | |||||||||||||||
|
用下列实验装置完成对应的实验,能达到实验目的的是( )
A . A
B . B
C . C
D . D
|
||||||||||||||||
| 8. 综合题 | 详细信息 |
|
化学与人类社会可持续发展密切相关,能源、环境、材料以及日常生活等都离不开化学.
|
|
| 9. 单选题 | 详细信息 | |||||||||||||||
|
浓硫酸与蔗糖反应的实验,对现象的解释不合理的是( )
A . A
B . B
C . C
D . D
|
||||||||||||||||
| 10. 实验探究题 | 详细信息 |
|
某化学兴趣小组设计下图实验装置研究浓硫酸与铁,铜两种金属分别如何反应,请参与探究并回答问题:
|
|
- 江苏省盐城市2020年高考化学6月模拟试卷
- 四川省绵阳市2016-2017学年高二下学期化学期末考试试卷
- 山西省大同市2017-2018学年高一下学期化学期末考试试卷
- 四川省南充市白塔中学2019-2020学年高二下学期化学开学考试卷
- 2015-2016学年北京二十四中高二下学期月考化学试卷(3月份)
- 2015-2016学年浙江省台州市、金华市、温州市部分学校联考高一下学期期中化学试卷
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.2元素周期表和元素周期律的应用
- 2017年安徽省合肥市高考化学一模试卷
- 2016-2017学年福建省福州市八县一中联考高三上学期期中化学试卷
- 2018年高考化学真题分类汇编专题06:化学反应速率和化学平衡
- 高中化学人教版必修1 第一章测试卷
- 2017-2018学年新人教版必修二高中化学第二章化学反应与能量2.3.1化学反应的速率
- 写出一个关于的二次函数 ▲ .使得当时, ;当时, .
- If better use is _____ yourspare time, you’ll make greater
- The newcomers found if impossible to _______themselves to th
- 中华文化“博大精深、源远流长”,对此下列说法不正确的是: A、中华文化有着辉煌的历程,秦朝时期在中华文化史上具有划时代的
- -- Do you mind my opening the window? It’s a bit hot in here
- 定义:对于函数f(x),若在定义域内存在实数x,满足f(﹣x)=﹣f(x),则称f(x)为“局部奇函数”. (1)已知二
- 某研究性学习小组设计了测定纯碱(Na2CO3)样品(只含NaCl杂质)中Na2CO3质量分数的实验方案.请回答下列问题:
- (5分)如图是探究“物体的动能的大小与什么因素有关?”的实验示意图.(1)该实验物体动能的大小是通过 ▲ 来反映的.(A
- 文化创作的灵感来自于( ) A.社
- 从2011年1月起,我国开始启用新的CPI统计方案,新的CPI统计方案仍然涉及8大类商品,但食品类商品在CPI统计中的权
- The dolphins are ______ interesting in the zoo.A.kinds ofB.k
- I spent the whole day repairing the motorbike. The work was_
- 若,,是与平行的单位向量,则=__
- 通以相等的电量,分别电解等浓度的硝酸银和硝酸亚汞(亚汞的化合价为+1)溶液,若被还原的硝酸银和硝酸亚汞的物质的量之比n(
- 19. (原创)下列各句中,没有语病的一句是()(3分) A. 英国大学里酝酿已久的对于脱欧公投结果的愤怒情绪,
- 线上与上文衔接的句子①-⑥,排列最恰当的一项是 在蒸汽机出现之前,必须解决许多技术问题和科学知识问题,如________
- “小嘛小儿郎,背着书包上学堂”,欢快熟悉的旋律响起,往昔岁月一一浮现,少年时代的回忆展开了它温馨美好的画卷。现在的孩子
- This job needs ______ patience and practice, after all, it w
- 设a,b∈R,则“(a-b)·a2<0”是“a<b”的( ) A.充分而不必要条件B.必要而不充分条件C.
- 17世纪,国际商业和金融中心是 A.阿姆斯特丹 B.伦敦 C.威尼斯 D.巴黎

 2CuO,CuO+H2SO4═CuSO4+H2O.对比甲的方案,你认为丙同学的优点是①,②.
2CuO,CuO+H2SO4═CuSO4+H2O.对比甲的方案,你认为丙同学的优点是①,②.

 cCu2S+dCuSO4+e H2O,则a:b=.
cCu2S+dCuSO4+e H2O,则a:b=.
 量取浓硫酸
量取浓硫酸  稀释浓硫酸
稀释浓硫酸  转移入容量瓶
转移入容量瓶  定容
定容






 溶液的试剂瓶不能用玻璃塞,原因可用化学方程式表示: .
溶液的试剂瓶不能用玻璃塞,原因可用化学方程式表示: .  ,在空气中会由淡绿色变为棕黄色,则这个变色过程中的
,在空气中会由淡绿色变为棕黄色,则这个变色过程中的 
 )中的
)中的  的含量.
的含量. 
 .当装置Ⅱ中出现现象时,立即停止同期.若
.当装置Ⅱ中出现现象时,立即停止同期.若  溶液的浓度为0.05
溶液的浓度为0.05 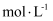 ,体积为20mL,此时收集到的
,体积为20mL,此时收集到的  与
与  的体积为297.6mL(已经折算为标准状况下的气体体积),由此可求得
的体积为297.6mL(已经折算为标准状况下的气体体积),由此可求得  溶液
溶液



