2015-2016学年北京二十四中高二下学期月考化学试卷(3月份)
2015-2016学年北京二十四中高二下学期月考化学试卷(3月份)
教材科目:化学
试卷分类:高二下学期
文件类型:.doc
发布时间:2026-04-01
授权方式:免费下载
下载地址:点此下载
教材科目:化学
试卷分类:高二下学期
文件类型:.doc
发布时间:2026-04-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 综合题 | 详细信息 |
|
已知下列热化学方程式:
①H2(g)+ ②H2(g)+ ③C(s)+ ④C(s)+O2(g)═CO2(g)△H=﹣393.5kJ•mol﹣1 回答下列各问题:
|
|
| 2. 单选题 | 详细信息 |
|
化学反应过程中总是伴随着能量的变化.下列反应既属于氧化还原反应,又属于吸热反应的是( )
A . 镁条在空气中燃烧
B . Ba(OH)2•8H2O与NH4Cl反应
C . 铝片与稀盐酸反应
D . 灼热的炭与CO2的反应
|
|
| 3. 单选题 | 详细信息 |
|
燃烧1g乙炔生成二氧化碳和液态水放出热量50kJ,则下列热化学方程式书写正确的是( )
A . 2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H=+50 kJ•mol﹣1
B . C2H2(g)+
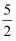 O2(g)═2CO2(g)+H2O(l)△H=﹣1 300 kJ
C . 2C2H2+5O2═4CO2+2H2O△H=﹣2 600 kJ
D . 2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H=﹣2 600 kJ•mol﹣1 O2(g)═2CO2(g)+H2O(l)△H=﹣1 300 kJ
C . 2C2H2+5O2═4CO2+2H2O△H=﹣2 600 kJ
D . 2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H=﹣2 600 kJ•mol﹣1
|
|
| 4. 单选题 | 详细信息 |
|
已知下列反应的热化学方程式为
·(1)CH3COOH(l)+2O2(g)═2CO2(g)+2H2O(l)△H1=﹣870.3kJ•mol﹣1 ·(2)C(s)+O2(g)═CO2(g)△H2=﹣393.5kJ•mol﹣1 ·(3)H2(g)+ 则反应2C(s)+2H2(g)+O2(g)═CH3COOH(l)的△H为( )
A . ﹣488.3 kJ•mol﹣1
B . ﹣191 kJ•mol﹣1
C . ﹣476.8 kJ•mol﹣1
D . ﹣1 549.6 kJ•mol﹣1
|
|
| 5. 单选题 | 详细信息 | ||||||||
|
下列电池工作时,O2在正极放电的是( )
A . A
B . B
C . C
D . D
|
|||||||||
| 6. 单选题 | 详细信息 |
|
查处酒后驾驶采用的“便携式乙醇测量仪”以燃料电池为工作原理,在酸性环境中,理论上乙醇可以被完全氧化为CO2 , 但实际乙醇被氧化为X,其中一个电极的反应式为:CH3CH2OH﹣2e﹣→X+2H+ . 下列说法中正确的是( )
A . 电池内部H+由正极向负极移动
B . 另一极的电极反应式为:O2+4e﹣+2H2O=4OH﹣
C . 乙醇在正极发生反应,电子经过外电路流向负极
D . 电池总反应为:2CH3CH2OH+O2→2CH3CHO+2H2O
|
|
| 7. 单选题 | 详细信息 |
|
镁及其化合物一般无毒(或低毒)、无污染,且镁原电池放电时电压高而平稳,使镁原电池越来越成为人们研制绿色原电池的关注焦点.其中一种镁原电池的反应为:xMg+Mo3S4
 MgxMo3S4;在镁原电池放电时,下列说法错误的是( ) MgxMo3S4;在镁原电池放电时,下列说法错误的是( )
A . Mg2+向正极迁移
B . 正极反应为:Mo3S4+2xe﹣=Mo3S42x﹣
C . Mo3S4发生氧化反应
D . 负极反应为:xMg﹣2xe﹣=xMg2+
|
|
| 8. 单选题 | 详细信息 |
|
人工光合作用能够借助太阳能,用CO2和H2O制备化学原料.下图是通过人工光合作用制备HCOOH的原理示意图,下列说法不正确的是( )
A . 该过程是将太阳能转化为化学能的过程
B . 催化剂a表面发生氧化反应,有O2产生
C . 催化剂a附近酸性减弱,催化剂b附近酸性增强
D . 催化剂b表面的反应是CO2+2H++2e一═HCOOH
|
|
| 9. 填空题 | 详细信息 |
|
已知下列热化学方程式:
①Fe2O3(s)+3CO(g)═2Fe(s)+3CO2(g)△H1=﹣25kJ•mol﹣1; ②3Fe2O3(s)+CO(g)═2Fe3O4(s)+CO2(g)△H2=﹣47kJ•mol﹣1; ③Fe3O4(s)+CO(g)═3FeO(s)+CO2(g)△H3=+19kJ•mol﹣1 . 写出FeO(s)被CO还原成Fe和CO2的热化学方程式. |
|
| 10. 综合题 | 详细信息 |
|
以下两个热化学方程式:
2H2(g)+O2(g)═2H2O(l)△H=﹣571.6kJ•mol﹣1 C3H8(g)+5O2(g)═3CO2(g)+4H2O(l)△H=﹣2220kJ•mol﹣1 试回答下列问题:
|
|
高中化学 试卷推荐
- 陕西省汉中市2020~2021学年下学期期末校级联考高一化学试题
- 陕西省宝鸡市金台区2020-2021学年高二上学期化学期中考试试卷(文)
- 广东省乐昌第二高中2020-2021学年高一上学期化学期中考试试卷
- 江西省赣抚吉名校2021-2022学年高三上学期化学开学考试试卷
- 浙江省丽水市2020-2021学年高二下学期普通高中教学质量监控化学试题
- 冲刺2021高考化学押题训练(八)化学反应速率与化学平衡
- 江苏省苏锡常镇四市2022届高三下学期教学情况调研(二)化学试题
- 安徽省芜湖市2020-2021学年高一下学期化学期中考试试卷
- 河南省济源平顶山许昌2021年高考化学二模试卷
- 浙江省舟山市2020-2021学年高一上学期化学期末考试试卷
- 北京市丰台区2021-2022学年高一下学期期中考试化学试题(B卷)
- 广东省东莞市七校2021-2022学年高一12月联考化学试题
最近更新
- 小明暑假去北京旅游,参观了圆明园遗址,导游说北京在近代曾经两次遭到外国列强的入侵和劫掠,大量珍贵文物至今流失海外。你知道
- 已知集合A={x|4≤≤16},B=[a,b],若A⊆B,则实数a-b的取值范围是( ) A. (-∞,-2]B
- 李清照的《武陵春》中表现景物依旧、人事已变,引发人内心伤感的词句是: , 。
- 2010年2月4日中新网消息,美国财经杂志《福布斯》公布香港富豪最新排行榜,长江实业及和记黄埔集团主席李嘉诚仍然稳坐香港
- “他们纵身一跃,划出了人生最壮丽的弧线;他们奋力一举,绽放出生命最高尚的光芒。”付东旭、陈及时、方超等勇救落水儿
- 独 处 涂华 ①在一次聚会的闲谈中,一位朋友大姐曾这样感慨,她说,就算十天内没有人和我说话,我也不会感觉到寂寞。说这番
- 小王同学在低倍显微镜视野中看到的物像如图,细胞甲作为主要观察的对象,他应将玻片A.向左上方移动
- 1986年3月为了发展我国高科技事业,批示了一项伟大计划,经过一百多位科学家的反复论证,形成了 A.《希望工程》
- 中华民国成立后,列宁高度评价了孙中山及其革命的卓越贡献,并认为孙中山领导的这场革命“正在破坏欧洲资产阶级的统治”。列宁的
- 已知函数时,则( ) 2,4,6 A. B. C.
- 分析一个DNA分子时,发现30%的脱氧核苷酸含有腺嘌呤,理论上该分子中一条链上鸟嘌呤含量的最大值可占此链碱基总数的 A.
- 对下面四个常见的化学反应进行对比分析: 分解反应:2KMnO4K2MnO4+MnO2+O2↑ 置换反应:2CuO+C2C
- 我国神话传说中,黄帝之后,黄河流域先后出了三个有名的人物叫尧、舜、禹,他们都是通过推举的方式成为部落联盟首领的。历史上把
- 如今,从中国的重要决定、决议的制定,到每年政府工作报告的起草;从重要人事任命,到重大工程建设,到民生政策的出台,都凝聚着
- 如图所示为人体内生理过程的图解,下列叙述正确的是()A. 肠道中的物质A通过协助扩散进入小肠上皮细胞内 B. 胰岛素能促
- p{font-size:10.5pt;line-height:150%;margin:0;padding:0;}td{f
- 十七届三中全会全面分析了当前形势和任务特别是经济形势,强调我国总体形势是好的,经济保持较快增长,金融业稳健运行,我国经济
- 7月6日,北京大兴召开民主党派座谈会。会议指出,近年来各民主党派提出了很多好的提案、议案和建议,并利用自身资源优势,开展
- 与纯水的电离相似,液氨中也存在着微弱的电离: 2NH3 NH4++NH2-,据此判断以下叙述中错误的是:A.液氨中含
- 如图1,窗框和窗扇用“滑块铰链”连接.图3是图2中“滑块铰链”的平面示意图,滑轨安装在窗框上,托悬臂安装在窗扇上,交点处
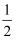 O2(g)═H2O(l)△H=﹣285.8kJ•mol﹣1
O2(g)═H2O(l)△H=﹣285.8kJ•mol﹣1







