冲刺2021高考化学押题训练(八)化学反应速率与化学平衡
教材科目:化学
试卷分类:高考
文件类型:.doc
发布时间:2026-04-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 综合题 | 详细信息 | ||||||
|
碳及其化合物在有机合成、溶液分析、电化学等方面,都有着重要应用。结合下列提供素材回答相关问题:
|
|||||||
| 2. 综合题 | 详细信息 |
|
明代《天工开物》记载了“火法”炼锌方法:“炉甘石(碳酸锌)十斤,装载入一泥罐内,然后逐层用煤炭饼垫盛,…,发火煅红,…,毁罐取出,即倭铅也”。现代工业开发了用NH3—NH4Cl水溶液浸出氧化锌烟灰(主要成分为ZnO 、Pb、CuO和As2O3)制取高纯锌的工艺流程如图所示。
已知浸出液含[Zn(NH3)4]2+、[Cu(NH3)4]2+、AsCl
|
|
| 3. 综合题 | 详细信息 | |||||||||||||||||||||||
|
据统计,约有90%以上的工业过程中需要使用催化剂,因此,对催化剂的研究已成为重要课题。
|
||||||||||||||||||||||||
| 4. 单选题 | 详细信息 |
|
蓝天保卫战—持续三年的大气治理之战,其中低成本、高效率处理SO2、NO2等大气污染物一直是化学研究的重点课题,研究它们的性质、制备在工业生产和环境保护中有着重要意义。一种处理SO2、NO2的研究成果,其反应原理为( )SO2(g)+NO2(g)=SO3(g)+NO(g) ΔH1=-41.8kJ·mol-1 , 标准状况下,SO2(g)+NO2(g)=SO3(s)+NO(g) ΔH2.下列有关说法错误的是
A . 该反应的ΔS>0
B . ΔH2<-41.8kJ·mol-1
C . SO2的生成速率和NO2的消耗速率相等说明该反应达到平衡状态
D . 标准状况下,该反应中每生成22.4L NO转移电子的数目约等于2×6.02×1023
|
|
| 5. 综合题 | 详细信息 |
|
汽车尾气中NOx(NO、NO2等)是形成雾霾及硝酸型酸雨的大气污染物之一、
|
|
| 6. 多选题 | 详细信息 | |||||||||||||||
|
在恒容密闭容器中发生反应:4HCl(g)+O2(g)
 2Cl2(g)+2H2O(g)。下列有关说法正确的是( ) 2Cl2(g)+2H2O(g)。下列有关说法正确的是( )
A . 该反应的ΔH>0
B . 400℃时,该反应的平衡常数的值为
 C . 400℃时,若X >8,则α2 >75%
D . 400℃时,向容器I平衡体系中再加入1molO2(g)和1molCl2(g),此时v (正)> v (逆)
C . 400℃时,若X >8,则α2 >75%
D . 400℃时,向容器I平衡体系中再加入1molO2(g)和1molCl2(g),此时v (正)> v (逆)
|
||||||||||||||||
| 7. 综合题 | 详细信息 |
|
实验室以天青石精矿(主要含SrSO4 , 还含有少量SiO2、CaSO4、BaSO4)为原料制取SrSO4 , 其实验流程如下:
|
|
| 8. 多选题 | 详细信息 |
|
丙酮是重要的有机合成原料,可以由过氧化氢异丙苯合成。其反应为:
 ,为了提高过氧化氢异丙苯的转化率,反应进行时需及时从溶液体系中移出部分苯酚。过氧化氢异丙苯的转化率随反应时间的变化如图所示。设过氧化氢异丙苯的初始浓度为x mol·L-1 , 反应过程中的液体体积变化忽略不计。下列说法正确的是( ) ,为了提高过氧化氢异丙苯的转化率,反应进行时需及时从溶液体系中移出部分苯酚。过氧化氢异丙苯的转化率随反应时间的变化如图所示。设过氧化氢异丙苯的初始浓度为x mol·L-1 , 反应过程中的液体体积变化忽略不计。下列说法正确的是( )
A . a、c 两点丙酮的物质的量浓度相等
B . b、c两点的逆反应速率:v(b)<v(c)
C . 100 ℃时,0~5 h 之间丙酮的平均反应速率为 0.14x mol·L-1·h-1
D . 若b点处于化学平衡,则120℃时反应的平衡常数

|
|
| 9. 综合题 | 详细信息 |
|
一种从阳极泥(主要成分为 Cu、Ag、Pt、Au、Ag2Se和Cu2S等)中回收 Se和贵重金属的工艺流程如下图所示。
已知:①该工艺中萃取与反萃取原理为: ② 回答下列问题:
|
|
| 10. 综合题 | 详细信息 |
|
二甲醚(CH3OCH3)被称为“21世纪的清洁燃料”。以 CO2、H2为原料制备二甲醚涉及的主要反应如下:
I. Ⅱ. 回答下列问题:
|
|
- 2016-2017学年河南省南阳市邓州市白牛高中高二上学期开学化学试卷
- 河南周口中英文学校2017-2018学年高三下学期化学第一次月考考试试卷
- 广东省深圳市2020年高考理综-化学二模试卷
- 辽宁省葫芦岛市2017-2018学年高考理综-化学二模考试试卷
- 安徽省皖江名校2017-2018学年高考理综-化学模拟考试试卷
- 辽宁省锦州市2019-2020学年高二下学期化学期末考试试卷
- 宁夏吴忠市吴忠中学2018-2019学年高一化学上学期期末模拟试卷
- 2016-2017学年河南省南阳市高二下学期期中化学试卷
- 2016-2017学年江西省赣州市厚德外国语学校高一上学期开学化学试卷
- 2015-2016学年山西省运城市高一下学期期中化学试卷
- 贵州省铜仁市西片区高中教育联盟2017-2018学年高二下学期化学期末考试试卷
- 人教版化学高二选修6第一单元实验1-1 蓝瓶子同步练习
- 如果您暑期准备或可能带孩子去上海参观世博会,原因是什么?(可多选)概括图表反映的现象:_________________
- 下列关于细胞结构和功能的叙述正确的是( ) A.精细胞和根尖分生区细胞都有细胞周期 B.乳酸菌、酵母菌和蓝藻的细胞内都
- My father warned me going to the West Coast because i
- 读某地等高线示意图,回答6﹣8题.6.山峰甲的海拔高度可能为( ) A.1000米 B.50
- Hurry up! There will be a movie ______ three minutes. A.in
- 用计算器求(-2184)÷14,按键顺序且显示的结果是: __________________________;
- 下列剪纸图案中,属于中心对称图形的是() A. B. C. D.
- 如图所示,在跟匀强磁场垂直的平面内放置一个折成锐角的裸导线MON,∠MON=α。在它上面搁置另一根与ON垂直的导线PQ,
- ________not todrive after drinking, some drivers are still t
- 圆周上有6个等分圆周的点,从这6个点中任取3点构成三角形,求所取三角形为直角三角形的概率.
- 阅读材料: 英国人一定是丧失了所有的道德和自由感,否则怎么会对这场世界经历过的最重要革命,对它正在进行的庄严方式,不表敬
- ---- Here. Your new computer is ready. ----Thank you. ---- _
- 已知ax2yb﹣bxay5=cx2y5,且无论x,y取何值该等式恒成立,则c的值等于__________.
- 下列各溶液中,微粒的物质的量浓度关系正确的是 A.0.1 mol/L Na2CO3溶液:c(OH-)=c(HCO3-)+
- 一个质点在恒力F作用下,在xOy平面内从O点运动到A点的轨迹如图12-1所示,且在A点时的速度方向与x轴平行,则恒力F的
- 2009年8月12日,哈尔滨市市长张效廉在市政府棚改工作推进专题会议上说,棚户区里住着生活最困难的人群,这里的居民,没有
- Thepassengers on the bus watched with sympathy as Susan made
- 2012年2月1日,新华社受权发布《关于加快推进_____________持续增强农产品供给保障能力的若干意见》,这是新
- We had ________ computer games yesterday. A. a fun playing
- 某浓度的氨水中存在下列平衡:NH3·H2ONH+OH-,如想增大NH3·H2O的电离度而不增大OH-的浓度,应采取的措
 ,熔点:
,熔点:  ,沸点:
,沸点:  )的反应如下:
)的反应如下: 





 液态水变成气态水吸收
液态水变成气态水吸收  的热量。则
的热量。则 
 。
。 的起始量进行反应①,下列能说明反应①达到化学平衡状态的是(填字母序号)。
的起始量进行反应①,下列能说明反应①达到化学平衡状态的是(填字母序号)。  不变 d.分压平衡常数
不变 d.分压平衡常数  不变
不变 f.混合气体的压强不变
f.混合气体的压强不变 的合金),利用
的合金),利用  和
和  制备二甲醚。观察图1回答问题。催化剂中
制备二甲醚。观察图1回答问题。催化剂中  约为时最有利于二甲醚的合成。
约为时最有利于二甲醚的合成。

 和
和  ,在不同条件下发生反应:
,在不同条件下发生反应:  。实验测得
。实验测得  的物质的量随温度、压强的变化如图3所示。
的物质的量随温度、压强的变化如图3所示。
 时,压强为
时,压强为  反应平衡时
反应平衡时  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。 M点
M点  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。 恒容密闭容器中进行上述反应(起始投料不变),在不同温度下上述反应的平衡常数的对数
恒容密闭容器中进行上述反应(起始投料不变),在不同温度下上述反应的平衡常数的对数  如图4所示。则温度为
如图4所示。则温度为  时,平衡常数
时,平衡常数  (保留三位小数),B、C、D、E四点中能正确表示该反应的
(保留三位小数),B、C、D、E四点中能正确表示该反应的  与T的关系的点为。
与T的关系的点为。
 。
。

 -k2
-k2  ,其中w为反应的瞬时总速率,等于正反应速率和逆反应速率之差,k1、k2是正、逆反应速率常数,则合成氨反应N2+3H2
,其中w为反应的瞬时总速率,等于正反应速率和逆反应速率之差,k1、k2是正、逆反应速率常数,则合成氨反应N2+3H2 




 (aq)
(aq) 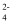 (aq)达到平衡,则反应的平衡常数为[Ksp(SrSO4)=3.2×10−7 , Ksp(SrCO3)=5.6×10−10]。
(aq)达到平衡,则反应的平衡常数为[Ksp(SrSO4)=3.2×10−7 , Ksp(SrCO3)=5.6×10−10]。



 ;
; 易与 Ag+形成配离子:
易与 Ag+形成配离子:  ,常温下该反应的平衡常数
,常温下该反应的平衡常数  。
。 ,该反应的平衡常数K'=。[已知
,该反应的平衡常数K'=。[已知  ]
]



 的△H=。
的△H=。

 的选择性=
的选择性=  ×100%。其中表示平衡时
×100%。其中表示平衡时  。已知:
。已知:  ,其中 Kp为以分压表示的平衡常数,T 为热力学温度。
,其中 Kp为以分压表示的平衡常数,T 为热力学温度。
 b.
b. 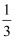 ~
~ 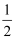 d. >
d. >  ,反应速率v=v正-v逆=k正p(CO2)·p(H2)-k逆p(CO)·p(H2O),其中k正、k逆分别为正、逆反应速率常数,p为气体的分压(分压=总压×物质的量分数)。
,反应速率v=v正-v逆=k正p(CO2)·p(H2)-k逆p(CO)·p(H2O),其中k正、k逆分别为正、逆反应速率常数,p为气体的分压(分压=总压×物质的量分数)。
 投料,CO2转化率为50%时,
投料,CO2转化率为50%时,  ,用气体分压表示的平衡常数 Kp=。
,用气体分压表示的平衡常数 Kp=。


