江苏省南京市六校联合体2022-2023学年高三8月联合调研化学试卷
江苏省南京市六校联合体2022-2023学年高三8月联合调研化学试卷
教材科目:化学
试卷分类:高三上学期
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
教材科目:化学
试卷分类:高三上学期
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | 详细信息 |
|
若将铜丝插入热浓硫酸中进行如图(a~d均为浸有相应试液的棉花)所示的探究实验,下列分析正确的是( )
A .
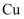 与浓硫酸反应,只体现 与浓硫酸反应,只体现  的酸性
B . a处变红,说明 的酸性
B . a处变红,说明  是酸性氧化物
C . b或c处褪色,均说明 是酸性氧化物
C . b或c处褪色,均说明  具有漂白性
D . 试管底部出现白色固体,说明反应中无 具有漂白性
D . 试管底部出现白色固体,说明反应中无  生成 生成
|
|
| 2. 单选题 | 详细信息 |
|
中国人民在悠久的历史中创造了绚丽多彩的中华文化,下列说法错误的是( )
A . 宋∙王希孟《千里江山图》卷中的绿色颜料铜绿的主要成分是碱式碳酸铜
B . “冰糖葫芦”是一种传统美食,山楂外面包裹的“糖衣”的主要成分是麦芽糖
C . “澄泥砚”是一种传统工艺品,是用胶泥烧制而成,其主要成分为硅酸盐
D . “蜀绣”是用蚕丝线在丝绸或其他织物上绣出图案的工艺,蚕丝的主要成分蛋白质
|
|
| 3. 单选题 | 详细信息 |
|
双氧水和“84”消毒液两者混合时可发生反应:NaClO+H2O2=NaCl+H2O+O2↑。下列有关说法错误的是( )
A . Na2O2中含有非极性共价键
B . NaClO 的电子式为
 C . H2O2中O元素的化合价为-1
D . H2O的空间构型为直线形
C . H2O2中O元素的化合价为-1
D . H2O的空间构型为直线形
|
|
| 4. 单选题 | 详细信息 |
|
短周期元素X、Y、Z、M的原子序数依次增大,他们组成一种团簇分子,结构如图所示。X、M的族序数等于周期数,Y是地壳中最丰富、分布最广的元素,Z原子最外层电子数为2。下列说法错误的是 ( )
A . 该团簇分子的分子式为 X2Z2M2Y6
B . 简单离子半径:Y>M
C . 工业上常电解熔融的ZY制取Z单质
D . 第一电离能: M<Z
|
|
| 5. 单选题 | 详细信息 |
|
氯仿(CHCl3)常因保存不慎而被氧化,产生剧毒物光气(COCl2),下列说法正确的是( )
A . CHCl3、COCl2分子中所有原子的最外层电子都满足8电子稳定结构
B . COCl2、CO2都是由极性键构成的非极性分子
C . 氯原子基态核外电子排布式为3s23p5
D . VIIA族元素氢化物的晶体类型相同,沸点:HF>HCl
|
|
| 6. 单选题 | 详细信息 |
|
周期表中VIIA族中氯元素及其化合物在生产、生活中有着广泛的应用。盐酸工业用途广泛,稀盐酸和稀氢氧化钠溶液反应的中和热为57.3 kJ/mol;氯化镁,通常含有六个分子的结晶水,即MgCl2·6H2O,易潮解,置于干燥空气中会风化而失去结晶水,若在空气中加热MgCl2·6H2O,生成的是Mg(OH)Cl或MgO。次氯酸钠与二氧化碳反应产生的次氯酸是漂白剂的有效成分。下列化学反应表示正确的是( )
A . 在空气中加热MgCl2·6H2O:MgCl2·6H2O=Mg(OH)Cl+HCl↑+5H2O↑
B . 过量SO2通入NaClO溶液中:SO2+H2O+ClO-=HClO+
 C . 用惰性电极电解饱和MgCl2溶液:2Cl-+2H2O
C . 用惰性电极电解饱和MgCl2溶液:2Cl-+2H2O Cl2↑+H2↑+2OH-
D . 稀硫酸与稀氢氧化钾溶液发生反应:H2SO4(l)+2KOH(l)=K2SO4(l)+2H2O(l) △H=-57.3 kJ/mol Cl2↑+H2↑+2OH-
D . 稀硫酸与稀氢氧化钾溶液发生反应:H2SO4(l)+2KOH(l)=K2SO4(l)+2H2O(l) △H=-57.3 kJ/mol
|
|
| 7. 单选题 | 详细信息 |
|
次氯酸钠与二氧化碳反应产生的次氯酸是漂白剂的有效成分。下列有关物质的性质与用途具有对应关系的是( )
A . NaCl易溶于水,可用于工业电解制备钠
B . FeCl3溶液具有酸性,可用于腐蚀印刷电路板上的Cu
C . 次氯酸(盐)具有不稳定性,可作杀菌消毒剂,还可作漂白剂
D . 氨气具有还原性,用浓氨水检验氯气管道是否泄漏
|
|
| 8. 单选题 | 详细信息 |
|
工业上以
 和纯碱为原料制备无水NaHSO3的主要流程如图,下列说法错误的是( ) 和纯碱为原料制备无水NaHSO3的主要流程如图,下列说法错误的是( )
已知:NaHSO3溶液呈弱酸性
A . 工业上用黄铁矿(FeS2 , 其中硫元素为-1价)在高温下和氧气反应制备SO2
B . 结晶后母液中含有NaHCO3
C . 中和后溶液中含Na2SO3和NaHCO3
D . 侯氏制碱法以H2O、NH3、CO2、NaCl为原料制备NaHCO3和NH4Cl
|
|
| 9. 单选题 | 详细信息 |
|
莽草酸(a)是抗病毒和抗癌药物中间体,其官能团修饰过程如图所示,下列说法错误的是( )
A . “M”为甲醇
B . 有机物b存在顺反异构
C . 等物质的量的a和b分别与足量的NaOH溶液反应,消耗NaOH的量不同
D . 有机物a、b、c分子中均含有3个手性碳原子
|
|
| 10. 单选题 | 详细信息 |
|
随着人们环保意识的增强,燃油汽车都已经装上了尾气处理装置。汽车尾气在催化剂作用下可发生如下反应:2NO(g)+2CO(g)
 2CO2(g)+N2(g),下列说法错误的是( ) 2CO2(g)+N2(g),下列说法错误的是( )
A . 该反应能自发进行,△H﹤0
B . 反应的平衡常数表达式为
 C . 反应中每消耗1molNO转移电子的数目约等于
C . 反应中每消耗1molNO转移电子的数目约等于 D . 实际应用中,加入高效催化剂的量越多,燃油汽车排放的尾气对空气污染程度越小
D . 实际应用中,加入高效催化剂的量越多,燃油汽车排放的尾气对空气污染程度越小
|
|
高中化学 试卷推荐
- 湖北省天门市、仙桃市、潜江市2017-2018学年高一下学期化学期末考试试卷
- 2015-2016学年甘肃省陇南市西和二中高一下学期期中化学试卷
- 第14讲:元素周期表和元素周期律
- 贵州省贵阳市2017-2018学年高考理综-化学一模考试试卷
- 河北省石家庄市2020年高考化学一模试卷
- 2015-2016学年河南省郑州106中高一下学期期中化学试卷
- 专题04:氧化还原反应
- 山西省晋中市2020年高考化学三模试卷
- 吉林省五地六市联盟2018-2019学年高二下学期化学期末考试试卷A卷
- 2016-2017学年黑龙江省双鸭山市友谊县红兴隆管理局一中高三上学期期中化学试卷
- 高中化学鲁科版(2019)选择性必修2 第1章第1节 原子结构模型
- 北京市房山区2020年高考化学一模试卷
最近更新
- 下列物质的用途与其物理性质有关的是 A.氧气用于急救病人 B.氢气用作清洁燃料 C.稀有气体做保护气D.铜丝做电线
- 世界三大宗教创立的先后顺序是 A.伊斯兰教、佛教、基督教 B.基督教、佛教、伊斯兰教 C.佛教、伊斯兰教、基督教
- 质量为m的物体从高处静止释放后竖直下落。在某时刻受到的空气阻力为f,加速度为a=g,则f的大小是…( )A.f=m
- Se是人体必需微量元素,下列有关和的说法正确的是( ) A. 和互为同素异形体
- 某校规划在一块长AD为18m,宽AB为13m的长方形场地ABCD上,设计分别与AD,AB平行的横向通道和纵向通道,其余部
- 常温下,向含有H2SO4的CuSO4溶液中逐滴加入含a mol溶质的NaOH溶液,恰好使溶液的pH=7,下列叙述错误的是
- 两个亲本的基因型分别为AAbb和aaBB,这两对基因按自由组合定律遗传。要培育出基因型为aabb的新品种,最简捷的方法是
- 55. There have been many changes in _____ history of _____ E
- 多党制是法国政体的一个特点,其主要表现有 ①存在两个左右政治局势的两大政党 ②党外有党,党内有派,党派林立 ③左右
- We try to find a table for seven, but they were all______. A
- 实用类文本阅读(12分) 阅读下面的文字,完成4-6题。(12分) 材料一:美国东部时间4月7日上午,美国中车麻省公司3
- 氢氧化镁固体在水中达到溶解平衡Mg(OH)2(s)Mg2+(aq)+2OH-(aq)时,为使Mg(OH)2固体的量减少,
- F省人大常委会向市民公开征集未来5年立法项目与建议草案,10天内共收到市民意见2081件次,其中立法建议221件,60%
- 下列对维护空气质量不利的作法的是( ) A、把庄稼的桔杆粉碎后翻耕 B、秋收后在田地焚烧麦桔 C、实行城
- 与直线垂直的抛物线的切线方程是 A. B. C. D.
- 下列说法不正确的是 () A
- 阅读下面的文字,完成6~8题。 “皮影”是对皮影戏和皮影戏人物(包括场面道具景物)制品的通用称谓
- 2015年,“中国梦”“大部制”依然是中国民众关注的热词。对中央权力部门进行改革,让权力相互制约在阳光下运行,成为人类文
- 下列四地所代表的实地面积最大的是( ) A B
- 如图所示,将一个体积为1.0×10-3m3、重6N的木块用细线系在底面积为400cm2的圆柱形容器的底部。当容器中倒入足







