高考二轮复习知识点:高考真题变式分类汇编:化学平衡的计算
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | 详细信息 |
|
对于某反应X+3Y=2E+2F,在甲、乙、丙、丁四种不同条件下,分别测得反应速率为:甲,v(X)=0.3mol•L﹣1min﹣1;乙,v(Y)=1.2mol•L﹣1min﹣1;丙,v(E)=0.6mol•L﹣1min﹣1;丁,v(F)=0.9mol•L﹣1min﹣1 . 则反应最快的是( )
A . 甲
B . 乙
C . 丙
D . 丁
|
|
| 2. 综合题 | 详细信息 | ||||||||||||||||||||
|
游离态碳在自然界存在形式有多种,在工业上有着重要用途。请回答下列问题:
|
|||||||||||||||||||||
| 3. 综合题 | 详细信息 |
|
工业上CO2用于生产燃料甲醇,既能缓解温室效应,也为能源寻找了新渠道。合成甲醇的反应为:CO2(g)+3H2(g)=CH3OH(g)+H2O(g)。
|
|
| 4. 综合题 | 详细信息 | ||||||||||||
|
石油化工生产中,利用裂解反应可以获得重要化工原料乙烯、丙烯。一定条件下,正丁烷裂解的主反应如下:
反应I
C4H10(g) 反应Ⅱ C4H10(g) 回答下列问题:
|
|||||||||||||
| 5. 多选题 | 详细信息 |
|
把2.5 mol A和2.5 mol B混合盛入容积为2 L的密闭容器里,发生如下反应:
3A(g) +B(g) ⇋ x C(g) + 2D(g),经5 s反应达平衡,在此5 s内C的平均反应速率为0.2 mol·L-1·s-1 , 同时生成1 mol D,下列叙述中错误的是:( )
A . x=4
B . 达到平衡状态时A的转化率为50%
C . 5s内B的反应速率v(B)=0.05 mol/(L·s)
D . 达到平衡状态时容器内气体的压强与起始时压强比为5: 6
|
|
| 6. 实验探究题 | 详细信息 |
|
亚硝酰氯(ClNO)是有机物合成中的重要试剂,可由NO与Cl2在常温常压下反应得到。ClNO部分性质如下:黄色气体,熔点:-59.6℃,沸点:-6.4℃,遇水易水解。已知:HNO2既有氧化性又有还原性;AgNO2微溶于水,能溶于硝酸:AgNO2+HNO3=
AgNO3+ HNO2。
|
|
| 7. 综合题 | 详细信息 |
|
CoS2催化CO烟气脱硫具有广阔的工业化前景。回答下列问题:
|
|
| 8. 综合题 | 详细信息 | ||||||||||||||||||
|
生产生活中氨及铵盐有重要用途,而汽车尾气中含 NO、NO2则应降低其排放.
|
|||||||||||||||||||
| 9. 单选题 | 详细信息 |
|
一定温度下,在一个容积为2L的密闭容器中发生反应:
 ,若0~10s内消耗了2mol C,下列说法正确的是( ) ,若0~10s内消耗了2mol C,下列说法正确的是( )
A . 0~10s内用C表示的平均反应速率为v(C)=0.1 mol·L-1·s-1
B . 当v正(N2O3)= v逆(CO2)时,反应达到平衡状态
C . 升高温度正反应速率加快,逆反应速率减慢
D . 该反应达平衡后,减小反应体系的体积,平衡向逆反应方向移动
|
|
| 10. 单选题 | 详细信息 |
|
氨的工业合成对工农业生产具有划时代意义。在容积固定的密闭容器中充入一定量的
 和 和  ,一定条件下发生反应 ,一定条件下发生反应  。下列有关叙述正确的是( ) 。下列有关叙述正确的是( )
A . 相同条件下,
 B . 温度不变时,向容器中充入氦气,反应速率加快
C . 升高温度,正反应速率减小,平衡向逆反应方向移动
D . 增大
B . 温度不变时,向容器中充入氦气,反应速率加快
C . 升高温度,正反应速率减小,平衡向逆反应方向移动
D . 增大  的浓度,能提高 的浓度,能提高  的转化率 的转化率
|
|
- 备考2019年高考化学二轮专题 12 常见有机物(必修)
- 人教版化学高二选修3第三章第四节离子晶体同步练习
- 广东省汕尾龙山中学2019-2020学年高二下学期化学第二次月考试卷
- 福建省泉州市2018-2019学年高二上学期化学期末考试试卷
- 广东省深圳市红岭中学等四校2019-2020学年高二下学期化学期中考试试卷
- 2015-2016学年山东省潍坊市高一下学期期中化学试卷
- 2015-2016学年广东省东莞市北师大石竹附属学校高一下学期期中化学试卷
- 广西桂林市、贺州市2017-2018学年高三上学期理综-化学期末考试试卷
- 人教版高中化学选修五 第五章 进入合成有机高分子化合物的时代—单元综合检测题
- 2015-2016学年湖北省部分重点中学高一下学期月考化学试卷(3月份)
- 浙江省温州市环大罗山联盟2018-2019学年高二下学期化学期中考试试卷
- 2015-2016学年北京二十四中高一上学期期中化学试卷
- 家庭照明电路中的用电器间是____________(串联/并联)连接的;使用测电笔检测电路时,若氖管发光,表明测电笔的笔
- 下列各项中最能体现中国在国际社会长期发挥重要作用的是( )A.担任联合国安理会常任理事国 B.在亚非会议上
- 英国工业革命中普遍出现了一种“由需要导致发明的模式”,这一模式最早体现在 A.毛纺织业的发展中B.棉纺织业的发展中C.交
- 假设你在自己的班级就学生对校服态度问题进行了调查(survey)。下面是对部分学生调查的统计表。请参照该统计表给校报写一
- 求下列函数的导数. y=3xex-2x+e;
- My mother used to ask me what the most important part of
- Faced with a toughjob market, fresh graduates are dreaming o
- 祖国统一、民族团结是各族人民之福,我们要不断增进民族团结、十分珍惜民族团结、自觉维护民族团结。这是因为
- 《十二铜表法》第九表规定了立法者不得为个人利益立法,贪官污吏应受到惩罚,任何人非经审判,不得被处死刑;第八表限制了利率,
- 国家决定限期淘汰一次性发泡塑料餐具等—批污染环境的产品,鼓励生产有利于节约资源、保护环境的产品。出台这项政策的原因是:(
- ---Do you know Peng Liyuan? --- Of course, she is F
- 在体积相同的两个密闭容器中分别充满O2、O3气体,当这两个容器内温度和气体密度相等时,下列说法正确的是() A.两种气体
- 小明在探究电流通过导体产生的热量与哪些因素有关时,把两段金属丝A、B(已知A、B两金属丝的电阻的大小关系为)串联后,分别
- Airpollution, such as haze, has become a serious prob
- 下列有关实验现象的描述正确的是()A. 硫在氧气中燃烧发出淡蓝色火焰 B. 无色酚酞试液遇稀盐酸变成红色 C. 硫酸铜溶
- 唐代黄巢的“冲天香阵透长安,满城尽带黄金甲”描写的是美丽的菊花。俗称的一朵菊花,实际上是( )A.一个花序B.一朵单
- 2011年9月20日,杂交水稻之父、袁隆平院士指导的超级稻试验田亩产达到920000克。那么试验田亩产数用科学记数法表示
- (海南卷) 下列有关线粒体和叶绿体的叙述,错误的是 A. 线粒体和叶绿体携带的遗传信息可以表达出来 B. 线粒体和叶绿体
- 下图是实验室制取气体的有关装置图,据图回答下列问题。 A B C
- 有X、Y、Z三种金属,如果把X和Y分别放入稀硫酸中,X溶解并产生氢气,Y不反应;如果把Y和Z分别放入硝酸银溶液中,过一会
 N2(g)+CO2(g),测得不同时间内各物质的物质的量如下表:
N2(g)+CO2(g),测得不同时间内各物质的物质的量如下表:


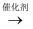 CH4(g)+CH3CH-CH3(g) △H1;
CH4(g)+CH3CH-CH3(g) △H1; ,前2amin内正丁烷的平均反应速率v(正丁烷)=MPa·min-1。
,前2amin内正丁烷的平均反应速率v(正丁烷)=MPa·min-1。 、
、  ,则该温度下反应I的压力平衡常数Kp=MPa(用平衡分压代替平衡浓度计算,分压一总压×物质的量分数,保留三位有效数字)。
,则该温度下反应I的压力平衡常数Kp=MPa(用平衡分压代替平衡浓度计算,分压一总压×物质的量分数,保留三位有效数字)。


 CoS(s) +COS(g) ∆H1
CoS(s) +COS(g) ∆H1 2CO2(g)+S(s) ∆H4=。 (用∆H1、 ∆H2、∆H3表示)
2CO2(g)+S(s) ∆H4=。 (用∆H1、 ∆H2、∆H3表示)

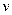 (N2)随时间变化如下表:
(N2)随时间变化如下表:
 图二
图二 
 N2+2CO2的反应速率随强的变化如图所示. 结合(3)中反应机理,试从吸附和解吸角度解释 bc段化学反应速率下降的原因 .
N2+2CO2的反应速率随强的变化如图所示. 结合(3)中反应机理,试从吸附和解吸角度解释 bc段化学反应速率下降的原因 .



