高考二轮复习知识点:物质的量浓度
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 综合题 | 详细信息 |
|
甲醛是深受关注的有机化合物.甲醛含量的测定有多种方法,例如:在调至中性的亚硫酸钠溶液中加入甲醛水溶液,经充分反应后,产生的氢氧化钠的物质的量与甲醛的物质的量相等,然后用已知浓度的硫酸滴定氢氧化钠.
完成下列填空:
|
|
| 2. 单选题 | 详细信息 |
|
NA为阿伏加德罗常数的值.下列说法正确的是( )
A . 0.1 mol 的11B中,含有0.6NA个中子
B . pH=1的H3PO4溶液中,含有0.1NA个H+
C . 2.24L(标准状况)苯在O2中完全燃烧,得到0.6NA个CO2分子
D . 密闭容器中1 mol PCl3与1 mol Cl2反应制备 PCl5(g),增加2NA个P﹣Cl键
|
|
| 3. 单选题 | 详细信息 |
|
洁厕灵和84消毒液混合使用会发生反应: NaClO+2HCl=NaCl+Cl2↑+H2O,生成有毒的氯气。下列说法正确的是( )
A . 每生成1mol氯气,转移的电子数为2NA
B . 1 mol NaCl含有的电子数为28NA
C . 1L0.2mol/ L NaClO溶液中含有的次氯酸根离子数为0.2NA
D . 标准状况下,将22.4L HCl溶解在0.5L水中,形成2mol/L的盐酸
|
|
| 4. 实验探究题 | 详细信息 |
|
已知: ①亚硝酸钠(NaNO2)是一种食品添加剂,为无色、无气味的同体,具有防腐和抗氧化作用。②AgNO2 是一种微溶于水、易溶于酸的浅黄色固体。
I.问题探究
|
|
| 5. 实验探究题 | 详细信息 | |||||||||||||||
|
为了探究氨气及氨水的还原性,某兴趣小组同学设计了以下探究活动。
I.探究氨气的还原性 该兴趣小组同学利用以下装置(夹持,加热仪器略)探究氯气与氨气的反应,其中A、F分别为氯气和氨气的发生装置,B 为纯净干燥的氯气与氨气反应的装置。
请回答下列问题:
|
||||||||||||||||
| 6. 单选题 | 详细信息 |
|
已知单位体积的稀溶液中,非挥发性溶质的分子或离子数越多,该溶液的沸点就越高。则下列溶液沸点最高的是()
A .
|
|
| 7. 单选题 | 详细信息 |
|
下列有关1mol NaOH的说法中,正确的是( )
A . NaOH的摩尔质量为40g
B . 1mol NaOH的质量为40g/mol
C . 标准状况下,1mol NaOH所占的体积为22.4L
D . 将1mol NaOH溶于水配成100ml溶液,则溶液中溶质的物质的量浓度为10mol/L
|
|
| 8. 单选题 | 详细信息 |
|
下图是实验室硫酸试剂标签上的部分内容,据此下列说法正确的是( )
A . 配制500mL4.6 mol/L的稀硫酸需取该硫酸125mL
B . 1molAl与足量的该硫酸反应产生3g氢气
C . 该硫酸的物质的量浓度为9.2mol/L
D . 将该硫酸加水配成质量分数49%的溶液时其物质的量浓度等于9.2mol/L
|
|
| 9. 单选题 | 详细信息 |
|
向mg镁和铝的混合物中加入适量的稀硫酸,恰好完全反应生成标准状况下的气体bL。向反应后的溶液中加入cmol/L氢氧化钾溶液VmL,使金属离子刚好沉淀完全,得到的沉淀质量为ng。再将得到的沉淀灼烧至质量不再改变为止,得到固体pg。则下列关系错误的是( )
A .
 B .
B .  C . n=m+17Vc
D .
C . n=m+17Vc
D . 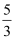 m<p< m<p< 
|
|
| 10. 单选题 | 详细信息 |
|
固体界面上强酸的吸附和离解是多相化学在环境、催化、材料科学等领域研究的重要课题。下图为少量HCl气体分子在253 K冰表面吸附和溶解过程的示意图。下列叙述错误的是( )
A . 冰表面第一层中,HCl以分子形式存在
B . 冰表面第二层中,H+浓度为5×10−3 mol·L−1(设冰的密度为0.9 g·cm−3)
C . 冰表面第三层中,冰的氢键网格结构保持不变
D . 冰表面各层之间,均存在可逆反应HCl
 H++Cl− H++Cl−
|
|
- 山东省威海荣成市2020-2021学年高一上学期化学期中考试试卷
- 安徽宣城市某高中2020-2021学年高二上学期化学10月月考试卷
- 江苏省常熟市2020-2021学年高一上学期化学期中考试试卷
- 河北省廊坊市香河县2020-2021学年高一下学期化学期末考试试卷
- 辽宁省葫芦岛市2022届高三一模化学试题
- 天津市静海区四校2020-2021学年高二上学期化学12月月考试卷
- 湖北省新高考联考协作体2021-2022学年高一下学期期中考试化学试题
- 宁夏中卫市2021年高考化学三模试卷
- 陕西省渭南市临渭区尚德中学2020-2021学年高三上学期化学第一次月考试卷
- 浙江省杭州地区(含周边)重点中学2021-2022学年高三上学期期中考试化学试题
- 福建省宁德市2021-2022学年高二上学期期末质量检测化学试题
- 广东省佛山市2020-2021学年高二上学期化学期末考试试卷
- - Hello, myname is Johnson. I believe you have a room _____
- 已知曲线E:ax2+by2=1(a>0,b>0),经过点M(,0)的直线l与曲线E交 于点A、B,且=-2.(1)若点B
- 基因的自由组合定律发生于图中哪个过程() AaBb1AB∶1Ab∶1aB∶1ab雌雄配子随机结合子代9种基因型4种表现型
- 在特异性免疫中发挥作用的主要细胞是() A.红细胞 B. 吞噬细
- 在恒容密闭容器中,NH3和NO在一定条件下发生如下反应: 2NH3(g) +NO(g)2N2(g) + 3H2O(g)
- —Would you like something about my foreign teacher? —Oh, I
- 下列物质中存在离子键、共价键和配位键的是() A.Na2O2
- 对于常数、,“”是“方程的曲线是椭圆”的( ) A.充分不必要条件 B
- 植物种子内所含物质氧化时,每克物质完全氧化释放能量最多的是() A.水 B.糖类 C.脂肪 D.
- 下列关于生物工程相关的叙述,不正确的是( ) A. 限制性内切酶和DNA连接酶作用的部位相同,但解开DNA的双螺旋
- 解不等式组:
- --What happened to you this morning? -- The teacher asked me
- 关于声音,下列说法中正确的是: A、我们能区分出小提琴和二胡的声音,是因为它们发出声音的音调不同; B、我们无法听到蝴蝶
- 阅读下面的文言文,完成下列小题。 来护儿,字崇善,未识而孤,养于世母吴氏.吴氏提携鞠养,甚有慈训,幼儿卓荦;初读《诗》,
- 欲将蛋白质从水溶液中析出而又不改变蛋白质的性质,应加入的试剂是A.溶液 B.(NH4)2SO4溶液 C.CuSO
- 以“仰望天空”为题,写一篇文章。要求:(1)不少于800字。(2)不要写成诗歌。(3)不得透露个人相关信息。
- The car factory has produced a new car of high quality; its
- 下列计算结果正确的是( ) A. B. C.
- 读下图,回答下列问题。(共16分) (1)若一艘轮船航行至A处附近时恰好日出,此时北京时间为19:00,则A点的昼
- 下图为某中学夏令营开展野外考察活动时,准备的活动区等高线地形图,读图回答4—5题。4.下列说法正确的是( ) A.山






