高考二轮复习知识点:难溶电解质的溶解平衡及沉淀转化的本质5
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 多选题 | 详细信息 |
|
下列说法正确的是( )
A . 在NaHS溶液中滴入少量的CuCl2溶液产生黑色沉淀,HS﹣电离程度增大,反应后溶液pH减小
B . 浑浊的苯酚试液中加入饱和Na2CO3溶液变澄清,则酸性:苯酚>碳酸
C . 在等浓度NaCl和Na2CrO4稀溶液中滴加AgNO3溶液,先析出AgCl,则Ksp(AgCl)<Ksp(Ag2CrO4)
D . 等体积、物质的量浓度的HA与NaA(HA为弱酸)混合溶液,其酸碱性取决于Ka(HA)的大小
|
|
| 2. 多选题 | 详细信息 | |||||||||||||||
|
下列根据实验操作或现象得出的结论正确的是( )
A . A
B . B
C . C
D . D
|
||||||||||||||||
| 3. 多选题 | 详细信息 | |||||||||||||||
|
根据下列实验操作和现象所得到的结论正确的是( )
A . A
B . B
C . C
D . D
|
||||||||||||||||
| 4. 多选题 | 详细信息 |
|
常温下,分别向体积均为
 、浓度均为 、浓度均为  的 的  和 和  溶液中滴加 溶液中滴加  的 的  溶液,滴加过程中溶液 溶液,滴加过程中溶液  和 和  与滴入 与滴入  溶液体积( 溶液体积( 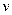 )的关系如图所示。[已知: )的关系如图所示。[已知:  , ,  ,忽略溶液混合时温度和体积的变化],下列说法错误的是( ) ,忽略溶液混合时温度和体积的变化],下列说法错误的是( )
A . 加入过量难溶
 可除去 可除去  溶液中混有的 溶液中混有的  B . e点纵坐标约为13.5
C . d点钾离子的物质的量浓度
B . e点纵坐标约为13.5
C . d点钾离子的物质的量浓度  D . 溶液的pH:d>c>a
D . 溶液的pH:d>c>a
|
|
| 5. 单选题 | 详细信息 |
|
已知相同温度下,
 。某温度下,饱和溶液中 。某温度下,饱和溶液中  、 、  、与 、与  的关系如图所示。 的关系如图所示。 下列说法正确的是( )
A . 曲线①代表
 的沉淀溶解曲线
B . 该温度下 的沉淀溶解曲线
B . 该温度下  的 的  值为 值为  C . 加适量
C . 加适量  固体可使溶液由a点变到b点
D . 固体可使溶液由a点变到b点
D .  时两溶液中 时两溶液中 
|
|
| 6. 实验探究题 | 详细信息 | ||||||||||||||
|
某小组探究卤素参与的氧化还原反应,从电极反应角度分析物质氧化性和还原性的变化规律。
|
|||||||||||||||
| 7. 综合题 | 详细信息 |
|
从钒铬锰矿渣(主要成分为
 、 、 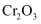 、 、 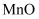 )中提铬的一种工艺流程如下: )中提铬的一种工艺流程如下: 已知:pH较大时,二价锰[
|
|
| 8. 综合题 | 详细信息 |
|
铜冶炼过程中,产生的粗硫酸镍废液中含有
 、 、 、 、 、 、 、 、 等杂质微粒,工业生产以此为原料,精制硫酸镍,主要流程如下: 等杂质微粒,工业生产以此为原料,精制硫酸镍,主要流程如下:
已知:常温下,
|
|
| 9. 综合题 | 详细信息 | ||||||||||||||||||
|
镍氢电池是一种新型绿色电池,利用废旧镍氢电池的金属电极芯(主要成分为Ni(OH)2、Co(OH)2及少量铁、铝的氧化物等)生产硫酸镍、碳酸钴工艺流程如下图:
已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
回答下列问题:
|
|||||||||||||||||||
| 10. 实验探究题 | 详细信息 |
|
含硫化合物在生产生活中有重要应用,实验小组对部分含硫化合物进行探究。回答下列问题:
|
|
- 吉林省汪清县第六中学2019-2020学年高二下学期化学6月月考试卷
- 专题28:醇、酚
- 2015-2016学年陕西省汉中市汉台中学高二下学期期中化学试卷
- 2016年高考理综真题试卷(化学部分)(浙江卷)
- 四川省遂宁市2019-2020学年高一上学期化学期末考试试卷
- 2016-2017学年河南省洛阳市高一上学期期末化学试卷
- 2016年福建省厦门市高考化学二模试卷
- 辽宁省辽阳市2019-2020学年高一下学期化学期末考试试卷
- 山东省青岛胶州市2019-2020学年高一下学期化学期末考试试卷
- 江苏省七市(南通、泰州、扬州、徐州、淮安、连云港、宿迁)2020年高考化学6月模拟试卷
- 2015-2016学年贵州省贵安新区三中高一下学期期中化学试卷
- 2018-2019学年上学期期末高一化学测试卷
- 建立于公元前202年的西汉政权首都在( ) A.咸阳B.长安C.洛阳
- 2.下列各句中,没有语病的一句是( )(3分) A.江苏交通厅负责人表示,将认真分析清明假期高速公路通行情况,听取各
- 已知凸多面体的各个面都是正三角形,并且过各顶点的棱数都是P,求P.
- 太阳的能量来自下面的反应:四个质子(氢核)聚变成一个粒子,同时释放出两个正电子和中微子(质量不计),即:。已知粒子的质量
- (2009山东卷理)已知α,β表示两个不同的平面,m为平面α内的 一条直线,则“”是“”的( ) A.
- 下列各句中加线的成语使用不恰当的一句是 ( ) A.青年人应怀有悲天悯人的胸襟,并以正义为前提。 B.他仍然是中国最高
- 在初级精母细胞中不可能出现的染色体行为是() A.联会 B.交叉互换 C.同源染色体分
- 根据下面文字的信息要点,拟一条一句话新闻,再拟一个标题。(一句话新闻不超过25个字,标题不超过12个字) 最近,国家财政
- 2014年我国进一步扩大人民币跃跨境使用,简化跨境贸易结算手续和审核流程,人民币跨境使用有利于( ) ①加强我国对外
- (06全国卷Ⅰ)锄足蟾蚪、雨蛙蝌蚪和蟾蝌蚪均以浮游 生物为食。在条件相同的四个池塘中,每池放养等量的三种蝌蚪,各池蝌蚪总
- Vicky, _____ born in China, lived and practiced law in publi
- 20世纪70年代,我国外交成就辉煌。这一时期下列外交成就取得的时间先后顺序是①中国在联合国的合法席位得到恢复 ②尼克松总
- 下列反应的离子方程式书写正确的是 ( ) A.氯气和水的反应: C12 + H2O == 2H++ C
- 如果∠A和∠B互补,且∠A>∠B,给出下列四个式子:①90°﹣∠B;②∠A﹣90°;③(∠A+∠B)④(∠A﹣∠B)其中
- 根据短文内容填空,每空一词。Dear Mike, We are your parents .We got your le
- 下列粒子的结构示意图中,表示同种元素的粒子的是( )A、①② B、②③ C、③④ D、
- 近年来,我国领导人频繁出该拉美、非洲、中东地区、我国与阿拉伯国宵、非洲、太平洋岛国和加勒比海地区国家建立多种合作论坛。至
- 有下列应用或实验现象:①在玻璃生产车间里,利用有真空吸盘的吊车吊运平板玻璃;②将两个表面光滑的铅块相互压紧后,能悬挂若干
- (2015届湖北黄冈中考)阅读下面的文字,完成后面题目。 【甲】庆历四年春,滕子京谪守巴陵郡。越明年,政通人和,百废具兴
- 下图海底地形中,表示大陆架的是( )A、① B、② C、③ D、④



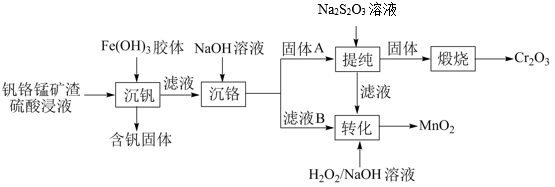
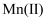 ](在空气中易被氧化.回答下列问题:
](在空气中易被氧化.回答下列问题: 溶液制备
溶液制备  胶体的化学方程式为。
胶体的化学方程式为。
 ]与pH关系如图1。已知钒铬锰矿渣硫酸浸液中
]与pH关系如图1。已知钒铬锰矿渣硫酸浸液中  ,“沉钒”过程控制
,“沉钒”过程控制 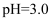 ,则与胶体共沉降的五价钒粒子的存在形态为(填化学式)。
,则与胶体共沉降的五价钒粒子的存在形态为(填化学式)。 
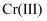 、
、 
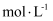 (
(  近似为
近似为 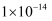 ,
,  的
的  近似为
近似为  )。
)。
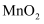 的离子方程式为。
的离子方程式为。
 的作用为。
的作用为。





 的作用是。
的作用是。 的目的是通过调pH进一步去除
的目的是通过调pH进一步去除 , 使
, 使
 。若溶液2中
。若溶液2中
 的操作是。
的操作是。

 的方案。
的方案。 溶液与
溶液与 粉末反应;Ⅱ.Cu粉与浓
粉末反应;Ⅱ.Cu粉与浓
 反应产物的影响,进行如下实验。
反应产物的影响,进行如下实验。 为白色难溶于水的固体,能溶于
为白色难溶于水的固体,能溶于 为白色固体,微溶于水,不易分解。
为白色固体,微溶于水,不易分解。 ;将一定质量
;将一定质量 的
的 的
的 , 则该步骤产生的白色沉淀为(填化学式)。
, 则该步骤产生的白色沉淀为(填化学式)。


