近三年高考化学真题分类汇编:电解质溶液(2022年)
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | 详细信息 |
|
水溶液呈酸性的盐是( )
A . NH4Cl
B . BaCl2
C . H2SO4
D . Ca(OH)2
|
|
| 2. 单选题 | 详细信息 |
|
下列物质属于非电解质的是( )
A . CH4
B . KI
C . NaOH
D . CH3COOH
|
|
| 3. 单选题 | 详细信息 |
|
已知25℃时二元酸H2A的Ka1=1.3×10-7 , Ka2=7.1×10-15。下列说法正确的是( )
A . 在等浓度的Na2A、NaHA溶液中,水的电离程度前者小于后者
B . 向0.1mol·L-1的H2A溶液中通入HCl气体(忽略溶液体积的变化)至pH=3,则H2A的电离度为0.013%
C . 向H2A溶液中加入NaOH溶液至pH=11,则c(A2-)>c(HA-)
D . 取pH=a的H2A溶液10mL,加蒸馏水稀释至100mL,则该溶液pH=a+1
|
|
| 4. 单选题 | 详细信息 |
|
某同学在两个相同的特制容器中分别加入20mL0.4mol·L-1Na2CO3溶液和40mL0.2mol·L-1NaHCO3溶液,再分别用0.4mol·L-1盐酸滴定,利用pH计和压力传感器检测,得到如图曲线:
下列说法正确的的是( )
A . 图中甲、丁线表示向NaHCO3溶液中滴加盐酸,乙、丙线表示向Na2CO3溶液中滴加盐酸
B . 当滴加盐酸的体积为V1mL时(a点、b点),所发生的反应用离子方程式表示为:HCO
 +H+=CO2↑+H2O
C . 根据pH—V(HCl)图,滴定分析时,c点可用酚酞、d点可用甲基橙作指示剂指示滴定终点
D . Na2CO3和NaHCO3溶液中均满足:c(H2CO3)-c(CO +H+=CO2↑+H2O
C . 根据pH—V(HCl)图,滴定分析时,c点可用酚酞、d点可用甲基橙作指示剂指示滴定终点
D . Na2CO3和NaHCO3溶液中均满足:c(H2CO3)-c(CO )=c(OH-)-c(H+) )=c(OH-)-c(H+)
|
|
| 5. 单选题 | 详细信息 |
|
常温下,一元酸
 的 的 。在某体系中, 。在某体系中, 与 与 离子不能穿过隔膜,未电离的 离子不能穿过隔膜,未电离的 可自由穿过该膜(如图所示)。 可自由穿过该膜(如图所示)。
设溶液中
A . 溶液Ⅰ中
 B . 溶液Ⅱ中的
B . 溶液Ⅱ中的 的电离度 的电离度 为 为 C . 溶液Ⅰ和Ⅱ中的
C . 溶液Ⅰ和Ⅱ中的 不相等
D . 溶液Ⅰ和Ⅱ中的 不相等
D . 溶液Ⅰ和Ⅱ中的 之比为 之比为
|
|
| 6. 综合题 | 详细信息 | |||||||||||||||||||||||||
|
废旧铅蓄电池的铅膏中主要含有
 、 、 、 、 和 和 , 还有少量 , 还有少量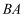 、 、 、 、 的盐或氧化物等。为了保护环境、充分利用铅资源,通过下图流程实现铅的回收。 的盐或氧化物等。为了保护环境、充分利用铅资源,通过下图流程实现铅的回收。
一些难溶电解质的溶度积常数如下表:
一定条件下,一些金属氢氧化物沉淀时的
回答下列问题:
|
||||||||||||||||||||||||||
| 7. 实验探究题 | 详细信息 | ||||||||||||||||||||||||||||||||||||||||
|
食醋是烹饪美食的调味品,有效成分主要为醋酸(用
 表示)。 表示)。  的应用与其电离平衡密切相关。25℃时, 的应用与其电离平衡密切相关。25℃时,  的 的  。 。
|
|||||||||||||||||||||||||||||||||||||||||
| 8. 实验探究题 | 详细信息 | |||||||||||||||
|
稀土(
已知:月桂酸
|
||||||||||||||||
| 9. 实验探究题 | 详细信息 |
|
铬及其化合物在催化、金属防腐等方面具有重要应用。
|
|
| 10. 单选题 | 详细信息 |
|
室温时,用
 的标准 的标准  溶液滴定 溶液滴定  浓度相等的 浓度相等的  、 、  和 和  混合溶液,通过电位滴定法获得 混合溶液,通过电位滴定法获得  与 与  的关系曲线如图所示(忽略沉淀对离子的吸附作用)。 的关系曲线如图所示(忽略沉淀对离子的吸附作用)。 若溶液中离子浓度小于  时,认为该离子沉淀完全。 时,认为该离子沉淀完全。  , ,  , ,  )。 )。
下列说法正确的是( )
A . a点:有白色沉淀生成
B . 原溶液中
 的浓度为 的浓度为  C . 当
C . 当  沉淀完全时,已经有部分 沉淀完全时,已经有部分  沉淀
D . b点: 沉淀
D . b点: 
|
|
- 2015-2016学年江苏省盐城市建湖二中高一下学期期中化学试卷
- 备考2019年高考化学二轮专题 04 离子反应
- 新疆昌吉市教育共同体四校2017-2018学年高二下学期化学期末考试试卷
- 2016-2017学年江苏省扬中、六合、句容、省溧、中华、江浦、华罗庚七校联考高三上学期期中化学试卷
- 2016-2017学年福建省福州市八县一中联考高二上学期期中化学试卷
- 2016-2017学年江西省吉安三中高二上学期期中化学试卷
- 2018年高考化学真题试卷(江苏卷)
- 吉林省蛟河市朝鲜族中学校2019-2020学年高二上学期化学期中考试试卷
- 浙江省“七彩阳光”新高考研究联盟2017-2018学年高一上学期化学期中考试试卷
- 陕西省榆林市2020年高考理综-化学3月线上模拟试卷
- 2015-2016学年河南省开封市兰考二中高二上学期期末化学试卷
- 2017年高考化学备考复习专题二:化学常用计量
- 5.下列各句中,没有语病的一项是( ) A.世界近代史证明,如果一个民族完全遗忘了自己的过去,那么必将失去自己的独立
- —Miss Broun is very busy, isn’t she? —So she is.She has
- 重庆一中渝北分校积极组织学生开展课外阅读活动,为了解全校学生每周课 外阅读的时间量t(单位:小时),采用随机抽
- .若点M的坐标是(a,b),且a>0,b<0,则点M在( ) A.第一象限;B.第二象限;C.第三象限
- 设是定义域为,最小正周期为的函数,若 则等于( ) A. B. C. D.
- 元朝时,专门负责管理全国佛教事务和藏族地区军政事务的机构是 A.中书省 B.行中书省 C.
- 如图所示,半径分别为R和r的甲、乙两个光滑的圆形轨道安置在同一竖直平面上,轨道之间有一条水平轨道CD相通,一小球以一定的
- 下列各句中没有语病的一项是( ) A.由于团省委的一系列关爱活动,使留守儿童感受到了人家庭的温暖。 B.我
- (本题满分8分)已知函数的最大值为. (Ⅰ)求常数的值; (Ⅱ)求函数的单调递增区间; (Ⅲ)若将的图象向左平移个单位,
- 第二节 根据短文内容,从短文后的选项中选出能填入空白处的最佳选项.选项中有两项为多余选项(共5小题;每小题2分,满分10
- 在下面一段文字横线处补写恰当的语句,使整段文字语意完整连贯,内容贴切,逻辑严密。每处不超过 15个字。 光,是人类的好朋
- 下列叙述错误的是 A.油脂属于脂类 B.油脂有固定的熔点C.油脂属于混合物 D.油脂的氢化也叫油脂的硬化
- 设,为坐标原点,动点满足,,则的最大值是 ( ) A.-1 B. 1
- 已知,求代数式的值。
- 今夜偏知春气暖,___________________。(刘方平《月夜》)
- (2015届湖北黄冈中考)古诗词名句填写 (1)独坐幽篁里,__________。(王维《竹里馆》) (2)______
- 在图2中小球均处于静止状态,a、b板都和小球接触。A图中b板在竖直位置,其它B、C、D图中b板均在水平位置。不计一切摩擦
- 开辟新航路的著名航海家迪亚士曾这样说道:“(海上探险)是为了像所有的男子汉都欲做到的那样,为上帝和陛下服务,将光明带给那
- --- What about___________concert? --- It was too boring,
- 党的十八大提出,要树立高度的文化自觉和文化自信,扎实推进社会主义文化强国建设。二十世纪以来中国文化的身影在哪里?不能说这


 , 当达到平衡时,下列叙述正确的是( )
, 当达到平衡时,下列叙述正确的是( )








 如下表:
如下表:



 的原因。
的原因。
 ),还要加入
),还要加入 。
。 , 其化学方程式为;
, 其化学方程式为; 的
的  溶液的体积为mL。
溶液的体积为mL。

 浓度,
浓度,  的
的  溶液,按下表配制总体积相同的系列溶液;测定
溶液,按下表配制总体积相同的系列溶液;测定  ,记录数据。
,记录数据。



 ,
,  。
。 的增加,
的增加,  的值逐渐接近
的值逐渐接近  。
。
 配制的溶液中,
配制的溶液中,  与资料数据
与资料数据  存在一定差异;推测可能由物质浓度准确程度不够引起,故先准确测定
存在一定差异;推测可能由物质浓度准确程度不够引起,故先准确测定  溶液,加入2滴酚酞溶液,用
溶液,加入2滴酚酞溶液,用  溶液滴定至终点,消耗体积为
溶液滴定至终点,消耗体积为  ,则该
,则该  。在答题卡虚线框中,画出上述过程的滴定曲线示意图并标注滴定终点。
。在答题卡虚线框中,画出上述过程的滴定曲线示意图并标注滴定终点。 溶液,如何准确测定
溶液,如何准确测定 

 熔点为
熔点为  ;月桂酸和
;月桂酸和  均难溶于水。该工艺条件下,稀土离子保持
均难溶于水。该工艺条件下,稀土离子保持  价不变;
价不变;  的
的  ;
;  开始溶解时的pH为8.8;有关金属离子沉淀的相关pH见下表。
开始溶解时的pH为8.8;有关金属离子沉淀的相关pH见下表。



 元素,滤液2中
元素,滤液2中  。为尽可能多地提取
。为尽可能多地提取  低于
低于  。
。  和
和  熔融盐制备
熔融盐制备  电子。
电子。 用作氢氧燃料电池电极材料时,能在碱性溶液中高效催化
用作氢氧燃料电池电极材料时,能在碱性溶液中高效催化  的还原,发生的电极反应为。
的还原,发生的电极反应为。 可由
可由  加热分解制备,反应同时生成无污染气体。
加热分解制备,反应同时生成无污染气体。 
 。
。 过程的焓变为(列式表示)。
过程的焓变为(列式表示)。
 的催化氧化。设计从
的催化氧化。设计从  的路线(用“→”表示含氮物质间的转化);其中一个有颜色变化的反应的化学方程式为。
的路线(用“→”表示含氮物质间的转化);其中一个有颜色变化的反应的化学方程式为。 溶液中存在多个平衡。本题条件下仅需考虑如下平衡:
溶液中存在多个平衡。本题条件下仅需考虑如下平衡: 



 与
与  的比值保持不变
的比值保持不变 时,
时,  溶液中
溶液中  随pH的变化关系如图2。当
随pH的变化关系如图2。当  时,设
时,设  、
、  与
与  的平衡浓度分别为x、y、z
的平衡浓度分别为x、y、z  ;计算溶液中
;计算溶液中 
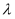 )有关;在一定波长范围内,最大A对应的波长(
)有关;在一定波长范围内,最大A对应的波长(  )取决于物质的结构特征;浓度越高,A越大。混合溶液在某一波长的A是各组分吸收程度之和。为研究pH对反应(ⅰ)和(ⅱ)平衡的影响,配制浓度相同、
)取决于物质的结构特征;浓度越高,A越大。混合溶液在某一波长的A是各组分吸收程度之和。为研究pH对反应(ⅰ)和(ⅱ)平衡的影响,配制浓度相同、  稀溶液,测得其A随
稀溶液,测得其A随  、
、  和
和  中,与
中,与  的值(填“增大”“减小”或“不变”)。
的值(填“增大”“减小”或“不变”)。


