高考二轮复习知识点:盖斯定律及其应用4
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | 详细信息 |
|
Zn还原SiCl4的反应如下:下列说法正确的是( )
SiCl4(g)+2Zn(l)⇌Si(s)+2ZnCl2(g)△H1 SiCl4(g)+2Zn(g)⇌Si(s)+2ZnCl2(g)△H2 .
A . Zn(l)=Zn(g)△H=
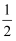 (△H1﹣△H2 )
B . 用硅制作的太阳能电池是将化学能转化为电能
C . 增加Zn(g)的量,△H2变大
D . 以Zn片、铜片和稀硫酸构成的原电池,Zn片表面有气泡产生. (△H1﹣△H2 )
B . 用硅制作的太阳能电池是将化学能转化为电能
C . 增加Zn(g)的量,△H2变大
D . 以Zn片、铜片和稀硫酸构成的原电池,Zn片表面有气泡产生.
|
|
| 2. 单选题 | 详细信息 |
|
已知:2C(s)+O2(g)═2CO(g)△H=﹣217kJ•mol﹣1
C(s)+H2O(g)═CO(g)+H2(g)△H=bkJ•mol﹣1 H﹣H,O﹣H和O=O键的键能分别为436、462和495kJ•mol﹣1 , 则b为( )
A . +352
B . +132
C . ﹣120
D . ﹣330
|
|
| 3. 单选题 | 详细信息 |
|
通过以下反应均可获取H2 . 下列有关说法正确的是( )
①太阳光催化分解水制氢:2H2O(l)═2H2(g)+O2(g)△H1=571.6kJ•mol﹣1 ②焦炭与水反应制氢:C(s)+H2O(g)═CO(g)+H2(g)△H2=131.3kJ•mol﹣1 ③甲烷与水反应制氢:CH4(g)+H2O(g)═CO(g)+3H2(g)△H3=206.1kJ•mol﹣1 .
A . 反应①中电能转化为化学能
B . 反应②为放热反应
C . 反应③使用催化剂,△H3减小
D . 反应CH4(g)═C(s)+2 H2(g)的△H=74.8kJ•mol﹣1
|
|
| 4. 单选题 | 详细信息 |
|
用CO通过下列方法可以合成甲醇。
①CO2(g)+2H2O(l) === CH3OH(g)+ ②CO(g)+ ③H2(g)+ 下列有关说法正确的是( )
A . 反应①使用催化剂可以提高甲醇产率
B . 反应②在任何条件下均能自发进行
C . 反应③在100℃时ΔH<-285.8 kJ·mol-1
D . 反应CO(g)+2H2(g)
|
|
| 5. 综合题 | 详细信息 |
|
氮元素的氢化物和氧化物在工业生产和国防建设中都有广泛应用,回答下列问题:
|
|
| 6. 综合题 | 详细信息 |
|
(14分)丁烯是一种重要的化工原料,可由丁烷催化脱氢制备.回答下列问题:
|
|
| 7. 单选题 | 详细信息 |
|
在好氧菌和厌氧菌作用下,废液中NH4+能转化为N2(g)和H2O(l),示意图如下:
反应I 反应Ⅱ 下列说法正确的是( )
A . 两池发生的反应中,氮元素只被氧化
B . 两池中投放的废液体积相等时,NH4+能完全转化为N2
C . 常温常压下,反应Ⅱ中生成22.4LN2转移的电子数为3.75×6 02×1023
D .

|
|
| 8. 单选题 | 详细信息 |
|
下图是通过热化学循环在较低温度下由水或硫化氢分解制备氢气的反应系统原理,下列说法错误的是( )
A . 反应②为反应③提供了原料
B . 反应②也是SO2资源利用的方法之一
C . 制得等量H2所需能量较少的是系统(I)
D . 系统(I)制氢的热化学方程式为H2O(l) = H2(g) + 1/2O2(g) ΔH = +286 kJ/mol
|
|
| 9. 单选题 | 详细信息 |
|
联氨(N2H4)常温下为无色液体,可用作火箭燃料。下列说法错误的是( )
① 2O2(g)+N2(g)=N2O4(l) ΔH1 ② N2(g)+2H2(g)=N2H4(l) ΔH2 ③ O2(g)+2H2(g)=2H2O(g) ΔH3 ④ 2 N2H4(l)+N2O4(l)=3N2(g)+4H2O(g) ΔH4=﹣1048.9 kJ·mol-1
A . O2(g)+2H2(g)=2H2O(l) ΔH5 , ΔH5>ΔH3
B . ΔH4﹦2ΔH3﹣2ΔH2﹣ΔH1
C . 1 mol O2(g) 和2 mol H2(g)具有的总能量高于2 mol H2O(g)
D . 联氨和N2O4作火箭推进剂的原因之一是反应放出大量的热
|
|
| 10. 综合题 | 详细信息 |
|
甲醇是一种重要的液体清洁燃料,工业上有多种制备甲醇的方法。
|
|
- 高中化学人教版 选修四 第二章 化学反应速率和化学平衡 第三节 化学平衡 化学平衡第一课时(可逆反应)
- 辽宁省沈阳市郊联体2018-2019学年高三上学期化学期末考试试卷
- 2016-2017学年江西省赣州市十三县(市)联考高二上学期期中化学试卷
- 2015-2016学年安徽省师大附中高一上学期期中化学试卷
- 北京师大附中2018-2019学年高一下学期化学期末考试试卷
- 第21讲:水溶液和弱电解质的电离
- 甘肃省宁县2018-2019学年高二上学期化学期末考试试卷
- 天津市滨海新区塘沽第一中学2019-2020学年高一下学期化学第一次月考试卷
- 第20讲:化学平衡的应用
- 河南省开封市2019-2020学年高二下学期化学期末考试试卷
- 安徽省滁州市明光中学2019-2020学年高二下学期化学开学考试卷
- 浙江省嘉兴市2018-2019学年高二下学期化学期末考试试卷
- 观察下列图形,是中心对称图形的是 A. B. C.
- 下列A栏是制取有关分散系的方法,B栏是分散系的种类,请将A栏中相关的题号填写在B栏相应的空格内。A栏:a.向Na2S溶液
- 把平凡的工作做好就是不平凡,把普通的工作做好就是不普通。其中蕴含的哲学观点是 A.矛盾双方的相互排斥和对立 B.
- For the loveof reading Theimportance of nurturing (培养) youn
- 小王一月收入5000多元,近日贷款买了辆轿车,月供2400元。小赵和小王是同学,无业在家,见小王买了新车,自己觉得很没面
- 宋代苏轼在《格物粗谈•果品》中记载“红柿摘下未熟,每篮用木瓜三枚放入,得气即发,并无涩味”.上述叙述中“得气即发”的“气
- 若直线到直线的角为,则实数的值等于 ( )A.0 B.
- 已知线段AB=10cm,点C是直线AB上一点,BC=4cm,若M是AC的中点,N是BC的中点,则线段MN的长度是() A
- 下列过程中有化学键断裂的同时,又有化学键形成的是 A.石墨转化为金刚石 B.碘升华 C.N
- 化学在生活中有着广泛的应用,下列对应关系错误的是( ) 化学性质 实际应用 A. Al2(SO4)3和小苏打反应 泡
- 若将三个数-,,表示在数轴上,其中介于2和3之间的数是_____。
- 新生命的孕育要经过复杂的过程,结合如图叙述不正确的是()A.①能产生卵细胞并分泌雌性激素 B.精子在②中与卵细胞结合成受
- 在以下说法中,正确的是: A.分子间距离为平衡距离时,分子势能最小 B.热量可能自发地从低温物体传到高温物体 C.晶
- 2.下列关于细胞的描述,正确的是 A.叶肉细胞
- 孙中山领导的辛亥革命推翻了中国两千多年的帝制,但革命的果实很快就被谁窃取了?
- 已知当时,函数的图像与的图像有且只有一个交点,则正实数的取值范围是 A. B
- 责任是 A.一个人应当做到事情 B.一个人应当做到事情和不应该做某些事情 C.想做什么就做什么 D.父母不让做非要做
- 下列四个选项中,字形和加点字字音全部正确的一组是( ) A.张牙舞爪(zhǎo) 教坊(fáng) 孝悌(tì)
- 直到19世纪初,德国人还自嘲说英国拥有海洋,法国拥有陆地,而德国只有“思想的天空”。德国在拥有“思想的天空”方面的主要成
- 下列句子中没有语病的一项是( ) A.上网的诱惑无法令现代人拒绝,但昂贵的网上消费又使网迷们心痛不已。 B.只要把自己所
 O2(g) ΔH1=+764.5 kJ·mol-1
O2(g) ΔH1=+764.5 kJ·mol-1 O2(g)===CO2(g) ΔH2=-283.0 kJ·mol-1
O2(g)===CO2(g) ΔH2=-283.0 kJ·mol-1




 CHOH(g)+ H2O(g) ∆H<0
CHOH(g)+ H2O(g) ∆H<0 = 3。
= 3。



