高考二轮复习知识点:化学平衡的计算2
高考二轮复习知识点:化学平衡的计算2
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 多选题 | 详细信息 | |||||||||||||||||||||||||||||||
|
在3个初始温度均为T℃的密闭容器中发生反应:2SO2(g)+O2(g)
 2SO3(g) (正反应放热)。下列说法正确的是( ) 2SO3(g) (正反应放热)。下列说法正确的是( )
A . a>1.6
B . b<0.8
C . 平衡时v正(SO2):v(I)<v(II)
D . 若起始时向容器I中充入1.0 mol SO2(g)、0.20 mol O2(g)和4.0molSO3(g),则反应将向正反应方向进行
|
||||||||||||||||||||||||||||||||
| 2. 多选题 | 详细信息 |
|
向起始温度为298K的10L刚性恒容密闭容器中充入1molNO和1molH2发生反应:2NO(g)+2H2(g)
 N2(g)+2H2O(g) N2(g)+2H2O(g)  。已知①体系内总压强(P)与时间(t)的关系如图所示: 。已知①体系内总压强(P)与时间(t)的关系如图所示: ②曲线中平衡时的温度与起始时的温度相同。 则下列说法中错误的是( )
A . 该反应的
 B . 0~10min内
B . 0~10min内  C . 298K时,该反应的平衡常数
C . 298K时,该反应的平衡常数  D . 10min时反应达到平衡,NO的转化率为80%
D . 10min时反应达到平衡,NO的转化率为80%
|
|
| 3. 多选题 | 详细信息 | ||||||||||||||||||||||||||||||||
|
一定温度下,在三个容积相同的恒容密闭容器中按不同方式投入反应物,发生反应2SO2(g)+ O2(g) ⇌2SO3(g)(正反应放热),测得反应的相关数据如下:
下列说法正确的是( )
A . v1< v2 , c2< 2c1
B . K1> K3 , p2> 2p3
C . v1< v3 , α1(SO2 ) >α3(SO2 )
D . c2> 2c3 , α2(SO3 )+α3(SO2 )<1
|
|||||||||||||||||||||||||||||||||
| 4. 多选题 | 详细信息 |
|
一定条件下,在
 的平衡体系中,X、Y、Z的浓度分别是2 mol/L,0.8 mol/L、2.4 mol/L,则X在起始时的浓度不可能是( ) 的平衡体系中,X、Y、Z的浓度分别是2 mol/L,0.8 mol/L、2.4 mol/L,则X在起始时的浓度不可能是( )
A . 3 mol/L
B . 0.2 mol/L
C . 4.4 mol/L
D . 4.8 mol/L
|
|
| 5. 多选题 | 详细信息 | ||||||||||||||||||||||||
|
相同温度下,分别在起始体积均为1L的两个密闭容器中发生反应:X2(g)+3Y2(g)⇌2XY3(g)△H=-akJ/mol。实验测得反应的有关数据如表。
下列叙述正确的是( )
A . 对于上述反应,①、②中反应的平衡常数K的值相同
B . ①中:从开始至10min内的平均反应速率υ(X2)=0.1mol/(L•min)
C . ②中:X2的平衡转化率小于10%
D . b>0.1a
|
|||||||||||||||||||||||||
| 6. 多选题 | 详细信息 |
|
对于
 , 一定条件下,将 , 一定条件下,将 X和 X和  通入 通入 的恒容密闭容器中,反应到 的恒容密闭容器中,反应到 时,测得Y的物质的量为 时,测得Y的物质的量为 , 当反应达到平衡时测得放出 , 当反应达到平衡时测得放出 热量,下列说法正确的是( ) 热量,下列说法正确的是( )
A . 第
 时,Y的反应速率为 时,Y的反应速率为 B . 前
B . 前 内,X的转化率为 内,X的转化率为 C . 当有
C . 当有 参与反应时,放出的热量为 参与反应时,放出的热量为 D . 达到化学平衡状态时,
D . 达到化学平衡状态时, 正 正  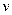 逆 逆 , 且Z的浓度不再变化 , 且Z的浓度不再变化
|
|
| 7. 综合题 | 详细信息 | |||||||||||||||||||
|
某空间站的生命保障系统功能之一是实现氧循环,其中涉及反应:
 回答问题:
|
||||||||||||||||||||
| 8. 多选题 | 详细信息 | ||||||||||||||||||||
|
在一体积为2 L的密闭容器中加入反应物N2、H2 , 发生如下反应:N2(g)+3H2(g)
 2NH3(g)。反应过程中的部分数据如表所示,下列说法正确的是( ) 2NH3(g)。反应过程中的部分数据如表所示,下列说法正确的是( )
A . 0~2 min内,NH3的反应速率为0.05 mol·L-1·min-1
B . 2 min时,H2的物质的量为0.3 mol
C . 4 min时,反应已达到平衡状态,此时正、逆反应的速率都为0
D . 4~6 min内,容器内气体的总物质的量不变
|
|||||||||||||||||||||
| 9. 多选题 | 详细信息 |
|
在一恒温恒容密闭容器中充入
 和 和 , 一定条件下发生反应: , 一定条件下发生反应: , 测得 , 测得 和 和 的浓度随时间变化如图所示。下列说法正确的是( ) 的浓度随时间变化如图所示。下列说法正确的是( )
A . 反应进行到3min时,该反应达到平衡状态
B . 从反应开始到平衡,
 的转化率为75%
C . 的转化率为75%
C .  , 氢气的平均反应速率为 , 氢气的平均反应速率为 D . 反应进行到10min时,该反应放出热量49.0kJ
D . 反应进行到10min时,该反应放出热量49.0kJ
|
|
| 10. 多选题 | 详细信息 |
|
在容积为2L的恒容密闭容器中充入
 、 、 , 在不同温度下发生反应: , 在不同温度下发生反应: , 测得 , 测得 的转化率与时间的关系如下图所示。下列说法正确的是 ( ) 的转化率与时间的关系如下图所示。下列说法正确的是 ( )
A .
 时, 时, 时的反应速率大于 时的反应速率大于 时,其中 时,其中 时 时 B .
B .  时的反应平衡常数 时的反应平衡常数 C .
C .  时,当容器中气体密度不再发生变化时,反应到达平衡状态
D . 时,当容器中气体密度不再发生变化时,反应到达平衡状态
D .  时,若起始向容器中加入催化剂,2s时, 时,若起始向容器中加入催化剂,2s时, 的转化率可能到达图中X点 的转化率可能到达图中X点
|
|
高中化学 试卷推荐
- 吉林省吉林市2018-2019学年高考理综-化学三模考试试卷
- 安徽省宣城市2019-2020学年高二上学期期末考试化学试题
- 安徽省A10联盟2019-2020学年高三下学期化学开学考试卷
- 广东省佛山市2017-2018学年高三理综-化学第二次模拟考试试卷
- 湖北省武汉2017-2018学年高二上学期化学期末考试试卷
- 2016年浙江省宁波市镇海中学高考化学一模试卷
- 安徽省安庆市太湖中学2017-2018学年高三上学期化学第三次月考考试试卷
- 2015-2016学年北京市东城区重点中学高三上学期期中化学试卷
- 专题9:铜及其化合物、金属冶炼一般原理
- 山西省运城市芮城县2018-2019学年高二上学期化学期末考试试卷
- 福建省南平市2019-2020学年高二下学期化学期末考试试卷
- 2016-2017学年陕西省咸阳市百灵中学高一上学期期中化学试卷
最近更新
- John says he’s 80 years old, but nobody ______him. A.bel
- . As a new graduate, he doesn’t know_______it takes to start
- 已知,函数,若满足关于的方程,则下列选项的命题中为假命题的是( ) A. B. C.
- 有关皮肤的叙述中,正确的是( ) A、皮肤大面积烧伤病人的非特异性免疫能力下降 B、注射青霉素前进行的“皮试”是将
- 小张按1美元兑换8元人民币的汇率换得1000美元,两年后美元兑换人民币的汇率下跌了20%。小张又将1000美元换回人民币
- 继昌隆缫丝厂和安庆军械所的根本区别是( ) A.企业生产的性质
- (8分)氢能是21世纪极具开发前景的新能源之一,它既是绿色能源,又可循环利用。请在下图的两个空框中填上循环过程中反应物和
- 依次填入下面这段文字横线处的词语,最恰当的一项是( )(2分) 如果说命运是那破旧的花架,只要意志坚强,它可以
- 移栽树苗时,其根部总是带有一个土坨,这是为了 A.防止秧苗出现萎蔫现象 B.防止秧苗的幼根和
- (4分)(双选)在一个密闭容器中用一可移动板隔开,左边充有氮气,右边充入H2、O2。在室温下用电火花点燃混合气体,反应后
- 读沿北纬36°纬线所做的我国地形剖面图1,回答下列问题:图1 (1)A为第____ 级阶梯,平均海拔_______ 米以
- 函数的定义域是( ) A. B. C. D.
- “北方吹来十月的风,惊醒我们苦兄弟。”与这句话直接有关的信息是 A.五四爱国运动 B.马克思主义在中国的传播
- 民生问题是永恒的焦点,在促进政府解决物价、住房、医疗、教育、就业等民生问题上,人大代表应该() A.行使决定权,对重大民
- 英国在17世纪中期爆发资产阶级革命,曾一度推翻国王、建立共和国;“光荣革命”后君主制经过改造得以保留下来,并逐步形成了为
- 下列句子中文言词语解析错误的一项是 A.以绳天下之梅 (约束)/ 名词用作动词 B.质于齐 (做人质)/ 名词用作动词
- 音调、__▲_____和音色是乐音的三个特征,其中__▲_____是由声源的振动频率决定噪声是当代社会的公害之一,有资料
- 第一部分 英语知识运用(共四节,满分45分) 语音知识(共5小题,每小题1分,满分5分) 从每小题的A、B、C、D四个选
- 下列句子没有语病的一项是( ) A.随着小说获奖的激动逐渐减退,使我开始相信,至少有一点我是想错了。 B.只是到了
- 历史上的标语口号浓缩地表现着不同时代的内容和特征,下列标语口号按其出现的时间先后顺序排列,正确的是 ①“打倒列强,除军阔

 , 电解反应的
, 电解反应的 。由此计算
。由此计算 的燃烧热(焓)
的燃烧热(焓)
 。
。

 与活化能(Ea)的关系为
与活化能(Ea)的关系为 。补充完成该反应过程的能量变化示意图(图2)。
。补充完成该反应过程的能量变化示意图(图2)。
 和
和 , 反应平衡后测得容器中
, 反应平衡后测得容器中 。则
。则 , 在反应器中按
, 在反应器中按 通入反应物,在不同温度、不同催化剂条件下,反应进行到2min时,测得反应器中
通入反应物,在不同温度、不同催化剂条件下,反应进行到2min时,测得反应器中 、
、 浓度(
浓度( )如下表所示。
)如下表所示。



 生成
生成 ;若某空间站的生命保障系统实际选择使用催化剂Ⅱ和400℃的反应条件,原因是。
;若某空间站的生命保障系统实际选择使用催化剂Ⅱ和400℃的反应条件,原因是。




